Lecture 11
Lecture 11: 细胞内区室与蛋白质分选(详细版)
课程:高等生物科学 | 南方科技大学 | 邓怿教授
---
预备知识:理解本讲需要的基础
0.1 蛋白质的基本结构回顾
蛋白质由氨基酸通过肽键(peptide bond)连接而成。每个氨基酸有一个氨基(-NH₂)和一个羧基(-COOH),连接后形成多肽链。多肽链有方向性:N 端(游离氨基端)是合成起始端,C 端(游离羧基端)是合成终止端。核糖体翻译 mRNA 时,总是从 N 端开始,向 C 端延伸。
蛋白质的四级结构:
- 一级结构:氨基酸的线性序列
- 二级结构:局部的规则折叠,主要有α螺旋(α-helix)和β折叠片(β-sheet)
- 三级结构:整条多肽链的三维折叠
- 四级结构:多个亚基的组装
蛋白质的功能高度依赖其三维结构。一个蛋白质如果没有正确折叠,通常会失去功能,甚至形成有毒的聚集体。
0.2 氨基酸的关键性质
本讲中频繁提到的氨基酸性质:
疏水性氨基酸(倾向于远离水,埋在蛋白质内部或嵌入脂双层):
- 亮氨酸(Leu, L)、异亮氨酸(Ile, I)、缬氨酸(Val, V)、丙氨酸(Ala, A)、苯丙氨酸(Phe, F)、甲硫氨酸(Met, M)
带正电的氨基酸(在生理 pH 下带正电荷):
- 赖氨酸(Lys, K)、精氨酸(Arg, R)
半胱氨酸(Cys, C):含 -SH 基团,两个 Cys 可以形成二硫键(-S-S-),对蛋白质折叠和稳定性很重要。
0.3 生物膜的基本性质
细胞膜(包括所有细胞器膜)由磷脂双分子层构成:两层磷脂分子,疏水尾部朝内,亲水头部朝外。这种结构对大多数亲水分子(离子、蛋白质、核酸等)构成了天然屏障。
因此,蛋白质要从细胞质进入一个膜包被的细胞器,要么穿过膜(需要专门的转运通道),要么通过膜泡融合的方式进入。这就是本讲讨论的核心问题。
0.4 GTPase 开关
本讲中多次出现 GTPase(如 SRP/SR 的 GTPase、Ran GTPase)。它们是分子开关:
- GTP 结合态(活化态):GTPase 与效应分子结合,执行功能
- GDP 结合态(失活态):GTPase 释放效应分子
- GEF(鸟嘌呤核苷酸交换因子):促进 GDP → GTP 交换,激活 GTPase
- GAP(GTPase 激活蛋白):刺激 GTP 水解为 GDP + Pi,失活 GTPase
GTPase 循环的本质是利用 GTP 水解的自由能来驱动构象变化,从而控制分子间相互作用的开与关。
0.5 分子伴侣(Molecular Chaperones)
分子伴侣是一类帮助其他蛋白质正确折叠、防止聚集的蛋白质。本讲涉及的分子伴侣:
- Hsp70 家族(如细胞质的 Hsc70、ER 腔内的 BiP、线粒体基质的 mtHsp70):结合暴露的疏水区域,防止错误折叠和聚集。需要消耗 ATP 进行结合-释放循环。
- Hsp90:帮助维持某些蛋白质的折叠状态
- Hsp60/Hsp10(Chaperonin):在线粒体基质中,提供一个封闭的"折叠笼",让蛋白质在隔离环境中正确折叠
0.6 SDS-PAGE 简介
SDS-PAGE(十二烷基硫酸钠-聚丙烯酰胺凝胶电泳)是分离蛋白质的常用方法。SDS 使所有蛋白质带上均一的负电荷,电泳时蛋白质仅按分子量大小分离——分子量越小,跑得越快。本讲中,它被用来区分含信号肽的前体蛋白(较大)和切除信号肽后的成熟蛋白(较小)。
---
第一部分:细胞内区室化(Intracellular Compartmentalization)
1.1 为什么真核细胞需要区室化?
这是一个非常基础但重要的问题。原核细胞(如大肠杆菌)只有约 4000 个基因,所有生化反应都在同一个细胞质空间中进行。真核细胞(如人类细胞约有 20000 个基因)需要更精细的组织方式,区室化提供了以下关键优势:
(1)创造不同的生化环境
不同的反应需要不同的条件。例如:
- 溶酶体内部 pH 约 4.5-5.0(酸性),用于水解酶的最适工作条件;而细胞质 pH 约 7.2。如果这些水解酶泄漏到细胞质中,由于 pH 不适合,活性会大幅降低,从而保护细胞。
- ER 腔是氧化环境(有利于二硫键形成),而细胞质是还原环境。分泌蛋白在 ER 中正确形成二硫键后才能获得功能。
- 线粒体基质维持碱性 pH 和高浓度的辅酶,适合三羧酸循环和脂肪酸氧化。
(2)增加反应效率
将相关的酶集中在一个小的区室内,大大提高了底物和酶的局部浓度。例如:
- 脂肪酸β-氧化的酶集中在过氧化物酶体和线粒体中
- 蛋白质糖基化的酶集中在 ER 和高尔基体中
(3)隔离危险反应
- 过氧化物酶体将产生 H₂O₂ 的氧化反应限制在膜内,防止 H₂O₂ 损伤细胞其他组分
- 溶酶体将降解酶封闭起来,防止不受控的细胞自身降解
(4)提供信号调控平台
许多信号通路依赖于蛋白质在不同区室间的转运。例如,转录因子从细胞质转运到细胞核是基因激活的关键步骤(如后文的 NF-AT 实例)。
1.2 各细胞器详细介绍
以肝细胞(hepatocyte)为例,这是一种功能非常活跃的细胞:
| 区室 | 体积占比 | 详细功能 |
|---|---|---|
| 细胞质(Cytosol) | 54% | 糖酵解、大部分氨基酸合成、脂肪酸合成、蛋白质翻译起始、信号转导、蛋白酶体降解 |
| 线粒体(Mitochondria) | 22% | 氧化磷酸化(ATP 合成)、三羧酸循环、脂肪酸β-氧化、氨基酸代谢、凋亡信号、钙储存 |
| 粗面内质网(Rough ER) | 9% | 分泌蛋白和膜蛋白的合成、信号肽切除、N-糖基化、二硫键形成、蛋白质质量控制 |
| 滑面 ER + 高尔基体 | 6% | 脂质合成(滑面 ER)、糖基化修饰(高尔基体)、蛋白质分选与包装(高尔基体) |
| 细胞核(Nucleus) | 6% | DNA 复制、转录、RNA 加工与剪接、核糖体亚基组装 |
| 过氧化物酶体 | 1% | H₂O₂ 代谢、超长链脂肪酸氧化、缩醛磷脂合成、胆汁酸合成 |
| 溶酶体(Lysosomes) | 1% | 蛋白质、脂质、多糖、核酸的降解;自噬作用 |
| 内体(Endosomes) | 1% | 内吞物质的分选(回收到质膜 vs 送到溶酶体降解) |
值得注意的是,不同类型的细胞,各细胞器的比例差异很大。例如:
- 分泌活跃的细胞(如胰腺腺泡细胞):粗面 ER 和高尔基体非常发达
- 肌肉细胞:线粒体占比更高
- 解毒功能活跃的肝细胞:滑面 ER 和过氧化物酶体更丰富
1.3 真核细胞内膜系统的演化假说(详述)
现代真核细胞的内膜系统是如何演化而来的?目前的主流假说如下:
第一阶段:膜灵活性的获得
- 起始细胞是一个厌氧古菌(anaerobic archaeon)
- 这个古菌的细胞壁发生退化或丧失,使其质膜变得更加灵活
- 细胞壁的丧失使古菌可以更容易地变形和吞噬
第二阶段:水平基因转移加速
- 没有坚硬细胞壁的灵活细胞更容易摄取周围的 DNA
- 来自古菌和细菌的水平基因转移大大增加
- 这加速了演化过程
第三阶段:内膜系统的形成
- 质膜不断向内折叠(invagination),逐渐将基因组 DNA 包裹起来
- 这些内折的膜最终形成了核膜(nuclear envelope)
- 核膜与质膜之间的连续膜结构演化为内质网(ER)
- 这解释了为什么核膜是双层膜,而且外核膜与 ER 是连续的
第四阶段:线粒体的内共生起源
- 一个好氧细菌(aerobic bacterium,可能是α-变形菌的祖先)被吞入宿主细胞
- 但没有被消化,而是存活下来,形成了原始线粒体(promitochondrion)
- 这种共生关系对双方有利:宿主获得了高效的 ATP 产生能力,细菌获得了保护和营养
支持内共生理论的证据:
- 线粒体有自己的环形 DNA(类似细菌基因组)
- 线粒体有自己的核糖体(70S,类似细菌,而非真核的 80S)
- 线粒体的双层膜:内膜来自原始细菌的质膜,外膜来自吞噬时的宿主质膜
- 线粒体的分裂方式类似细菌二分裂
- 线粒体 DNA 的序列与α-变形菌高度相似
第五阶段:细胞复杂性的爆发
- 线粒体提供的充裕 ATP 使细胞能够长得更大
- 更大的细胞需要更复杂的内膜系统来组织各种生化反应
- 高尔基体、溶酶体、内体等膜结构逐渐分化
> 注意:叶绿体的起源也是内共生——一个光合蓝细菌(cyanobacterium)被吞入,这发生在线粒体内共生之后。植物细胞因此同时拥有线粒体和叶绿体。
1.4 蛋白质在不同区室间的运输流程
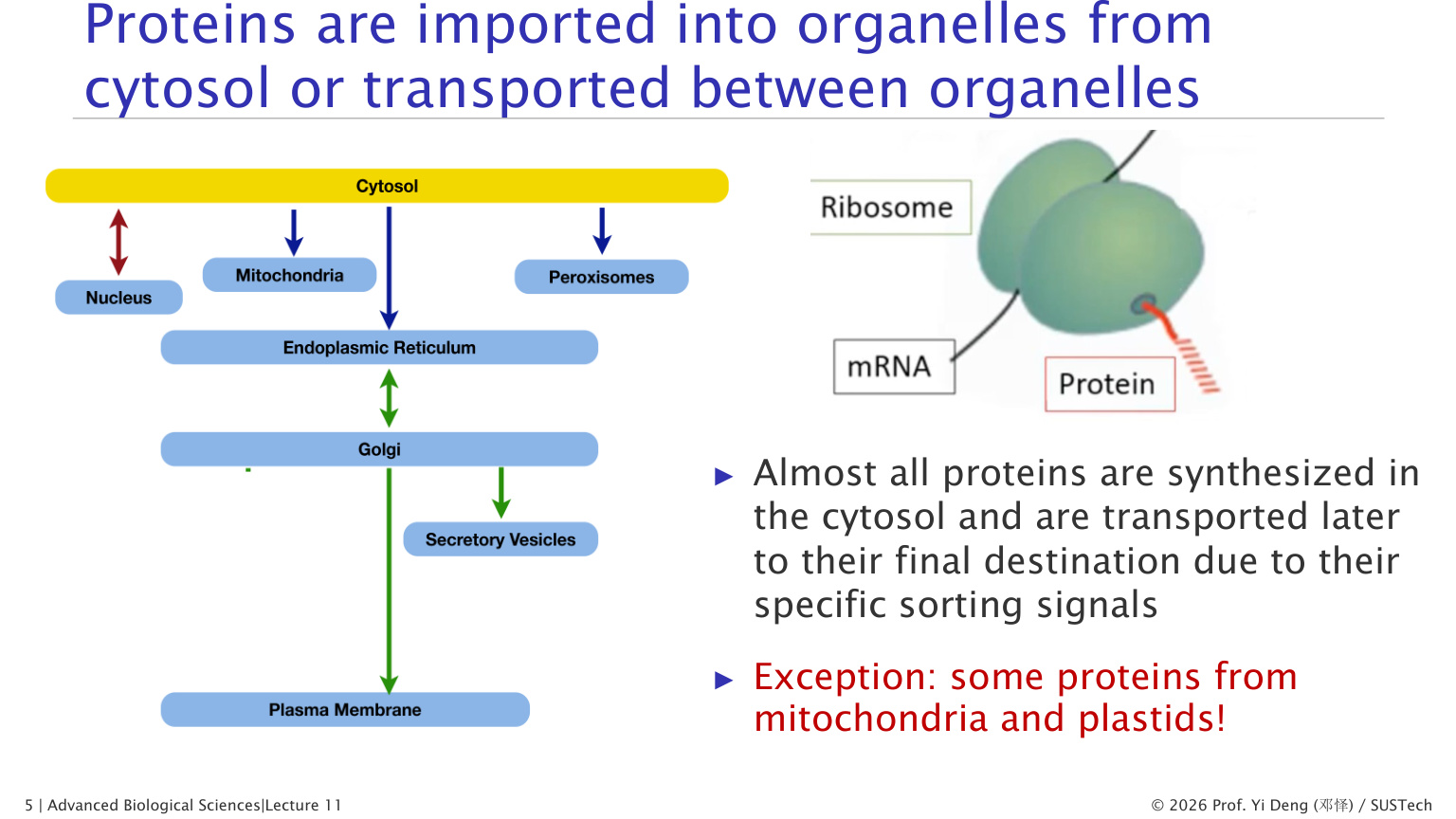
细胞中几乎所有蛋白质的合成都始于细胞质中的游离核糖体。那么,蛋白质如何到达正确的目的地?
关键原则:分选信号决定目的地。
蛋白质的运输路线(从细胞质出发):
┌─→ 细胞核(门控运输,NLS/NES)
│
├─→ 线粒体(跨膜运输,前导序列)
│
细胞质 ────────├─→ 过氧化物酶体(跨膜运输,PTS1/PTS2)
(翻译起始处) │
├─→ 叶绿体(跨膜运输,转运肽)[仅植物]
│
└─→ 内质网(ER)──→ 高尔基体 ──┬→ 溶酶体
(跨膜运输, (囊泡运输)├→ 质膜
信号肽) ├→ 分泌囊泡 → 细胞外
└→ 内体例外情况:
- 线粒体和叶绿体自身基因组编码了一小部分蛋白质(线粒体基因组编码约 13 个蛋白质,其余约 1000-1500 个线粒体蛋白由核基因编码并从细胞质进口)
- 没有任何分选信号的蛋白质默认留在细胞质
1.5 三种运输方式的详细比较
(1)门控运输(Gated transport)
- 路径:细胞质 ↔ 细胞核
- 通道:核孔复合体(NPC)
- 货物状态:蛋白质保持折叠态通过(NPC 孔径足够大,约 40 nm)
- 选择性机制:FG 核孔蛋白形成的选择性屏障 + 核转运受体(importin/exportin)
- 能量:Ran-GTP 梯度
- 特点:双向运输(进口和出口同时发生)
(2)跨膜运输(Transmembrane transport / Protein translocation)
- 路径:细胞质 → ER / 线粒体 / 过氧化物酶体 / 叶绿体
- 通道:蛋白质转运通道(translocator/translocon)
- ER:Sec61
- 线粒体外膜:TOM;内膜:TIM23/TIM22
- 叶绿体:TOC/TIC
- 货物状态:蛋白质必须未折叠才能穿过窄小的通道(例外:过氧化物酶体可进口折叠蛋白)
- 能量:ATP(分子伴侣)、GTP(SRP/SR)、膜电位(线粒体)
- 特点:蛋白质像"蛇"一样穿过膜上的通道
(3)囊泡运输(Vesicular transport)
- 路径:ER → 高尔基体 → 溶酶体/质膜/细胞外;以及内吞途径
- 机制:供体膜出芽(budding)形成运输囊泡,囊泡移动到目标膜,与之融合(fusion)
- 货物状态:蛋白质在囊泡内部(腔内蛋白)或嵌在囊泡膜中(膜蛋白),不直接穿过膜
- 关键分子:COPI/COPII/Clathrin 被膜蛋白(coat proteins)、SNARE(膜融合机器)、Rab GTPase(靶向调控)
- 特点:膜的拓扑关系始终保持——ER 腔 = 高尔基体腔 = 囊泡内 = 细胞外
1.6 分选信号(Sorting Signal)的深入理解
分选信号的本质是蛋白质中携带的"地址标签",告诉细胞的运输机器该蛋白质的目的地。
信号序列(Signal Sequence)的特征:
- 通常是一段连续的氨基酸序列
- 长度通常为 3-60 个氨基酸
- 不依赖精确的氨基酸序列,而是依赖物理化学性质(如疏水性、正电荷)
- 许多信号序列在蛋白质到达目的地后被蛋白酶切除
信号斑(Signal Patch)的特征:
- 由蛋白质三维折叠后,多个在一级序列中不相邻的氨基酸在空间上聚集形成
- 只有在蛋白质正确折叠后才存在
- 不会被切除(切除会破坏蛋白质结构)
- 例子:甘露糖-6-磷酸标记(用于溶酶体酶的分选)
各细胞器信号序列的特征对比:
| 目的地 | 信号名称 | 位置 | 关键特征 | 是否被切除 |
|---|---|---|---|---|
| ER | 信号肽(Signal peptide) | N 端 | 疏水核心(6-15 个疏水 aa) | 是(信号肽酶切除) |
| 线粒体基质 | 前导序列(Pre-sequence) | N 端 | 两亲性α螺旋(正电荷+疏水交替) | 是(MPP 切除) |
| 过氧化物酶体 | PTS1 | C 端 | -SKL 或类似三肽 | 否 |
| 过氧化物酶体 | PTS2 | N 端 | ~9 aa 共识序列 | 是/否(取决于物种) |
| 细胞核进口 | NLS | 任意位置 | 富含 Lys/Arg | 否 |
| 细胞核出口 | NES | 任意位置 | 富含 Leu | 否 |
| ER 滞留 | KDEL/HDEL | C 端 | 四肽 KDEL(ER 可溶蛋白) | 否 |
---
第二部分:内质网(ER)蛋白质进口
2.1 历史背景(详述)
ER 蛋白质进口的研究是细胞生物学的经典故事,跨越了半个世纪。
Albert Claude(1899-1983) 和 Keith Roberts Porter(1912-1997)
20 世纪 40 年代,Claude 在洛克菲勒大学率先将细胞匀浆和差速离心技术应用于细胞生物学。他将细胞打碎后,通过不同转速的离心,分离出不同大小的细胞组分:低速沉淀(细胞核和碎片)、中速沉淀(线粒体)、高速沉淀(微粒体=ER 碎片)。
Porter 随后利用当时刚发展起来的电子显微镜,首次清晰地拍摄到了细胞内的膜结构网络,并将其命名为"endoplasmic reticulum"(内质网,意为"细胞质内的网状结构")。
George Palade(1912-2008)
Palade 用电子显微镜进一步研究了 ER 的超微结构。他的关键发现:
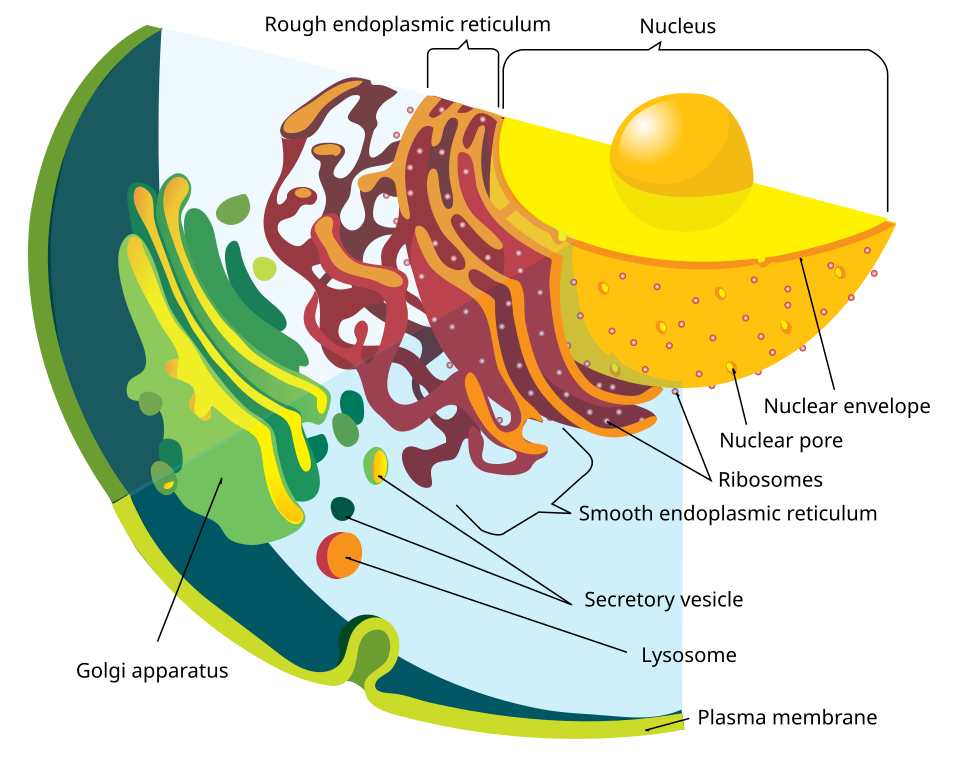
- ER 膜上附着着大量核糖体(ribosomes),呈"小黑点"状——这就是粗面 ER(rough ER)
- 没有核糖体附着的 ER 是滑面 ER(smooth ER)
- 通过放射性同位素追踪实验,他揭示了分泌途径(secretory pathway):蛋白质在粗面 ER 合成 → 运输到高尔基体 → 包装到分泌囊泡 → 释放到细胞外
Claude、Palade 和 Christian de Duve(发现溶酶体和过氧化物酶体)共同获得了 1974 年诺贝尔生理学或医学奖。
> Palade 提出的关键问题:"为什么核糖体附着在 ER 上,而不附着在线粒体上?"这个问题的答案需要等到 Blobel 的工作才被揭示。
Günter Blobel(1936-2018)
Blobel 是信号肽假说(signal hypothesis)的提出者和证明者。他的核心发现:
1. 信号肽假说(1971 年提出):蛋白质的 N 端含有一段特殊的信号序列,决定其是否进入 ER。带有信号肽的蛋白质被特异性地引导到 ER 膜上翻译。 2. 用体外翻译系统证明了信号肽的存在和功能 3. 概括性地提出:所有跨膜运输的蛋白质都携带"拓扑发生信号"(topogenic signals),决定其在膜中的位置和方向
Blobel 因此获得 1999 年诺贝尔生理学或医学奖。
2.2 体外翻译实验的详细解析
这个实验是理解信号肽假说的基础。让我们一步步拆解:
实验材料:
1. mRNA:编码一种分泌蛋白(例如免疫球蛋白轻链)的 mRNA。可以从分泌活跃的细胞中提取,也可以体外转录获得。 2. 翻译系统:兔网织红细胞裂解液(rabbit reticulocyte lysate)。网织红细胞是即将成熟的红细胞,细胞质中充满了核糖体、tRNA、翻译因子和 ATP/GTP 等——是一个完美的无细胞翻译系统。 3. 微粒体(microsomes):通过差速离心从细胞匀浆中分离的 ER 碎片。匀浆时 ER 断裂,但由于膜的自密封性质,断裂的 ER 会自发形成封闭的小囊泡(微粒体)。微粒体保留了 Sec61 转运通道和信号肽酶。
微粒体的分离方法:
- 将细胞匀浆
- 低速离心去除细胞核和碎片
- 高速离心(100,000 × g)沉淀微粒体
- 蔗糖密度梯度离心进一步分离粗面微粒体(密度大,含核糖体)和滑面微粒体(密度小)
实验设计(两组对照):
| 组别 | 条件 | 预期结果 |
|---|---|---|
| 实验组 A | mRNA + 核糖体 无微粒体 | 翻译出含信号肽的前体蛋白(分子量较大) |
| 实验组 B | mRNA + 核糖体 有微粒体 | 翻译出信号肽被切除的成熟蛋白(分子量较小) |
结果分析(SDS-PAGE):
- 无微粒体组:凝胶上出现一条分子量较大的条带——这是前体蛋白(precursor),包含信号肽
- 有微粒体组:凝胶上出现一条分子量较小的条带——这是成熟蛋白(mature protein),信号肽已被切除
- 两者的分子量差异约 1.5-3 kDa,正好对应信号肽的大小
进一步实验——蛋白酶保护实验:
在有微粒体的条件下翻译后,加入蛋白酶(如蛋白酶 K):
- 如果蛋白质已经被转运到微粒体内部,膜会保护它不被降解
- 如果蛋白质还在微粒体外面,会被蛋白酶降解
结果:成熟蛋白被微粒体膜保护(不被降解),证明它确实被转运到了微粒体腔内。
如果先用去污剂(detergent)破坏微粒体膜再加蛋白酶,成熟蛋白也会被降解——进一步证明保护来自于膜。
Blobel 的"读出实验"(Readout experiment):
这是一个更精巧的实验设计: 1. 先在无微粒体条件下开始翻译,使核糖体-mRNA-新生链复合物(RNC)积累 2. 用去污剂从微粒体膜上提取核糖体(这些核糖体正在翻译,被"冻结"在不同的翻译阶段) 3. 将这些 RNC 放入新的翻译系统中继续翻译("读出"剩余序列) 4. 分析产物:有些是前体蛋白(信号肽还在),有些是成熟蛋白(信号肽已被切除)
这个实验证明了信号肽的切除发生在翻译过程中,即共翻译切除。
2.3 N-端信号序列的深入分析
信号肽的三段式结构(详细版):
N ──[ n 区 ]──[ h 区(疏水核心) ]──[ c 区 ]──↓切割位点── 成熟蛋白 ── C
正电荷 6-15个疏水氨基酸 含SPase切割位点
1-5 aa (Leu, Ile, Val, 小侧链aa在-1和-3位
Ala, Phe等) (Ala, Gly, Ser)各区域的功能:
n 区(N-terminal region):
- 长度:1-5 个氨基酸
- 含 1-2 个带正电的氨基酸(Lys 或 Arg)
- 功能:帮助信号肽正确插入 Sec61 通道。正电荷与 Sec61 通道入口处的负电荷相互作用,促进插入。同时,正电荷遵循"正电荷内侧规则",确保 N 端留在细胞质侧。
h 区(Hydrophobic core):
- 长度:6-15 个氨基酸
- 全部或几乎全部为疏水氨基酸
- 这是信号肽最关键的区域——SRP54 的 M 域(methionine-rich domain)识别的就是这段疏水核心
- 功能机制:疏水核心可以形成α螺旋,与 SRP54 的疏水口袋结合。之后,疏水核心通过 Sec61 的侧向门插入脂双层。
c 区(C-terminal region / Cleavage region):
- 长度:3-7 个氨基酸
- 遵循 "-3, -1 规则":切割位点上游第 -1 位和第 -3 位必须是小侧链氨基酸(通常是 Ala、Gly 或 Ser)。这是信号肽酶(SPase)识别切割位点的关键。
- 信号肽酶切除信号肽后,切割位点处成为新的 N 端
为什么信号肽没有共识序列(consensus sequence)?
不同蛋白质的信号肽在氨基酸序列上几乎没有相似性。这是因为信号肽的功能不依赖于特定的氨基酸,而依赖于物理化学性质——特别是足够长的连续疏水区段。这也是为什么可以用人工设计的疏水肽段替代天然信号肽,仍然能功能性地引导蛋白质进入 ER。
2.4 SRP 的结构与功能(详述)
SRP 的组成(真核生物,以哺乳动物为例):
SRP 是一个核糖核蛋白复合物(ribonucleoprotein),由 6 个蛋白质亚基和 1 个 RNA 分子组成:
| 组分 | 功能 |
|---|---|
| 7SL RNA(~300 nt) | SRP 的骨架,连接各蛋白亚基 |
| SRP9/SRP14 异二聚体 | 结合核糖体,造成翻译暂停(elongation arrest) |
| SRP19 | 帮助 SRP54 结合到 7SL RNA 上 |
| SRP54 | 核心亚基:N 端 GTPase 域 + C 端 M 域(识别信号肽) |
| SRP68/SRP72 异二聚体 | 连接 SRP 的两个功能域;SRP68 与核糖体和 7SL RNA 都有相互作用 |
SRP 的形状像一个细长的"热狗",中间有铰链(hinge),可以弯折。信号肽结合口袋在一端(SRP54),翻译暂停域在另一端(SRP9/14)。
SRP 识别信号肽的分子机制:
SRP54 的 M 域(methionine-rich domain)形成一个疏水口袋。甲硫氨酸的侧链(-CH₂-CH₂-S-CH₃)灵活且疏水,可以适应不同序列的信号肽——就像一只"灵活的手套",可以包裹住各种形状的疏水肽段。这解释了为什么 SRP 能够识别序列差异很大的信号肽。
翻译暂停(Elongation arrest)的意义:
当 SRP 结合信号肽后,SRP9/14 与核糖体的因子结合位点相互作用,减慢或暂停翻译延伸。这一步骤至关重要,因为:
1. 防止过早折叠:如果翻译继续而蛋白质还在细胞质中,新生多肽可能开始折叠或与其他蛋白质相互作用,形成无法通过 Sec61 窄通道的结构。 2. 提供时间窗口:给 SRP-RNC 复合物足够的时间找到 ER 膜上的 SRP 受体。 3. 防止聚集:疏水信号肽如果暴露在细胞质的水性环境中太久,可能导致蛋白质聚集。
> 原核生物的类似物:细菌也有 SRP 系统,但更简单——只有一个蛋白质 Ffh(SRP54 的同源物)和一个 4.5S RNA。细菌 SRP 不引起翻译暂停(细菌细胞很小,核糖体到质膜距离短)。
2.5 SRP-SR 相互作用与 GTP 调控(详述)
SRP 受体(SR)的结构:
SRP 受体是一个异二聚体,位于 ER 膜上:
- SRα:外周膜蛋白,含 GTPase 域,与 SRP54 的 GTPase 域相互作用
- SRβ:跨膜蛋白,含另一个 GTPase 域,将 SR 锚定在 ER 膜上
GTPase 双开关机制:
SRP54 和 SRα 各自含有一个 GTPase 域。它们的工作方式与经典的 Ras 家族 GTPase 不同——SRP 和 SR 相互作为对方的 GAP:
1. 在细胞质中:SRP54 结合 GTP,SRα 也结合 GTP 2. SRP 与 SR 对接:两个 GTPase 域直接接触,形成一个共享的活性位点 3. 信号肽转移:SRP 释放信号肽,信号肽被转交给 Sec61 通道 4. GTP 水解:两个 GTPase 相互刺激对方水解 GTP → GDP + Pi 5. 解离:GTP 水解后,SRP 与 SR 解离。SRP 回到细胞质,SR 留在 ER 膜上
这个双 GTPase 机制确保了高保真度——只有当 SRP 正确携带了含信号肽的核糖体,并与 SR 正确对接时,GTP 才会被水解。这避免了空载的 SRP 或不含信号肽的核糖体被错误地靶向到 ER。
2.6 Sec61 转运通道的结构与功能(详述)
Sec61 的三维结构(来自 X 射线晶体学和冷冻电镜):
Sec61α 是核心亚基,有 10 个跨膜α螺旋(TM1-TM10)。这 10 个螺旋分为两半(TM1-5 和 TM6-10),像两扇"蛤壳"一样围成一个通道。
关键结构元件:
堵头(Plug):
- 位于通道腔侧(ER 腔侧)
- 是一个短的α螺旋(α2a,约 10 个氨基酸)
- 在静息状态下,堵头堵住通道出口
- 功能:防止小分子和离子泄漏。ER 腔中 Ca²⁺ 浓度比细胞质高约 5000 倍,如果通道不关闭,Ca²⁺ 会大量外流,破坏细胞信号
- 当信号肽插入通道后,堵头被推开(displaced),通道打开
侧向门(Lateral gate / Seam):
- TM2b 和 TM7 之间有一条"缝"
- 在信号肽插入后,侧向门打开,让疏水的信号肽和跨膜区域从通道"溜"到脂双层中
- 对于分泌蛋白:信号肽通过侧向门离开通道后被信号肽酶切除
- 对于膜蛋白:跨膜区域通过侧向门永久嵌入脂双层
环缢(Pore ring):
- 通道最窄处有 6 个疏水氨基酸(多为异亮氨酸)的侧链朝向通道中心
- 形成一个疏水密封,在通道开启时包裹住穿过的多肽链
- 防止小分子从通道壁渗漏
Sec61 如何工作——一个统一模型:
1. 静息态:堵头关闭通道,侧向门关闭,通道密封 2. 核糖体对接:翻译中的核糖体对接到 Sec61 的细胞质面。核糖体的出口隧道正好对准 Sec61 通道的入口。 3. 信号肽插入:信号肽作为α螺旋插入通道,与通道壁的疏水残基相互作用 4. 堵头打开:信号肽推开堵头,通道腔侧开放 5. 侧向门打开:信号肽通过侧向门进入脂双层 6. 肽链穿过:后续的多肽链通过通道进入 ER 腔 7. 信号肽切除:信号肽酶切除信号肽 8. 通道关闭:翻译完成后,核糖体脱离,堵头回位,通道重新密封
2.7 共翻译转运 vs 翻译后转运(详述)
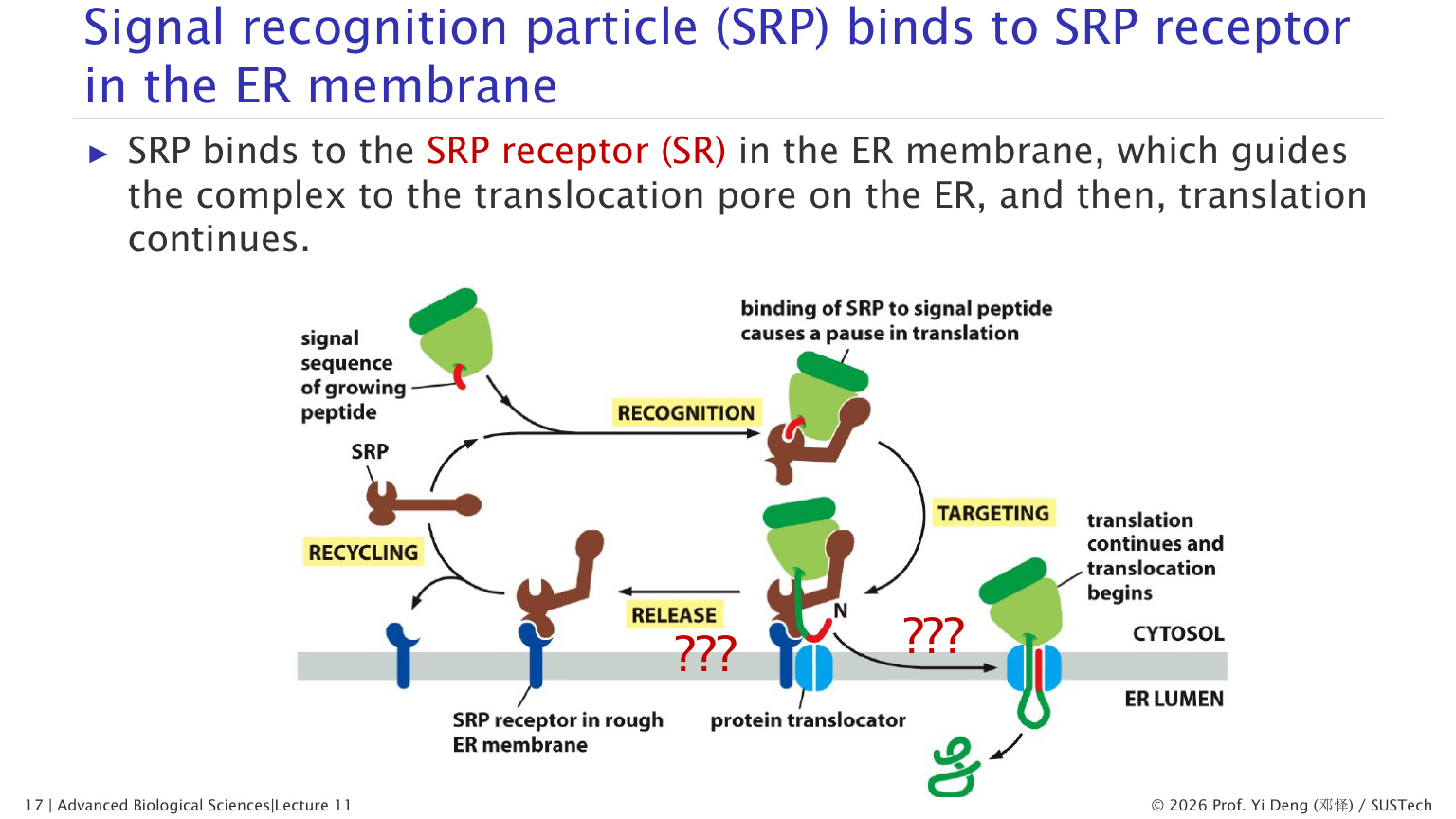
共翻译转运(Co-translational translocation)——主要方式:
在哺乳动物细胞中,大多数进入 ER 的蛋白质使用共翻译转运。整个过程可以总结为 8 个步骤:
1. mRNA 在细胞质中开始翻译 2. 信号肽从核糖体出口隧道中冒出(约翻译 70 个氨基酸后,信号肽刚好露出) 3. SRP 识别并结合信号肽 4. SRP 与核糖体结合,暂停翻译 5. SRP-RNC 复合物靶向 ER 膜上的 SRP 受体 6. GTP 水解驱动 SRP 释放信号肽,核糖体转移到 Sec61 上 7. 翻译恢复,新生肽链边翻译边穿过 Sec61 进入 ER 腔 8. 信号肽酶切除信号肽,蛋白质在 ER 腔中折叠,核糖体脱离
优势:蛋白质边合成边转运,不需要在细胞质中维持未折叠状态。
翻译后转运(Post-translational translocation)——酵母中更常见:
某些小的分泌蛋白(特别是在酵母中),由于翻译速度快,SRP 来不及识别就翻译完成了。这些蛋白通过翻译后转运进入 ER。
关键差异:
- 不需要 SRP 和 SRP 受体
- 蛋白质在细胞质中完全翻译完成
- 需要细胞质 Hsp70 分子伴侣维持蛋白质的未折叠状态
- 需要 Sec62-Sec63 复合物帮助蛋白质对接到 Sec61 上
- BiP(ER 腔内的 Hsp70 分子伴侣)通过"棘轮机制"拉动蛋白质进入 ER 腔
BiP 的棘轮机制(Brownian ratchet): 1. 多肽链通过热运动(布朗运动)在 Sec61 通道中双向随机移动 2. 当一段多肽露出通道的腔侧时,BiP-ATP 结合该段多肽 3. BiP 水解 ATP 变为 BiP-ADP,紧紧抱住多肽 4. 多肽不能再往回退(被 BiP "锁住") 5. 下一段多肽继续随机运动露出...重复以上过程 6. 最终,蛋白质被逐步"拉"入 ER 腔
这类似于一个棘轮:允许单方向运动,阻止反方向运动。每次 BiP 结合都消耗一个 ATP,因此翻译后转运是一个耗能过程。
2.8 膜蛋白拓扑结构的建立(全面详解)
膜蛋白的拓扑结构(topology)指的是蛋白质的哪些部分在细胞质侧、哪些在 ER 腔侧、以及有多少个跨膜区域。拓扑结构在蛋白质合成时就确定了,后续不再改变。
理解拓扑学的一个核心关系:
- ER 腔 = 高尔基体腔 = 囊泡内部 = 细胞外
- 细胞质 = 细胞质
这是因为囊泡运输保持了膜的方向性。所以:
- Type I 膜蛋白的 N 端在 ER 腔 = 成熟后 N 端在细胞外
- 膜蛋白的细胞质面结构域参与细胞内信号传导
Type I 膜蛋白的合成过程(以 LDL 受体为例):
1. N 端信号肽出现 → SRP 识别 → 靶向 ER 膜 → 信号肽作为起始转移序列(start-transfer sequence)插入 Sec61 2. 翻译继续,蛋白质穿过通道进入 ER 腔 3. 信号肽通过侧向门进入脂双层,被信号肽酶切除 4. 翻译继续,直到遇到一段疏水的停止转移序列(stop-transfer sequence) 5. 停止转移序列是一个约 20-25 个氨基酸的疏水区段,它停留在 Sec61 通道中,不再继续穿过 6. 停止转移序列通过侧向门横向移动到脂双层中,成为跨膜锚定区(transmembrane anchor) 7. 之后翻译的部分留在细胞质侧 8. 最终拓扑:N 端(在 ER 腔/细胞外)—— 跨膜区 —— C 端(在细胞质)
Type II 膜蛋白的合成过程(以转铁蛋白受体为例):
1. 蛋白质没有 N 端可切割信号肽 2. 翻译开始后,一段内部的疏水序列从核糖体出口隧道冒出 3. 这段序列称为信号锚定序列(signal-anchor sequence),兼具信号肽和跨膜锚的功能 4. SRP 识别这段疏水序列,靶向 ER 膜 5. 关键:信号锚定序列的方向取决于其两侧的电荷分布 6. 对于 Type II:正电荷在信号锚序列的 N 端侧 → N 端留在细胞质侧(正电荷内侧规则) 7. 信号锚序列两端的"+" 侧留细胞质,"-" 侧穿过去 8. C 端部分穿过通道进入 ER 腔 9. 最终拓扑:N 端(细胞质)—— 跨膜区 —— C 端(ER 腔/细胞外)
Type III 膜蛋白(以细胞色素 P450 为例):
- 与 Type II 的区别仅在于信号锚序列两侧的电荷分布相反
- 正电荷在信号锚序列的 C 端侧 → C 端留在细胞质侧
- 最终拓扑:N 端(ER 腔)—— 跨膜区 —— C 端(细胞质)
> 正电荷内侧规则(Positive-inside rule) 是膜蛋白拓扑学的核心原则。信号锚定序列两侧,含更多正电荷(Arg, Lys)的一端留在细胞质侧。改变电荷分布可以翻转膜蛋白的方向。这条规则也适用于细菌膜蛋白。
Type IV 多次跨膜蛋白的合成(以 GPCR 为例):
多次跨膜蛋白有多个跨膜区域,它们交替作为起始转移信号和停止转移信号:
以一个 7 次跨膜的 GPCR 为例(Type IV-A,N 端在细胞质):
1. 第一个疏水区段作为信号锚定序列(SA),插入 Sec61,N 端留在细胞质(正电荷内侧规则) 2. 翻译继续,多肽进入 ER 腔 3. 第二个疏水区段作为停止转移锚定序列(STA),停留在通道中,C 端侧回到细胞质 4. 第三个疏水区段又作为 SA,开始新一轮转运 5. 如此交替,直到所有跨膜区域都插入膜中
Type IV-B(N 端在 ER 腔)则是第一个 SA 的方向相反,使 N 端进入 ER 腔。
Sec61 通道的侧向门在这个过程中不断开合,每个跨膜区域都通过侧向门释放到脂双层中。
尾锚定蛋白(Tail-anchored proteins)的特殊进口机制:
TA 蛋白的跨膜区位于 C 端最后 ~20 个氨基酸。当翻译完成时,这段跨膜区还埋在核糖体内部,SRP 无法在翻译过程中识别到它。因此 TA 蛋白使用一条完全不同的途径——GET 途径:
GET 途径的步骤: 1. 捕获:TA 蛋白从核糖体释放后,其疏水 C 端暴露。预靶向复合物(由 Sgt2 + Get4 + Get5 组成)识别并保护疏水的跨膜区。 2. 转交:Sgt2 将 TA 蛋白转交给 Get3(一种 ATPase)。Get3 结合 ATP 后呈"关闭"构象,形成一个疏水凹槽,紧紧包裹 TA 蛋白的跨膜区。 3. 靶向:Get3-TA 蛋白复合物靶向 ER 膜上的受体 Get1-Get2。 4. 插入:Get3 水解 ATP,构象改变为"打开"态,释放 TA 蛋白,跨膜区插入 ER 膜。 5. 循环:Get3 回到细胞质,准备下一轮循环。
TA 蛋白的例子:
- SNARE 蛋白(如 VAMP/synaptobrevin、syntaxin):囊泡融合的核心机器
- Bcl-2 家族蛋白:凋亡调控
- Sec61β:Sec61 转运通道的 β 亚基本身就是 TA 蛋白
GPI 锚定蛋白的生成(详述):
GPI 锚定蛋白经历了一个独特的两步过程:
1. 第一步——作为跨膜蛋白合成:蛋白质含有 N 端信号肽和 C 端跨膜区/GPI 信号序列。它先作为 Type I 样膜蛋白插入 ER 膜。 2. 第二步——跨膜区替换为 GPI 锚:
- ER 腔内有一个预先合成好的 GPI 锚前体(glycosylphosphatidylinositol anchor),插在 ER 膜内叶
- GPI 转氨酶(GPI transamidase) 切除蛋白质的 C 端跨膜区/GPI 信号序列
- 同时将蛋白质的新 C 端与 GPI 锚通过酰胺键连接
GPI 锚的完整结构(从蛋白质到膜):
蛋白质-C端 —— 磷酸乙醇胺(phosphoethanolamine)
|
甘露糖 — 甘露糖 — 甘露糖(3 mannose)
|
葡糖胺(glucosamine)
|
肌醇(inositol)
|
磷脂(嵌入膜外叶)GPI 锚定蛋白的特点:
- 只在细胞表面的外叶
- 可以被 PI-PLC(磷脂酶 C) 切割释放
- 常存在于脂筏(lipid raft) 微域中
- 功能多样:酶、受体、粘附分子等
---
第三部分:线粒体蛋白质进口
3.1 线粒体的结构详述
线粒体是"细胞的发电站",有独特的双膜结构:
外膜(Outer Mitochondrial Membrane, OMM):
- 含大量porin/VDAC(电压依赖性阴离子通道),使小分子(< ~5 kDa)可以自由通过
- 因此,膜间隙的小分子组成与细胞质相似
- 外膜相对简单,蛋白质含量较低
膜间隙(Intermembrane Space, IMS):
- 小分子组成类似细胞质
- 含有多种功能蛋白:
- 细胞色素 c:电子传递链组分,凋亡时释放到细胞质触发 caspase 级联
- Mia40/Erv1:氧化折叠系统
- 各种激酶
内膜(Inner Mitochondrial Membrane, IMM):
- 高度不透性:即使是 H⁺ 也不能自由通过(除了通过特异性载体/通道)
- 向内折叠形成嵴(cristae),极大地增加表面积
- 含有:
- 电子传递链复合物(Complex I-IV)
- ATP 合酶(Complex V)
- 各种代谢物载体蛋白(ADP/ATP 载体、磷酸载体等)
- 蛋白质导入通道(TIM23、TIM22、OXA)
- 磷脂组成特殊:含大量心磷脂(cardiolipin)(类似细菌膜,支持内共生起源)
- 蛋白质:脂质比例高达 3:1(细胞质膜约 1:1)
基质(Matrix):
- 含:三羧酸循环酶、脂肪酸β-氧化酶、氨基酸代谢酶
- 线粒体 DNA(~16.5 kb 环形分子,编码 13 个蛋白质、22 个 tRNA、2 个 rRNA)
- 线粒体核糖体(mitoribosomes):70S 类型(细菌样)
- 分子伴侣:mtHsp70、Hsp60/Hsp10
- 蛋白酶:MPP(加工前导序列)
3.2 线粒体前导序列(Pre-sequence)的详细特征
线粒体基质蛋白的 N 端前导序列与 ER 信号肽有本质区别:
| 特征 | ER 信号肽 | 线粒体前导序列 |
|---|---|---|
| 长度 | 16-30 aa | 10-70 aa(通常 20-40 aa) |
| 关键结构 | 连续疏水区(α螺旋) | 两亲性α螺旋(amphipathic helix) |
| 电荷 | N 端少量正电荷 | 丰富的正电荷(Arg > Lys) |
| 疏水性 | 高度疏水核心 | 一面疏水、一面亲水(带正电) |
| 切除 | 信号肽酶切除 | MPP(线粒体加工肽酶)切除 |
| 二级结构 | 疏水α螺旋 | 两亲性α螺旋 |
两亲性α螺旋的示意:
如果将前导序列画成α螺旋,从端面看(helical wheel projection),你会看到:
- 一面全是疏水氨基酸(Leu, Ile, Val, Phe)
- 另一面全是带正电荷的氨基酸(Arg, Lys)和极性氨基酸
这种两亲性结构是被 TOM 受体(Tom20)识别的关键。Tom20 有一个疏水凹槽,可以结合前导序列的疏水面,而正电荷面暴露在外。
为什么线粒体前导序列富含精氨酸(Arg)而不是赖氨酸(Lys)?
这可能与识别特异性有关。Arg 的胍基有独特的氢键模式,可能有助于与 Tom20 受体的特异性识别,以及与内膜膜电位的相互作用。
3.3 线粒体蛋白转运机器(全面详解)
TOM 复合物(Translocase of the Outer Membrane)
TOM 是所有核编码线粒体蛋白进入线粒体的第一道关卡。
组成:
- Tom20:初级受体,识别前导序列的疏水面。Tom20 是一种外周膜蛋白,N 端锚定在外膜,C 端的 TPR(tetratricopeptide repeat)结构域伸向细胞质,暴露一个疏水凹槽。
- Tom22:二级受体(cis 受体),将前导序列从 Tom20 传递到 Tom40 通道。Tom22 在膜间隙侧也有结构域(trans 受体),帮助蛋白质穿过通道后的释放。
- Tom70:识别含内部靶向信号的前体蛋白(如载体蛋白类),通常与 Hsp70/Hsp90 协作。
- Tom40:核心通道亚基,形成β-barrel 结构(由β折叠片围成的桶状通道),约 22 Å 内径。每个 TOM 复合物含 2 个 Tom40 拷贝(即双通道)。
- Tom5, Tom6, Tom7:小 Tom 蛋白,调节通道的组装和稳定性。
SAM 复合物(Sorting and Assembly Machinery)
- 也称为 TOB(Topogenesis of Outer membrane β-barrel proteins)
- 功能:将β-barrel 蛋白正确折叠并插入外膜
- 核心亚基:Sam50(本身是β-barrel 蛋白)
- 工作路径:前体蛋白穿过 TOM → 在膜间隙由小 Tim 伴侣护送 → SAM 将其从膜间隙侧插入外膜
- 例子:VDAC/Porin、Tom40 本身
TIM23 复合物
TIM23 负责转运含有 N 端前导序列的蛋白质。
组成:
- Tim23:核心通道亚基,与 Tim17 形成通道
- Tim17:与 Tim23 共同形成转运通道
- Tim50:识别从 TOM 穿过来的前导序列(膜间隙侧受体)
- Tim21:连接 TIM23 与呼吸链复合物 III/IV
- PAM(Presequence translocase-Associated Motor)复合物:
- Tim44:将 mtHsp70 锚定到 TIM23 的基质侧出口
- mtHsp70(Ssc1 in yeast):ATP 驱动的分子伴侣,拉动多肽进入基质
- Mge1:mtHsp70 的核苷酸交换因子(NEF),促进 ADP → ATP 交换
- Tim14/Pam18:mtHsp70 的 J 蛋白(co-chaperone),刺激 ATP 水解
- Tim16/Pam16:调节 Tim14
TIM22 复合物
TIM22 负责将多次跨膜的载体蛋白插入内膜。
靶向的蛋白质:
- ADP/ATP 载体(AAC/ANT)
- 磷酸载体
- 二羧酸载体
- Tim22 和 Tim23 本身
这些蛋白的特征是含有内部靶向信号(不是 N 端前导序列),由 4-6 个跨膜结构域组成。
进口路径: 1. 前体蛋白被细胞质 Hsp70/Hsp90 维持在可溶状态 2. Tom70 识别这些复合物 3. 穿过 TOM 通道 4. 在膜间隙,小 Tim 蛋白(Tim9-Tim10-Tim12 复合物)接力护送 5. 蛋白质被传递到 TIM22 6. 膜电位(Δψ)驱动跨膜区段插入内膜 7. 不需要 ATP 水解(与 TIM23 不同)
OXA 复合物(Oxidase Assembly machinery)
- OXA1(酵母中称为 Oxa1p)是核心亚基
- 属于 YidC/Oxa1/Alb3 蛋白家族(存在于所有生命域)
- 功能:从基质侧将蛋白质插入内膜
- 主要用于:
- 线粒体自身基因组编码的蛋白质(在基质中翻译后插入内膜)
- 某些核编码蛋白:先进入基质,再通过 OXA 插入内膜("保守插入途径")
- 例子:细胞色素氧化酶(Complex IV)的某些亚基
3.4 基质蛋白进口的驱动力(详述)
进口线粒体基质蛋白需要两种能量:
(1)内膜膜电位(Δψ,约 -180 mV,基质侧为负)
线粒体内膜维持着显著的质子电化学梯度(由呼吸链产生的质子泵维持):
- 基质侧:H⁺ 浓度低(pH ~8)、负电位
- 膜间隙侧:H⁺ 浓度高(pH ~7)、正电位
前导序列富含正电荷(Arg, Lys),会被负电位电泳(electrophoresis)拉入基质。这类似于电场驱动带电粒子运动。
实验证据:
- 用解偶联剂(如 CCCP、valinomycin)消除膜电位 → 蛋白质进口立即停止
- 恢复膜电位 → 进口恢复
膜电位主要驱动前导序列穿过内膜,是进口的早期步骤。
(2)ATP 水解(mtHsp70 驱动的棘轮机制)
基质中的 mtHsp70 消耗 ATP 拉动蛋白质的后续部分进入基质。
详细机制: 1. 前导序列穿过 TIM23 后,被基质中的 Tim44 捕获 2. Tim44 将 mtHsp70-ATP 招募到通道出口 3. mtHsp70 结合露出基质的多肽段 4. Tim14(J 蛋白)刺激 mtHsp70 的 ATP 水解活性 5. mtHsp70-ADP 紧紧"夹住"多肽(类似"老虎钳"),蛋白质不能回退 6. Mge1(NEF)促进 ADP → ATP 交换,mtHsp70 释放多肽 7. 下一个 mtHsp70 分子结合更前方的多肽段 8. 重复步骤 3-7,蛋白质被逐步拉入基质
最终,进入基质的蛋白质:
- 前导序列被 MPP(Mitochondrial Processing Peptidase) 切除
- 在 Hsp60/Hsp10 chaperonin 系统帮助下正确折叠
3.5 线粒体内膜和膜间隙蛋白的进口(五种途径详解)
途径 1:TOM → TIM23 侧向释放到内膜
适用于:含 N 端前导序列 + 一个疏水停止转移序列的内膜蛋白
过程: 1. 前导序列被膜电位驱动穿过 TOM 和 TIM23 2. 前导序列在基质被 MPP 切除 3. 后续的疏水停止转移序列到达 TIM23 通道时,不再继续穿过 4. TIM23 的侧向门打开,将疏水区域释放到内膜脂双层中 5. 蛋白质锚定在内膜上:N 端域在基质,C 端域在膜间隙
TIM23 复合物存在两种形态:
- TIM23-PAM(含 mtHsp70 马达):用于完全转运到基质
- TIM23-SORT(与 Tim21 和呼吸链结合):用于侧向释放到内膜
途径 2:TOM → TIM23 → 基质 → OXA 插入内膜(保守插入途径)
适用于:某些内膜蛋白,含前导序列 + 第二信号序列
过程: 1. 蛋白质完全进入基质(通过 TOM + TIM23) 2. 前导序列被 MPP 切除 3. 第二信号序列(内部疏水区段)被 OXA 复合物识别 4. OXA 将蛋白质从基质侧"推"入内膜
为什么叫"保守"插入途径?因为这与细菌中 YidC 将新合成蛋白插入质膜的途径同源——反映了线粒体的细菌起源。
途径 3:经过两次蛋白酶切割进入膜间隙
适用于:某些膜间隙蛋白
过程: 1. 蛋白质含有前导序列 + 紧随其后的疏水序列 2. 前导序列穿过 TOM 和 TIM23 进入基质 3. 疏水序列作为停止转移信号,锚定在内膜中 4. 第一次切割:基质中的 MPP 切除前导序列 5. 第二次切割:膜间隙侧的蛋白酶切除锚定区 6. 切割后的蛋白质被释放到膜间隙中
途径 4:TOM → Mia40 氧化折叠捕获(MIA 途径)
适用于:小的膜间隙蛋白,含 CX₃C 或 CX₉C 基序
这些蛋白通常是 ~10 kDa 的小蛋白,以还原(未折叠)状态穿过 TOM 通道。它们没有 N 端前导序列。
过程: 1. 还原态蛋白(-SH 自由基)穿过 TOM 通道进入膜间隙 2. 膜间隙中的氧化还原酶 Mia40(Mitochondrial Intermembrane space Import and Assembly protein)识别蛋白质 3. Mia40 将自己的二硫键(-S-S-)转移给底物蛋白,使底物形成分子内二硫键 4. 折叠后的蛋白质太大,无法再穿回 TOM 通道 → 被"锁"在膜间隙中 5. Mia40 变为还原态后,被 Erv1(一种巯基氧化酶)再氧化 6. Erv1 将电子最终传递给呼吸链(通过细胞色素 c → 复合物 IV → O₂)
这个机制非常精巧——利用蛋白质折叠本身作为"单向阀",确保蛋白质只能进不能出。
途径 5:TOM → 小 Tim → TIM22 多次跨膜蛋白插入内膜
适用于:代谢物载体蛋白家族(MCF,Mitochondrial Carrier Family)
过程: 1. 前体蛋白在细胞质中被 Hsp70/Hsp90 维持可溶 2. Tom70 受体识别 Hsp-前体复合物 3. 前体穿过 TOM 通道 4. 在膜间隙中,小 Tim 伴侣(Tim9-Tim10 六聚体环)包裹住前体的疏水跨膜区段 5. 小 Tim 将前体传递到 TIM22 复合物 6. 膜电位(Δψ)驱动跨膜区段插入内膜(不需要 ATP) 7. 蛋白质在内膜中获得最终的折叠构象
---
第四部分:过氧化物酶体蛋白质进口
4.1 过氧化物酶体的形态和功能(扩展版)
形态:
- 单层膜包被的球形细胞器
- 直径 0.1-1 μm
- 每个细胞含数百到上千个(肝细胞和肾细胞中特别丰富)
- 在电子显微镜下,某些物种的过氧化物酶体含有结晶核心(paracrystalline core),由大量堆积的酶(如尿酸氧化酶 urate oxidase)构成
核心代谢功能:
(1)H₂O₂ 代谢
过氧化物酶体因其利用 H₂O₂ 的反应而得名:
- 氧化酶(如氨基酸氧化酶、D-氨基酸氧化酶、脂酰-CoA 氧化酶)消耗 O₂,产生 H₂O₂:
- RH₂ + O₂ → R + H₂O₂
- 过氧化物酶反应(peroxidation):利用 H₂O₂ 氧化有害底物:
- H₂O₂ + R'H₂ → R' + 2H₂O
- 底物包括苯酚、甲醛、甲酸、乙醇(肝脏中!喝酒后,肝脏过氧化物酶体利用此反应氧化部分乙醇)
- 过氧化氢酶(catalase) 分解过量 H₂O₂:
- 2H₂O₂ → O₂ + 2H₂O
- Catalase 是过氧化物酶体含量最丰富的酶之一
> 有趣的是,catalase 可以在分解 H₂O₂(catalatic activity)和利用 H₂O₂ 氧化底物(peroxidatic activity)之间切换,取决于 H₂O₂ 浓度。
(2)脂肪酸β-氧化
过氧化物酶体和线粒体都能进行脂肪酸β-氧化,但分工不同:
- 过氧化物酶体:氧化超长链脂肪酸(>C22)和支链脂肪酸。过氧化物酶体中的第一步氧化反应由酰基-CoA 氧化酶催化,电子直接传给 O₂ 产生 H₂O₂(不产生 ATP)。
- 线粒体:氧化短链和中链脂肪酸,产生 FADH₂ 和 NADH → ATP。
过氧化物酶体将超长链脂肪酸缩短后(至 C8 左右),产物转运到线粒体继续完全氧化。
(3)缩醛磷脂(plasmalogen)合成
过氧化物酶体催化缩醛磷脂合成的前两步反应。缩醛磷脂是一类特殊的磷脂,在 sn-1 位通过乙烯基醚键(vinyl ether bond,而非酯键)与脂肪酸链连接。
缩醛磷脂占大脑磷脂的约 20%,是髓鞘(myelin sheath)的重要组分。髓鞘是包裹神经轴突的绝缘层,对于神经信号的快速传导至关重要。
> 临床意义:Zellweger 综合征患者由于 PEX 基因突变导致过氧化物酶体无法正确组装,缺乏缩醛磷脂合成和超长链脂肪酸氧化能力,表现为严重的神经发育障碍、肝脏和肾脏功能异常,通常在出生后数月内死亡。
(4)其他功能
- 胆汁酸合成(侧链氧化)
- 乙醛酸循环(植物过氧化物酶体,又称乙醛酸体 glyoxysome)
- 嘌呤分解(某些物种)
- 光呼吸(植物)
4.2 过氧化物酶体蛋白进口的特殊机制(详述)
过氧化物酶体的蛋白质进口系统与 ER 和线粒体有根本不同:
独特特征: 1. 蛋白质以折叠态进口:与 ER(需解折叠或边翻译边转运)和线粒体(需解折叠穿过窄通道)不同 2. 甚至可以进口寡聚体:已组装的多亚基复合物可以整体被进口 3. 进口通道是瞬时组装的:不像 Sec61 或 TOM/TIM 那样永久存在于膜上
两种过氧化物酶体靶向信号:
PTS1(Peroxisomal Targeting Signal 1):
- 位于蛋白质的 C 端最后 3 个氨基酸
- 经典三肽:-SKL(Ser-Lys-Leu)
- 变体也可以:-SRL、-AKL、-SQL 等(共识是小/正电荷/疏水)
- 大约 95% 的过氧化物酶体基质蛋白使用 PTS1
- 被胞质受体 Pex5 识别
PTS2:
- 位于蛋白质 N 端附近
- 共识序列:-R/K-L/V/I-X₅-H/Q-L/A-(约 9 个氨基酸)
- 只有少数蛋白使用
- 被胞质受体 Pex7 识别
- 在某些物种(哺乳动物)中,PTS2 在进口后被切除
Pex5 的"穿梭受体"机制(Cycling receptor model):
1. 识别:胞质中的 Pex5 识别并结合含 PTS1 的货物蛋白 2. 对接:Pex5-货物复合物与过氧化物酶体膜上的对接复合物(Pex14 + Pex13)结合 3. 转位:Pex5 连同货物一起部分或完全插入膜中(甚至可能进入过氧化物酶体腔内)。这是一个争议话题——Pex5 本身可能作为临时转运通道的一部分。 4. 释放:货物在过氧化物酶体腔内释放 5. 回收:Pex5 被单泛素化(与 Pex4 泛素连接酶相关)后,被 Pex1-Pex6 AAA-ATPase从膜中拉出,回到胞质中去泛素化后重新使用
> 如果 Pex5 的回收失败(如 Pex1 或 Pex6 突变),Pex5 被多泛素化并送去蛋白酶体降解。这会导致过氧化物酶体进口功能丧失——这正是某些 Zellweger 综合征变体的分子基础。
4.3 过氧化物酶体的起源(详述)
过氧化物酶体的起源有两条途径,目前认为两者共存:
途径 1:从 ER 从头生成(de novo biogenesis)
1. 过氧化物酶体膜蛋白(如 Pex3、Pex16)首先在 ER 中合成 2. 它们从 ER 芽出到前过氧化物酶体囊泡(pre-peroxisomal vesicles) 3. Pex19(胞质伴侣/受体)识别并护送其他膜蛋白到这些前体囊泡 4. 多个前体囊泡融合形成新的过氧化物酶体 5. 新的过氧化物酶体通过从胞质进口基质蛋白来成熟
途径 2:生长和分裂
1. 已存在的过氧化物酶体持续从胞质进口蛋白质和脂质 2. 过氧化物酶体体积增大 3. 通过 Pex11(膜变形蛋白)和 DRP(dynamin-related protein,如 Dnm1/Drp1) 介导的分裂(fission),产生子代过氧化物酶体
正常情况下,途径 2 是维持过氧化物酶体数量的主要方式。途径 1 可能在过氧化物酶体完全缺失时(如 Zellweger 综合征的某些基因型被遗传互补后)启动从头合成。
---
第五部分:核蛋白的进口与出口
5.1 核质运输概述
细胞核是真核细胞中唯一使用门控运输的细胞器。核膜将遗传物质与细胞质分隔,但基因表达需要持续的核-质交流:
进口核内的分子及其功能意义:
- 组蛋白(H2A, H2B, H3, H4, H1):DNA 复制时大量需要,用于新染色质组装。组蛋白是碱性蛋白(富含 Lys 和 Arg),本身就含有类 NLS 序列。
- DNA 聚合酶、DNA 连接酶、拓扑异构酶:DNA 复制和修复
- RNA 聚合酶 I/II/III:转录
- 转录因子:基因调控。许多转录因子的核进口是基因激活的关键调控步骤。
- RNA 剪接因子(snRNPs 等):mRNA 前体加工
- 核糖体蛋白:在核仁中与 rRNA 组装成核糖体亚基前体
从核内出口的分子:
- mRNA(以 mRNP 形式):成熟 mRNA 与多种蛋白质结合后出核
- tRNA:在核内加工成熟后出口
- 核糖体亚基前体(40S 和 60S pre-subunits):在核仁组装后出核,在细胞质中完成最终成熟
- 某些蛋白质:如用过的 snRNP 蛋白需要回到细胞质
运输的规模和速度:
一个典型的增殖中的哺乳动物细胞,每分钟需要:
- 进口约 100 万个组蛋白分子
- 出口约 3 条新合成的核糖体亚基前体每秒
- 出口数千条 mRNA 分子
NPC 的运输速率可达 ~1000 个大分子/秒/NPC,考虑到每个细胞有 3000-4000 个 NPC,总通量极其可观。
5.2 核孔复合体(NPC)详解
NPC 是已知最大的蛋白质复合物之一:
| 特征 | 数值 |
|---|---|
| 总分子量 | ~125 MDa(脊椎动物)/ ~50 MDa(酵母) |
| 直径 | ~120 nm(外径) |
| 中心通道直径 | ~40 nm |
| 高度(跨核膜厚度) | ~200 nm(含胞质纤维和核篮) |
| 核孔蛋白种类 | ~30 种 |
| 总蛋白质拷贝数 | ~500-1000 个(每种 8-48 拷贝,八重对称) |
| 每个细胞 NPC 数量 | ~3000-4000 |
NPC 的分层结构:
从细胞质到核内,NPC 可以分为以下几层:
(1)胞质纤维(Cytoplasmic filaments)
- 约 8 条纤维从 NPC 的细胞质面向外伸出,长约 50 nm
- 由 Nup358/RanBP2 构成
- 功能:初步捕获从细胞质靠近的 Importin-货物复合物
- Nup358 含有 FG 重复序列和 Ran 结合位点
(2)细胞质环(Cytoplasmic ring)
- 由 Y-复合物(Nup107-160 复合物)组成的外环
- 八重旋转对称
(3)中心通道(Central channel)
- 由 FG-核孔蛋白(FG-Nups) 的无序 FG 重复结构域填充
- FG 重复序列呈本征无序蛋白(intrinsically disordered protein)状态
- 形成选择性通透屏障
(4)核质环(Nuclear ring)
- 另一组 Y-复合物
(5)核篮(Nuclear basket)
- 8 条纤维从核面伸出,在末端汇合形成篮状结构
- 由 Nup153(含大量 FG 重复)和 TPR 蛋白组成
- 功能:mRNA 出口质量控制的检查站
FG 重复序列——选择性屏障的核心:
FG-Nups 含有数十到数百个苯丙氨酸-甘氨酸(FG)重复序列,以不同间距排列(如 FG、FXFG、GLFG)。
这些 FG 重复形成了 NPC 的选择性通透屏障。目前有几种模型解释其工作原理:
- 选择性相分离模型(Selective phase model):FG 重复之间的疏水相互作用形成一种"凝胶"相,排斥没有核转运受体的大分子。核转运受体(importin/exportin)表面有多个疏水口袋,可以与 FG 重复相互作用,从而"溶解"到这个凝胶中,携带货物穿过。
- 虚拟门控模型(Virtual gate model):FG 重复快速运动产生"熵屏障",大分子被排斥。核转运受体通过与 FG 重复的相互作用克服这个屏障。
- 林状纤维模型(Forest model):FG 重复形成不同高度和密度的"树林",只有与 FG 重复亲和的受体才能穿越。
无论哪种模型,核心原则是一致的:核转运受体通过与 FG 重复的疏水相互作用穿越 NPC,而不携带受体的大分子被排斥。
5.3 核定位信号(NLS)的详细分析
经典 NLS(cNLS)的两种类型:
(1)单部分 NLS(Monopartite NLS)
由一段连续的碱性氨基酸组成:
- 经典例子:SV40 大 T 抗原的 NLS:-PKKKRKV-
- 特征:4-8 个碱性氨基酸(Lys/Arg)的簇
SV40 T 抗原 NLS 的实验验证(详述):
实验 1——突变分析:
- 野生型 NLS:-Pro-Pro-Lys-Lys-Lys-Arg-Lys-Val-
- 突变型(K128T):-Pro-Pro-Lys-Thr-Lys-Arg-Lys-Val-
- 结果:仅一个氨基酸的改变就完全阻断了核进口
- 意义:证明了序列的特异性,不是简单的正电荷效应
实验 2——融合蛋白实验(pyruvate kinase 实验):
- 丙酮酸激酶(~60 kDa)正常在细胞质中
- 将 SV40 NLS 融合到丙酮酸激酶上
- 用荧光显微镜观察定位
- 正常丙酮酸激酶:弥散分布在细胞质中(核内也有少量,因为 <60 kDa 可以一定程度被动扩散入核)
- NLS-丙酮酸激酶:高度集中在细胞核中(远超被动扩散水平)
- 意义:NLS 是充分条件——将任何胞质蛋白融合 NLS 就能使其进入细胞核
(2)双部分 NLS(Bipartite NLS)
由两簇碱性氨基酸组成,中间由约 10 个氨基酸的连接区隔开:
- 经典例子:nucleoplasmin 的 NLS:-KR-PAATKKAGQA-KKKK-
- 两个碱性簇分别与 Importin-α 的两个 NLS 结合位点相互作用
非经典 NLS:
并非所有 NLS 都是碱性氨基酸簇。某些蛋白质使用非经典 NLS:
- PY-NLS:含有保守的 R/K/H-X(2-5)-PY 基序,被 Importin-β2/Transportin 直接识别
- 信号斑(Signal patch):在三维结构表面形成的 NLS,只有折叠后才存在
NLS 的关键特性总结:
- 富含 Lys 和/或 Arg
- 可以位于蛋白质的任何位置(N 端、C 端、中间)
- 不被切除(与 ER 信号肽和线粒体前导序列不同)
- 一个蛋白质可以同时含有 NLS 和 NES(决定其稳态分布)
5.4 核进口受体系统(详述)
Importin 超家族(Karyopherin-β 家族):
哺乳动物中有约 20 种 karyopherin-β 家族成员,包括进口受体和出口受体。它们的共同特征是:
- 含有约 20 个 HEAT 重复序列(Huntingtin, Elongation factor 3, PR65/A, TOR)
- HEAT 重复形成超螺旋结构,呈"弹簧"状
- 可以与 FG-Nup 的 FG 重复相互作用
- 可以与 Ran-GTP 结合(Ran 结合改变其构象,控制货物的结合/释放)
经典核进口途径(Importin-α/β 途径):
这是最早被阐明、最经典的核进口途径:
组分:
- Importin-α:适配蛋白(adaptor),N 端有自抑制的 IBB 域(Importin-β binding domain),中间有 ARM 重复(Armadillo repeat),形成凹槽识别经典 NLS
- Importin-β:转运受体,与 Importin-α 的 IBB 域结合,与 FG-Nup 相互作用
步骤: 1. 货物识别(细胞质):Importin-α 的 ARM 结构域识别货物蛋白的 NLS。同时,Importin-β 结合 Importin-α 的 IBB 域,形成三元复合物:Importin-β : Importin-α : 货物 2. 穿越 NPC:Importin-β 与 FG-Nup 的 FG 重复反复结合-解离,携带整个复合物穿过中心通道 3. 核内释放(核内):核内高浓度的 Ran-GTP 与 Importin-β 结合 → Importin-β 构象改变 → 释放 Importin-α → Importin-α 的 IBB 域自身折叠回来,竞争性地将 NLS 货物从 ARM 结构域挤出 → 货物被释放到核内 4. 受体回收:
- Importin-β-Ran-GTP 复合物回到细胞质。在细胞质,RanGAP + RanBP1 促进 Ran 水解 GTP → GDP。Ran-GDP 释放 Importin-β,Importin-β 回到可用状态。
- Importin-α 由出口受体 CAS/CSE1L 携带 Ran-GTP 从核内运出细胞质。在细胞质,Ran-GTP 水解后,CAS 释放 Importin-α。
- Ran-GDP 通过 NTF2(Nuclear Transport Factor 2)被运回核内。在核内,RCC1(RanGEF)催化 GDP → GTP 交换,维持核内 Ran-GTP 高浓度。
直接 Importin-β 途径:
某些货物蛋白不需要 Importin-α 适配蛋白,直接被 Importin-β 家族成员识别:
- Importin-β1 可以直接识别某些含 IBB-like 域的蛋白
- Importin-β2/Transportin 识别含 PY-NLS 的蛋白
- Importin-7 识别组蛋白 H1
- Importin-4 识别组蛋白 H3-H4
5.5 核出口系统(详述)
核出口信号(NES):
- 典型的 NES 是富含亮氨酸的序列
- 共识模式:Φ-X(2-3)-Φ-X(2-3)-Φ-X-Φ(Φ = 疏水氨基酸,通常是 Leu, Ile, Val, Phe, Met)
- 例如:HIV Rev 蛋白的 NES:-LPPLERLTL-
- NES 比 NLS 更难预测,因为很多蛋白质内部都有疏水氨基酸簇
CRM1/Exportin 1——主要的蛋白质出口受体:
CRM1 是最重要的蛋白质出口受体,识别富含 Leu 的 NES。
出口三元复合物的形成(在核内): 1. 核内 Ran-GTP 浓度高 2. Ran-GTP 首先与 CRM1 结合 → CRM1 构象改变 3. 构象改变后的 CRM1 现在可以识别并结合 NES 货物 4. 形成三元复合物:CRM1 : Ran-GTP : NES-货物
出口后(在细胞质): 1. RanGAP + RanBP1 促进 Ran 水解 GTP 2. Ran-GDP 不再能稳定 CRM1 的"货物结合"构象 3. CRM1 释放货物到细胞质 4. CRM1 回到核内准备下一轮出口
> 药物工具:Leptomycin B(LMB) 是 CRM1 的特异性抑制剂,通过共价修饰 CRM1 的 Cys528 来阻断 NES 识别。LMB 可以阻断几乎所有 CRM1 介导的核出口,是研究核出口的重要工具。
mRNA 出口——一条不同的途径:
值得注意的是,mRNA 的出口不使用 CRM1 途径,而是使用专门的 Mex67-Mtr2(酵母)/ NXF1-NXT1(哺乳动物)途径。mRNA 出口与 mRNA 加工(剪接、多聚腺苷酸化)紧密偶联,只有正确加工的 mRNA 才被允许出口——这是基因表达的重要质量控制步骤。
5.6 Ran GTPase 循环的全面解析
Ran 循环是理解核运输方向性的核心。让我们从最基本的原理出发:
Ran 的基本数据:
- Ran 是 Ras 超家族的小 GTPase(~25 kDa)
- 是细胞中最丰富的 GTP 结合蛋白之一
- 大部分 Ran(~80%)位于核内
Ran 梯度的建立:
| 调控因子 | 位置 | 功能 | 结果 |
|---|---|---|---|
| RCC1(RanGEF) | 核内(结合染色质) | GDP → GTP 交换 | 核内 Ran-GTP 高 |
| RanGAP1 | 细胞质(和 NPC 细胞质面) | 刺激 GTP 水解 | 胞质 Ran-GDP 高 |
| RanBP1 | 细胞质 | 辅助 RanGAP1 | 增强 GTP 水解效率 |
| NTF2 | 双向 | 将 Ran-GDP 从细胞质运回核内 | 维持核内 Ran 总量 |
为什么 RCC1 在核内?
RCC1 直接结合核小体(nucleosome),因此被锚定在染色质上。只要 DNA 在核内,RCC1 就在核内 → Ran-GTP 就在核内产生。这个简单的定位原则建立了整个 Ran 梯度。
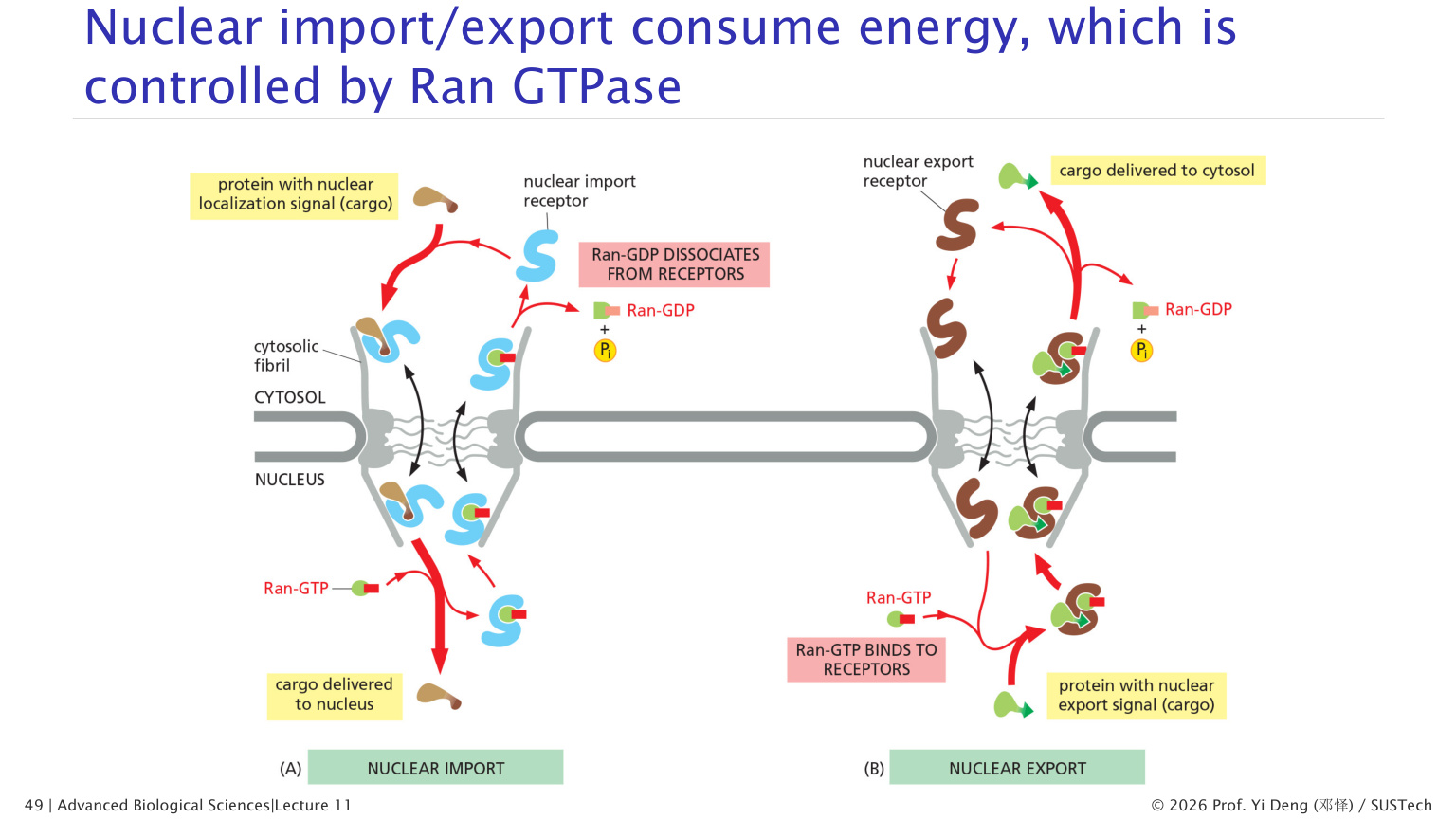
Ran 梯度如何决定运输方向——统一原则:
| 核内(Ran-GTP 高) | 细胞质(Ran-GDP 高) | |
|---|---|---|
| Importin | Ran-GTP 结合 → 释放货物 | Ran-GDP 解离 → 可结合货物 |
| Exportin | Ran-GTP 结合 → 可结合货物 | Ran-GTP 水解 → 释放货物 |
本质上,Ran-GTP 对 Importin 和 Exportin 的作用完全相反:
- 对 Importin:Ran-GTP 引起释放货物
- 对 Exportin:Ran-GTP 促进结合货物
这保证了进口货物在核内被释放,出口货物在细胞质被释放——方向性由此建立。
每次运输循环消耗多少能量?
每次 Importin 或 Exportin 的一个往返循环:
- 消耗 1 个 GTP(Ran-GTP → Ran-GDP)
- 还需要 1 个 GTP 来将 Ran-GDP 重新激活为 Ran-GTP(通过 NTF2 运回核内 + RCC1 催化交换)
- GTP 的再生需要 ATP(NDP kinase 催化:ATP + GDP → ADP + GTP)
所以,核运输本质上是消耗 ATP 驱动的过程。
5.7 NF-AT 核质穿梭的调控(全面解析)
NF-AT(Nuclear Factor of Activated T cells)家族蛋白是研究核质穿梭调控的最佳模型之一。让我们详细分析每一步。
NF-AT 的结构域组成:
N端 ─[ C1 ][ C2 ]─[ A ]─[ Z ]──────[ Rel Homology Domain (RHD) ]── C端
└─────┘ └──┘ └──────── NLS ────────────┘
Calcineurin NLS masking DNA 结合域
结合位点 domain (磷酸化位点)
另外:CKIα 结合位点位于 N 端区域关键结构域功能:
- C1/C2 域:Calcineurin(钙调磷酸酶)的结合位点。Calcineurin 必须结合到这里才能去磷酸化 NF-AT。
- A 域 + Z 域:含有被磷酸化的丝氨酸残基。磷酸化时,这个区域的构象遮盖(mask)NLS,同时暴露 NES。去磷酸化时,NLS 暴露,NES 被遮盖。
- RHD(Rel Homology Domain):DNA 结合域,与 NF-κB 家族有结构相似性。含有 NLS。
- CKIα 结合位点:CKI(Casein Kinase I)结合并在核内重新磷酸化 NF-AT。
静息状态下的 T 细胞(低 Ca²⁺):
1. NF-AT 被多种激酶磷酸化:
2. 磷酸化导致:
3. 稳态结果:NF-AT 主要位于细胞质
- CKI(Casein Kinase I):在核内和细胞质中都有活性
- GSK3(Glycogen Synthase Kinase 3):在细胞质中磷酸化
- DYRK1/2:磷酸化引发(priming)位点
- NLS masking domain 折叠回来覆盖 RHD 中的 NLS → Importin 无法识别
- NES 暴露 → CRM1 可以识别
T 细胞受体(TCR)激活后:
1. TCR 结合抗原-MHC 复合物 2. 激活 PLCγ → 产生 IP₃ 3. IP₃ → ER 释放 Ca²⁺ → 胞质 Ca²⁺ 升高 4. Ca²⁺ 与 钙调蛋白(calmodulin) 结合 5. Ca²⁺/calmodulin 激活 Calcineurin(钙调磷酸酶,丝氨酸/苏氨酸磷酸酶) 6. Calcineurin 结合 NF-AT 的 C1/C2 域 7. Calcineurin 去磷酸化 NF-AT 的多个磷酸化位点 8. 去磷酸化导致:
9. NF-AT 快速进入细胞核
- NLS masking domain 构象改变 → NLS 暴露 → Importin-α/β 识别
- NES 被遮盖 → CRM1 无法识别
NF-AT 在核内的命运:
进入核内后: 1. NF-AT 与 DNA 上的 NFAT 结合位点结合 2. 通常与 AP-1(Fos/Jun)形成复合物,共同激活靶基因 3. 靶基因包括:IL-2(T 细胞增殖的关键细胞因子)、IL-4、TNF-α、IFN-γ 等 4. 同时,核内的激酶(CKIα、GSK3 等)持续磷酸化 NF-AT 5. 只要 Calcineurin 活性存在(Ca²⁺ 持续升高),去磷酸化速率 > 磷酸化速率 → NF-AT 留在核内 6. 一旦 Ca²⁺ 信号消失 → Calcineurin 失活 → 磷酸化速率 > 去磷酸化速率 → NLS 被遮盖、NES 暴露 → CRM1 介导快速出核
> 关键概念:NF-AT 的核出口是组成性的(constitutive)——CRM1 始终可以将暴露 NES 的 NF-AT 运出核。NF-AT 的核积累完全依赖于持续的 Ca²⁺/Calcineurin 信号来维持去磷酸化状态。这使得 NF-AT 成为 Ca²⁺ 信号的忠实传感器——信号在,NF-AT 在核内;信号消失,NF-AT 立即出核。
动态成像实验:
用 GFP-NF-AT4 融合蛋白的实时成像清楚展示了这种动态穿梭:
- 刺激 T 细胞(Ca²⁺ 升高):GFP 荧光在 ~8 分钟内从细胞质转移到核内(Import)
- 去除刺激(Ca²⁺ 降低):GFP 荧光在 ~20 分钟内回到细胞质(Export)
- 再次刺激:可以再次快速入核(Re-import)
免疫抑制药物的作用机制:
两种最重要的移植免疫抑制剂都通过阻断 Calcineurin 来抑制 NF-AT 的核进口:
环孢素 A(Cyclosporin A, CsA):
- 来源:真菌代谢产物
- 机制:CsA 与亲环蛋白(cyclophilin)结合 → CsA-cyclophilin 复合物抑制 Calcineurin → NF-AT 不能去磷酸化 → 不能入核 → T 细胞不能激活 → 免疫抑制
FK506/他克莫司(Tacrolimus):
- 来源:链霉菌代谢产物
- 机制:FK506 与 FKBP12 结合 → FK506-FKBP12 复合物抑制 Calcineurin → 同样的下游效应
- 药效比 CsA 更强(约 100 倍)
这两种药物是器官移植后防止排斥反应的基石药物,每年挽救成千上万的生命。它们的发现也反向验证了 NF-AT/Calcineurin 途径在 T 细胞激活中的核心地位。
5.8 Digitonin 透化实验——鉴定核运输因子的经典方法(详述)
这个实验体系的建立是核运输领域的里程碑,值得详细理解。
Digitonin 的选择性透化原理:
Digitonin 是一种甾体皂苷(steroid saponin),从毛地黄植物中提取。它的关键化学特性是:
- 与胆固醇(cholesterol)有高亲和力
- 在低浓度下,digitonin 与质膜中的胆固醇相互作用,在膜上形成孔洞,使质膜变得可透性
- 核膜的胆固醇含量远低于质膜,因此在同样浓度的 digitonin 下,核膜不受影响
不同膜的胆固醇含量:
- 质膜:~30-40%(占膜脂的比例)→ 容易被 digitonin 透化
- ER 膜:~5%
- 线粒体内膜:<5%
- 核膜:~10% → 在适当的 digitonin 浓度下不受影响
实验流程:
1. 将培养的细胞(如 HeLa 细胞或 BHK 细胞)用低浓度(~40-50 μg/ml)digitonin 处理 ~5 分钟 2. 质膜被透化 → 细胞质内容物(包括可溶性蛋白、核糖体、小分子等)流出 3. 洗涤去除 digitonin 和溢出的细胞质 4. 现在的细胞:质膜有孔(可进入),核膜和 NPC 完好 5. 加入以下成分:
6. 用荧光显微镜观察核内荧光积累
- 荧光标记的 NLS-蛋白(如 fluorescein-BSA-NLS)作为报告分子
- 测试不同条件:
- 仅加报告分子(无胞质因子)
- 加报告分子 + 胞质提取物
- 加报告分子 + 纯化的 Importin-α + Importin-β + Ran-GTP + NTF2 + ATP
结果:
| 条件 | 核内荧光 | 解释 |
|---|---|---|
| 报告分子 alone | 无/很少 | 缺乏运输因子 |
| + 完整胞质提取物 | 强 | 含所有必需因子 |
| + Importin-α/β + Ran-GDP + NTF2 + ATP 再生系统 | 强 | 确认最小必需因子 |
| + Importin-α/β(无 Ran) | 结合 NPC 但不释放 | Ran 是释放货物到核内所必需的 |
| + ATP 耗尽 | 无 | 核运输是耗能过程 |
这个实验体系还被用来进一步鉴定了:
- Importin-α 和 Importin-β 的各自角色
- Ran 的 GTP/GDP 循环
- NTF2 的功能
- CAS 作为 Importin-α 出口受体的角色
---
总结与综合对比
各运输途径的全面对比
| 特征 | ER 进口 | 线粒体基质进口 | 过氧化物酶体进口 | 核进口 | 核出口 |
|---|---|---|---|---|---|
| 信号类型 | N 端信号肽(疏水) | N 端前导序列(两亲性α螺旋) | PTS1(C 端-SKL)或 PTS2 | NLS(Lys/Arg 富集) | NES(Leu 富集) |
| 信号位置 | N 端 | N 端 | C 端或 N 端 | 任意 | 任意 |
| 信号切除 | 是(SPase) | 是(MPP) | 通常否 | 否 | 否 |
| 受体 | SRP | Tom20/Tom22/Tom70 | Pex5/Pex7 | Importin-α/β | CRM1 (Exportin 1) |
| 通道 | Sec61 | TOM + TIM23 | Pex 复合物(瞬时) | NPC(FG-Nup) | NPC(FG-Nup) |
| 蛋白折叠状态 | 未折叠(共翻译) | 未折叠 | 折叠态 | 折叠态 | 折叠态 |
| 运输时机 | 共翻译(主要) | 翻译后 | 翻译后 | 翻译后 | 翻译后 |
| 能量来源 | GTP(SRP/SR) | Δψ + ATP(mtHsp70) | ATP(Pex1/Pex6) | GTP(Ran 循环) | GTP(Ran 循环) |
| 膜层数 | 1 层 | 2 层(同时) | 1 层 | 2 层(但通过孔) | 2 层(但通过孔) |
| 分子伴侣 | BiP(翻译后转运) | Hsp70/90(胞质)+ mtHsp70(基质) | — | — | — |
三种运输机制的核心逻辑
1. 门控运输(核运输):蛋白质保持折叠态,通过巨大的 NPC(~40 nm 通道),由 Importin/Exportin 识别信号并穿越 FG 屏障。方向性由 Ran-GTP 梯度控制。
2. 跨膜运输(ER、线粒体等):蛋白质必须解折叠(大多数情况),通过膜上的蛋白质通道(~1-2 nm 内径)穿过脂双层。方向性由信号序列被受体识别 + 膜另一侧的"拉力"(分子伴侣或膜电位)驱动。
3. 囊泡运输(分泌途径):蛋白质始终在膜内(腔内或嵌在膜中),通过膜泡的出芽和融合在细胞器之间传递。方向性由被膜蛋白(coat proteins)、SNARE 和 Rab GTPase 控制。
---
本讲义基于 SUSTech 邓怿教授 Lecture 11 课件整理并大幅扩展,参考教材:Molecular Biology of the Cell (Alberts et al., 7th Ed)、Molecular Cell Biology (Lodish et al., 9th Ed)、Essential Cell Biology (Alberts et al.)。适合零基础到进阶学习使用。