Lecture 12
Lecture 12: 细胞内囊泡运输 (Intracellular Vesicular Traffic)
学习笔记 — 基于邓怿教授 (SUSTech) 课件整理
---
写在前面:为什么要学囊泡运输?
真核细胞内部有许多膜包裹的"房间"(细胞器),每个房间里住着不同的蛋白质和酶,各司其职。问题来了:一个在内质网(ER)上合成的蛋白质,怎么准确地被送到高尔基体、溶酶体、或者细胞表面? 答案就是——囊泡运输(vesicular traffic)。细胞用小小的膜泡(vesicle)像"快递包裹"一样,把货物从一个细胞器精确运送到另一个细胞器。
---
第一部分:囊泡运输概述 (Overview of Vesicular Traffic)
1.1 历史背景:George Palade 的开创性工作
George Palade(1912–2008),耶鲁大学,1974年诺贝尔生理学或医学奖得主。他被誉为"现代细胞生物学之父",第一个用电子显微镜系统描绘了细胞内的分泌通路。
他在1975年发表于 Science 的经典论文中,绘制了细胞内运输的路线图:蛋白质从粗面内质网 → 高尔基体 → 分泌囊泡 → 细胞外。
1.2 Jamieson & Palade 的脉冲追踪实验 (Pulse-Chase Experiment)
这是理解分泌途径的经典实验,步骤如下:
实验材料:豚鼠胰腺切片(pancreas,是分泌蛋白质的"专业选手")
实验步骤:
1. 脉冲(Pulse)阶段:将胰腺薄切片放入含放射性亮氨酸的培养基中短暂培养。放射性亮氨酸会被掺入到正在合成的蛋白质中,相当于给蛋白质"贴了标签"。
2. 追踪(Chase)阶段:把切片转移到含非放射性亮氨酸的培养基中继续培养。此时新合成的蛋白质不再被标记,我们就可以追踪那些已经标记了的蛋白质去了哪里。
实验结果(通过放射自显影观察银颗粒的位置):
| 时间点 | 放射性标记的位置 | 含义 |
|---|---|---|
| 3 分钟 | 内质网 (ER) | 蛋白质刚刚合成,还在ER中 |
| 10 分钟 | 高尔基体 (Golgi) | 蛋白质已经从ER转运到Golgi |
| 40 分钟 | 分泌囊泡 (secretory vesicles) | 蛋白质已经被包装到分泌囊泡中,准备分泌 |
核心结论:蛋白质沿着 ER → Golgi → 分泌囊泡 的路线依次运输,这个过程是有序的、定向的。
1.3 用荧光显微镜实时观察蛋白质运输
工具:VSVG-GFP(水泡性口炎病毒 G 蛋白与绿色荧光蛋白的融合体)
巧妙之处:这个蛋白有一个温度敏感突变(ts045)——
- 40°C:蛋白质发生错误折叠,被滞留在 ER 中
- 32°C:蛋白质正确折叠,作为一个同步群体从 ER → Golgi → 质膜 依次移动
这让科学家可以像看电影一样,实时追踪一波蛋白质从 ER 出发、经过 Golgi、最终到达质膜的全过程。荧光定量分析显示:ER 的荧光先下降,Golgi 的荧光先升后降,质膜的荧光持续上升——完美符合"接力运输"模型。
1.4 囊泡运输的核心问题
关于囊泡运输,细胞需要解决四个关键问题:
1. 囊泡如何形成?(Vesicle formation / budding) 2. 囊泡如何从原始膜上剪切下来?(Vesicle fission) 3. 囊泡如何与靶膜融合?(Vesicle fusion) 4. 整个过程如何被精确调控?(Regulation)
1.5 2013年诺贝尔生理学或医学奖
James Rothman、Randy Schekman 和 Thomas Südhof 因发现调控囊泡运输的分子机器而共同获奖。他们分别用不同的方法揭示了这个系统的核心组件。
1.6 Schekman 的酵母遗传学方法
Randy Schekman 使用出芽酵母(Saccharomyces cerevisiae)进行遗传筛选。
策略:寻找温度敏感(Ts)突变体——
- 在允许温度 24°C 正常生长和分泌
- 在限制温度 37°C 分泌受阻
筛选方法:
1. 在主平板上培养酵母菌落 2. 复制到两块平板:一块 24°C,一块 37°C 3. 对分泌酶活性进行染色检测 4. 在 37°C 下分泌减少的菌落就是候选突变体
关键发现:鉴定了一系列 sec 突变体(secretion-defective),这些突变体在限制温度下出现不同的表型。通过电子显微镜观察,可以看到 sec1 突变体在限制温度下积累了大量囊泡(vesicles, Ve),而在允许温度下形态正常。
1.7 五类 sec 突变体揭示分泌通路的顺序
根据突变体在限制温度下蛋白质积累的位置,可以分为五类:
| 类别 | 蛋白积累位置 | 受损功能 |
|---|---|---|
| Class A | 细胞质中 | 进入 ER 的转运 |
| Class B | 粗面 ER 中 | 从粗面 ER 出芽形成囊泡 |
| Class C | ER-Golgi 转运囊泡中 | 转运囊泡与 Golgi 的融合 |
| Class D | Golgi 中 | 从 Golgi 到分泌囊泡的转运 |
| Class E | 分泌囊泡中 | 分泌囊泡到细胞表面的转运 |
意义:通过双突变体分析(将两类突变组合),可以确定各步骤的先后顺序。这就像交通堵塞——如果在路上的两个不同点同时设置路障,车辆只会堵在前面那个路障处。
1.8 Rothman 的体外生化方法
James Rothman 使用体外囊泡出芽实验(in vitro vesicle budding assay):
基本原理:
1. 从细胞中分离供体膜(microsomes 或半完整细胞) 2. 加入待测蛋白质 + GTP 3. 孵育后离心(13,000g)分离囊泡 4. 用电子显微镜观察是否产生囊泡
通过这种方法,可以逐一添加或去除蛋白质,确定哪些是囊泡形成必需的。用TEM(透射电镜)观察,可以看到约 100 nm 大小的囊泡,表面覆盖着蛋白质外壳。
1.9 囊泡有蛋白质外套 (Coat Proteins)
运输囊泡的表面覆盖着特定的外套蛋白(coat proteins)。
外套蛋白的功能:
1. 驱动膜的弯曲和囊泡形成:外套蛋白组装成笼状结构,把平坦的膜"拱"成球形 2. 选择货物:通过与货物蛋白质上的分选信号结合,确保正确的蛋白质被装入囊泡 3. 决定运输方向:不同类型的外套蛋白介导不同方向的运输
1.10 三种主要的被膜囊泡
| 囊泡类型 | 外套蛋白 | 运输方向 |
|---|---|---|
| COPII | Sec23/24, Sec13/31, Sar1 | ER → Golgi(顺行运输) |
| COPI | coatomer (α-ζ七个亚基) | Golgi → ER(逆行运输),Golgi 内转运 |
| Clathrin | clathrin + 接头蛋白 (AP) | TGN → 内体/溶酶体,质膜 → 内体(内吞) |
记忆技巧:COPII = "二号往前走"(ER→Golgi),COPI = "一号往回走"(Golgi→ER)。
1.11 GTP酶控制外套蛋白的组装与解聚
核心发现:在体外出芽实验中加入不可水解的 GTP 类似物(如 GTPγS),会导致被膜囊泡大量积累。
为什么? 因为外套蛋白的组装和解聚受到小GTP酶(small GTPase)的调控:
- GTP 结合态(活性态)→ 招募外套蛋白,促进囊泡出芽
- GTP 水解为 GDP(非活性态)→ 外套蛋白脱落(uncoating)
如果 GTP 不能被水解,外套蛋白就无法脱落,囊泡就一直穿着"外套"——无法与靶膜融合。
两种关键的外套招募 GTP 酶:
| GTP酶 | 控制的囊泡类型 |
|---|---|
| Sar1 (Secretion-Associated Ras-superfamily-related protein 1) | COPII 囊泡 |
| ARF (ADP-Ribosylation Factor) | COPI 和 clathrin 囊泡 |
1.12 Sar1 如何招募 COPII 外套蛋白
COPII 囊泡形成的详细步骤:
1. Sec12(是 Sar1 的 GEF,即鸟苷酸交换因子)位于 ER 膜上 2. Sec12 将 Sar1 上的 GDP 换成 GTP → Sar1 被激活 3. 活化的 Sar1-GTP 暴露出疏水性 N 端,像"锚"一样插入 ER 膜 4. Sar1-GTP 招募 Sec23/Sec24 内层外套复合物
5. 最后招募 Sec13/Sec31 外层外套,形成完整的 COPII 笼状结构
- Sec24:负责识别和结合货物蛋白(cargo sorting)
- Sec23:是 Sar1 的 GAP(GTP酶活化蛋白),能促进 GTP 水解
重要概念:GEF 和 GAP
| 蛋白 | 全名 | 功能 |
|---|---|---|
| GEF | Guanine nucleotide Exchange Factor | 催化 GDP → GTP,激活 GTPase |
| GAP | GTPase-Activating Protein | 促进 GTP 水解为 GDP,失活 GTPase |
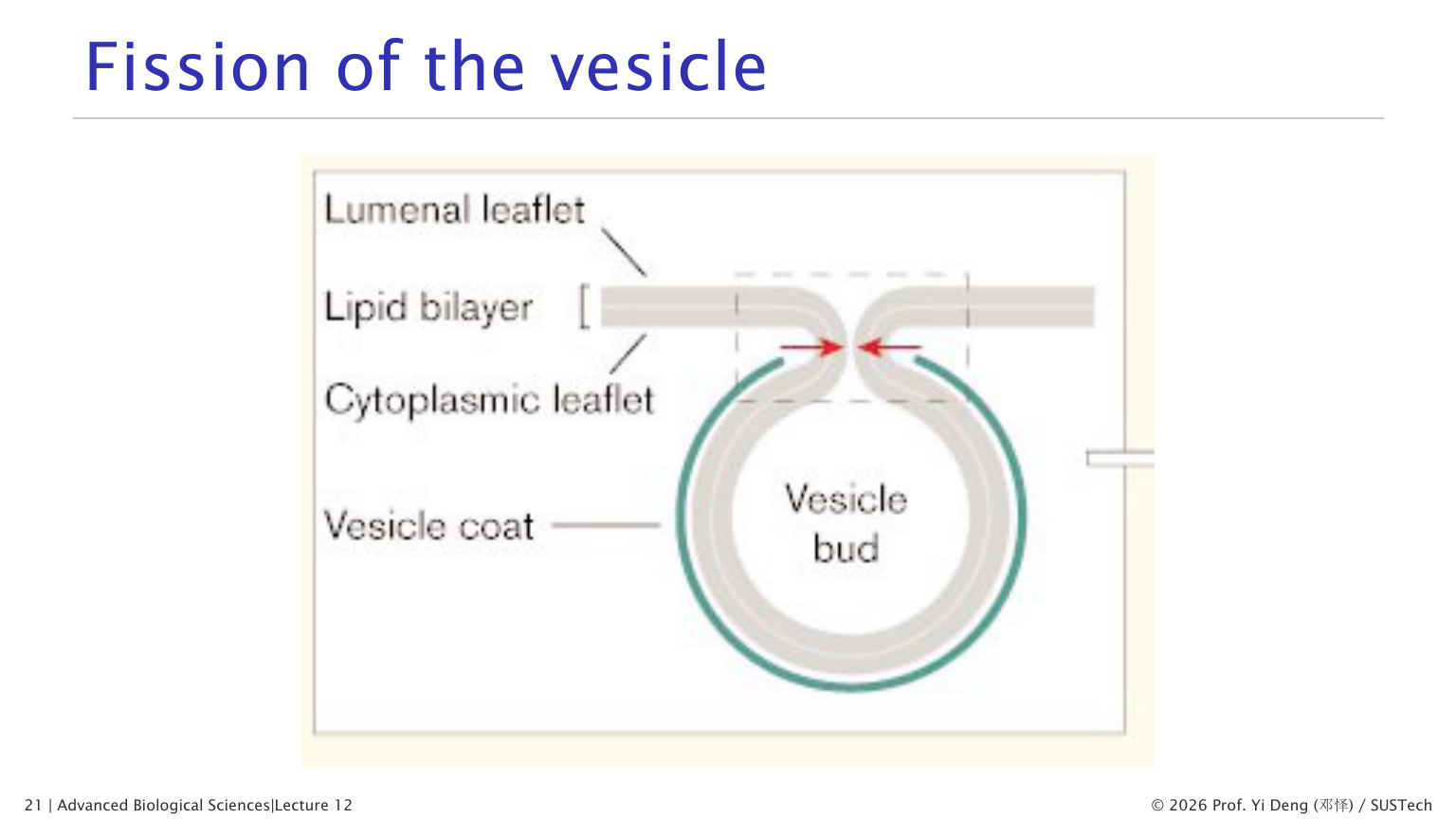
1.13 囊泡的剪切 (Fission)
当外套蛋白将膜弯曲到一定程度后,囊泡颈部的膜需要被"剪断"才能完全脱离供体膜。这个过程涉及膜的重组——两层脂双层(细胞质面小叶和腔面小叶)在颈部融合并断裂,形成独立的囊泡。
1.14 Rothman 发现膜融合所需的蛋白质
Rothman 的巧妙实验——体外囊泡运输重建:
实验设计:
- 供体 Golgi("Donor"):含有 VSV-G 蛋白(在 cis-Golgi 中),但缺少糖基转移酶
- 受体 Golgi("Acceptor"):含有糖基转移酶(在 medial-Golgi 中),但没有 VSV-G
检测方法:如果 VSV-G 蛋白被转运到受体 Golgi,糖基转移酶就会在 VSV-G 上添加放射性糖基,可以通过测量放射性来定量转运效率。
结果:放射性标记随时间增加,说明 VSV-G 确实通过囊泡从供体转运到了受体。
1.15 NEM 的发现——通往 NSF 和 SNARE 的线索
NEM(N-ethylmaleimide,N-乙基马来酰亚胺) 是一种化学试剂,能修饰蛋白质上的巯基(-SH)。
关键发现:加入 NEM 后,囊泡运输被阻断。但阻断发生在融合步骤,而非出芽步骤——细胞中积累了大量约 70 nm 的未被膜囊泡(uncoated vesicles),它们携带着 VSV-G 蛋白,但无法与靶膜融合。
这说明:存在某种对 NEM 敏感的细胞质蛋白,对膜融合至关重要。
1.16 SNARE 蛋白介导膜融合的特异性
NSF:N-ethylmaleimide-Sensitive Factor(NEM 敏感因子)——正是上面实验中被 NEM 抑制的那个蛋白。NSF 是一种 ATPase。
SNARE:Soluble NSF Attachment protein Receptor(可溶性 NSF 附着蛋白受体)
SNARE 蛋白介导膜融合的机制:
1. v-SNARE(vesicle-SNARE):位于囊泡膜上 2. t-SNARE(target-SNARE):位于靶膜上 3. v-SNARE 和 t-SNARE 相互识别并缠绕,形成trans-SNARE 复合物(跨膜 SNARE 束),将两层膜拉近 4. 膜被拉得足够近后发生融合 5. 融合后,NSF 利用 ATP 水解的能量,将 SNARE 复合物拆开(dissociation),回收利用
特异性:不同的细胞器有不同的 SNARE 蛋白组合,只有匹配的 v-SNARE / t-SNARE 才能形成稳定的复合物,从而确保囊泡只与正确的靶膜融合。
1.17 Rab 蛋白引导囊泡到达靶膜
Rab 蛋白 是另一个大家族的小 GTP 酶(人类有超过 60 种),每种 Rab 蛋白定位在不同的细胞器膜上。
Rab 蛋白介导的三步曲:
1. 系留(Tethering):Rab-GTP(活性态)招募系留因子(tethering factors),在远距离"抓住"运输囊泡 2. 对接(Docking):囊泡被拉近靶膜 3. 融合(Fusion):v-SNARE 和 t-SNARE 形成 trans-SNARE 复合物,驱动膜融合
融合后,Rab 蛋白上的 GTP 被水解为 GDP,Rab-GDP 被 GDI(GDP Dissociation Inhibitor,GDP 解离抑制因子)从膜上取下,送回细胞质中循环利用。
1.18 囊泡运输的完整流程总结
一个运输囊泡的"生命周期":
1. 出芽(Budding):GTP 酶激活 → 招募外套蛋白 → 选择货物 → 膜弯曲 → 囊泡形成 2. 运动(Movement):囊泡沿细胞骨架(微管)运动,由马达蛋白驱动 3. 系留(Tethering):Rab 蛋白和系留因子将囊泡"捕获"到靶膜附近 4. 融合(Fusion):SNARE 蛋白介导膜融合,货物被释放
参与的分子角色:
| 分子 | 功能 |
|---|---|
| 外套蛋白(coat protein) | 驱动囊泡形成,选择货物 |
| 货物受体(cargo receptor) | 识别并结合要运输的蛋白质 |
| 马达蛋白(motor protein) | 沿细胞骨架运动 |
| 系留因子(vesicle tether) | 远距离捕获囊泡 |
| v-SNARE / t-SNARE | 介导膜融合 |
| Rab GTPase | 调控系留和融合 |
---
第二部分:从 ER 到 Golgi 的运输
2.1 蛋白质通过 COPII 囊泡离开 ER
COPII 外套的组成(前面已经介绍):
- Sar1-GTP:插入膜中,启动过程
- Sec23/Sec24(内层外套):Sec24 识别货物上的ER 出口信号(exit signal)
- Sec13/Sec31(外层外套):形成笼状结构
货物的选择:
- 膜蛋白(membrane-bound cargo):在其细胞质面结构域上携带分选信号,直接被 Sec24 识别
- 可溶性分泌蛋白(soluble cargo):不直接与外套蛋白接触,而是通过膜蛋白受体间接被选入囊泡(受体的细胞质面与 Sec24 结合,腔面与可溶性货物结合)
- 未折叠/错误折叠的蛋白:被 ER 中的分子伴侣(如 BiP) 结合并滞留,不能离开 ER
2.2 ER 出口需要正确的蛋白折叠
核心原则:只有正确折叠和组装的蛋白质才能离开 ER。
以 IgG(免疫球蛋白 G)的组装为例:
1. 抗体重链被合成后,立即被分子伴侣 BiP 结合并滞留在 ER 中 2. 轻链合成后与重链组装 3. 组装过程中 BiP 逐渐释放 4. 只有当 2 条重链 + 2 条轻链完全组装成 Y 形四聚体后,BiP 完全释放,抗体才能被装入 COPII 囊泡分泌出去
如果亚基缺失或折叠错误,BiP 不释放,蛋白质就永远留在 ER 中。这是 ER 的质量控制(quality control) 机制。
2.3 COPII 囊泡不都是圆球形
有趣的发现:COPII 外套是一个灵活的系统,可以形成不同形状的囊泡:
- 小的球形囊泡(~60-80 nm):运输常规大小的蛋白质
- 大的管状囊泡:运输超大货物,如原胶原(procollagen)——长约 300 nm 的三螺旋纤维,根本装不进小囊泡!
要形成管状囊泡,需要额外的包装蛋白(packaging proteins) 与 Sec13/Sec31 外套配合。
2.4 囊泡管状簇 (VTCs) 和 ER 出口位点
ER 出口位点(ERES, ER Exit Site):ER 膜上的特定区域,没有核糖体(称为过渡性 ER,transitional ER),是 COPII 囊泡出芽的地方。
VTC(Vesicular-Tubular Cluster):
- COPII 囊泡从 ERES 出芽后,不是直接飞到 Golgi,而是先在附近聚集形成 VTC
- VTC 也叫 ERGIC(ER-Golgi 中间区室)
- VTC 沿着微管向 Golgi 方向运动
- 在 VTC 阶段,COPI 囊泡已经开始形成,执行逆行运输(将 ER 驻留蛋白送回 ER)
2.5 高尔基体的形态和结构
高尔基体不是简单的"一摞煎饼"!
高尔基体由一系列功能不同的扁平囊状结构(cisternae)堆叠而成,不同层具有不同的酶:
| 区域 | 主要功能 |
|---|---|
| cis-Golgi 网络 (CGN) | 分选站;溶酶体蛋白的寡糖磷酸化 |
| cis 面 | 去除甘露糖残基 |
| medial 面 | 去除甘露糖;添加 GlcNAc |
| trans 面 | 添加半乳糖 (Gal);添加唾液酸 (NANA) |
| trans-Golgi 网络 (TGN) | 酪氨酸和碳水化合物的硫酸化;最终分选站——蛋白质被分拣到溶酶体、质膜或分泌囊泡 |
方向性:cis 面朝向细胞核/ER,trans 面朝向质膜。
高尔基体的cisternae之间有管状连接,整体结构比教科书上画的复杂得多。
2.6 高尔基体内部运输的两种模型
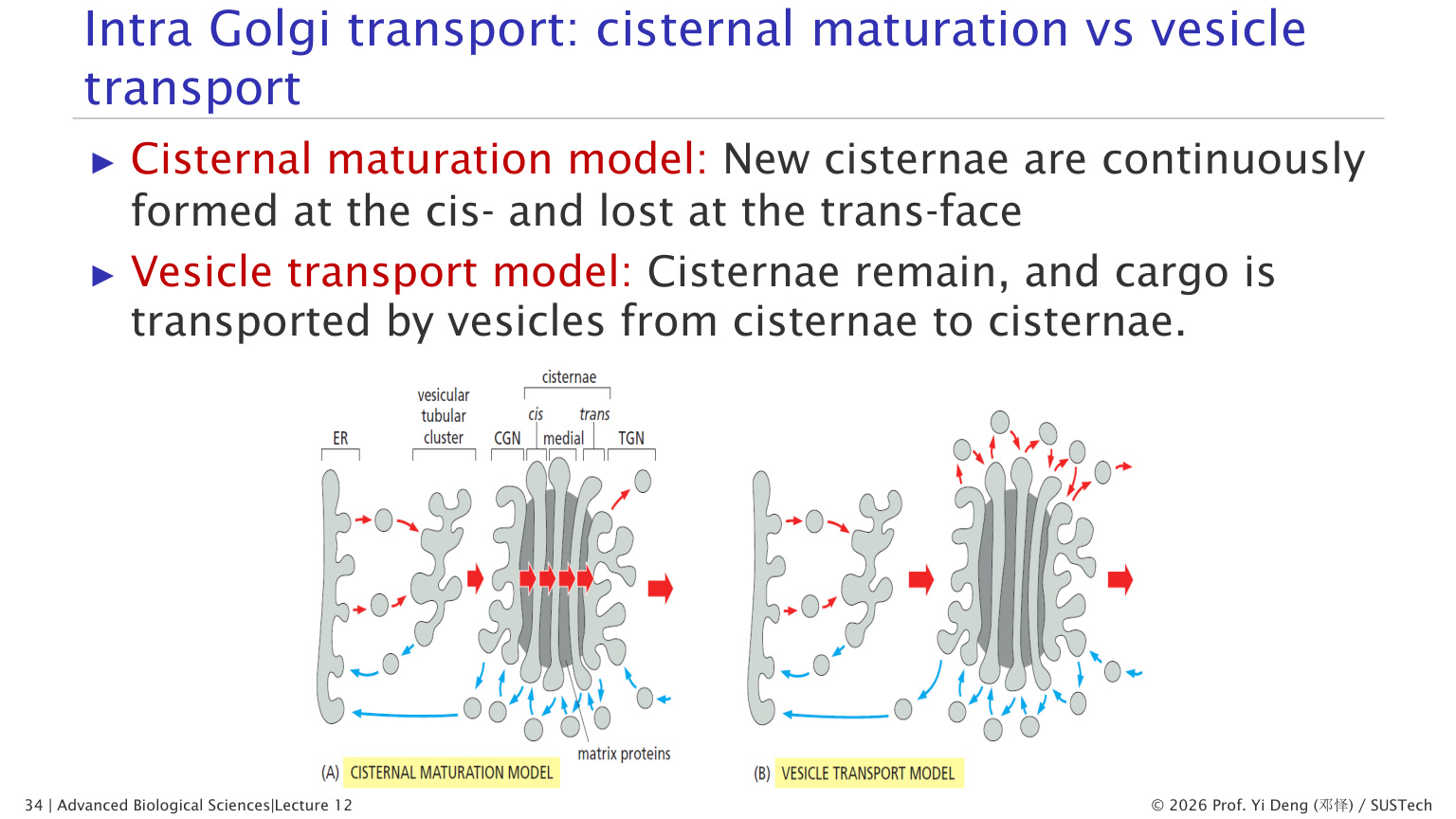
关于蛋白质如何穿过高尔基体的多层结构,有两种模型之争:
模型 A:囊池成熟模型(Cisternal Maturation Model)
- 新的 cisterna 在 cis 面不断形成,旧的在 trans 面不断消解
- 整个 cisterna 带着货物一起"向前走"
- 酶通过 COPI 囊泡逆行运输,从成熟的 cisterna 被送回到较年轻的 cisterna
- 这个模型能解释大型货物(如原胶原纤维)如何穿过 Golgi——它们太大了,装不进小囊泡
模型 B:囊泡运输模型(Vesicle Transport Model)
- Cisternae 是固定不动的
- 货物通过囊泡从一层 cisterna 转运到下一层
目前的共识:两种机制可能同时存在,不同类型的货物可能使用不同的机制。
2.7 COPI 介导的逆行运输
为什么需要逆行运输?
ER 中有很多驻留蛋白(如分子伴侣 BiP),它们本不应该离开 ER,但有时会意外地被"裹挟"进 COPII 囊泡中。COPI 囊泡的一个重要功能就是把这些"泄漏"出去的 ER 蛋白送回来。
2.8 ER 检索信号 (ER Retrieval Signals)
ER 驻留蛋白之所以能被"找回来",是因为它们携带特定的检索信号:
| 蛋白类型 | 检索信号 | 识别机制 |
|---|---|---|
| ER 驻留膜蛋白 | C 端 KKXX 基序 | 直接被 COPI 外套识别 |
| ER 驻留可溶性蛋白 | C 端 H/KDEL 序列 | 被 KDEL 受体识别 |
KDEL 受体的工作机制(非常巧妙):
- KDEL 受体是一个跨膜蛋白,在 ER 和 Golgi 之间穿梭
- 在 Golgi 中(pH 较低,H⁺浓度较高):KDEL 受体与带有 KDEL 信号的蛋白高亲和力结合
- 结合后,KDEL 受体-货物复合物被装入 COPI 囊泡,送回 ER
- 在 ER 中(pH 较高):KDEL 受体释放货物
- 空的 KDEL 受体再通过 COPII 囊泡回到 Golgi,准备下一轮运输
利用 pH 差异来调控结合/释放——这是细胞中反复出现的精妙设计!
2.9 ER → Golgi 运输总结
要点回顾:
- COPII 囊泡从 ER 出口位点(ERES)出芽,介导 ER → Golgi 的顺行运输
- 膜蛋白通过细胞质面的出口信号被选入 COPII 囊泡
- 可溶性分泌蛋白通过"批量流动(bulk-flow)"或受体介导进入 COPII 囊泡
- 只有正确折叠的蛋白才能离开 ER(质量控制)
- COPI 囊泡介导逆行运输,将 ER 驻留蛋白送回
- ER 驻留蛋白靠 KKXX(膜蛋白)或 H/KDEL(可溶性蛋白)信号被检索回来
---
第三部分:蛋白质糖基化 (Protein Glycosylation)
3.1 两种糖基化类型
糖基化是在蛋白质上添加糖链的翻译后修饰,对蛋白质的折叠、稳定性、识别和功能都很重要。
| 类型 | 连接位点 | 连接方式 | 起始位置 |
|---|---|---|---|
| N-糖基化 | 天冬酰胺 (Asn) 的酰胺氮 | N-乙酰葡糖胺 (GlcNAc) 连接到 Asn | ER(开始),Golgi(修饰) |
| O-糖基化 | 丝氨酸 (Ser) 或苏氨酸 (Thr) 的羟基氧 | N-乙酰半乳糖胺 (GalNAc) 连接到 Ser/Thr | Golgi |
3.2 N-糖基化的详细过程
第一步:在 ER 中的 en bloc 转移
N-糖基化有一个识别序列:Asn-X-Ser/Thr(X 可以是除 Pro 以外的任何氨基酸)。
过程:
1. 一个预制的 14 糖寡聚糖(3 葡萄糖 + 9 甘露糖 + 2 GlcNAc)被连接在 ER 膜中的多萜醇磷酸(dolichol-P)上 2. 当新生肽链从核糖体中伸出、进入 ER 腔时,寡糖基转移酶(oligosaccharyl transferase, OST) 将整个 14 糖一次性(en bloc) 转移到 Asn 上 3. 然后在 ER 腔中,3 个葡萄糖和 1 个甘露糖被酶移除(糖修剪)
第二步:两种最终产物
| 类型 | 特征 | 产生位置 |
|---|---|---|
| 高甘露糖型(High-mannose) | 主要含甘露糖残基 | 只在 ER 中修剪 |
| 复杂型(Complex) | 含多种糖(GlcNAc, Gal, NANA/唾液酸) | 在 Golgi 中进一步修饰 |
3.3 Golgi 中的 N-糖基化修饰
在蛋白质通过 Golgi 的不同层时,糖链被不同的酶依次修饰:
| Golgi 层 | 酶 | 反应 |
|---|---|---|
| Cis | 甘露糖苷酶 I (Mannosidase I) | 移除甘露糖残基 |
| Medial | GlcNAc 转移酶 | 添加 GlcNAc |
| Medial | 甘露糖苷酶 II (Mannosidase II) | 进一步移除甘露糖 |
| Trans | 多种转移酶 | 添加半乳糖 (Gal)、唾液酸 (NANA/Sialic acid) |
这个过程就像流水线——蛋白质通过不同的"车间",在每个车间接受不同的加工。
3.4 O-糖基化
O-糖基化完全发生在 Golgi 中(不同于 N-糖基化从 ER 开始)。
两种最重要的 O-糖基化:
1. 黏蛋白型 O-聚糖(Mucin-type O-glycans):GalNAc 连接到 Ser/Thr → 常见于黏蛋白,保护上皮表面 2. 糖胺聚糖(GAG)链:木糖 (Xylose) 连接到 Ser → 形成蛋白聚糖(proteoglycans)的长糖链
---
第四部分:从 TGN 到溶酶体的运输
4.1 溶酶体的基本特征
溶酶体(Lysosome) 是细胞的"消化工厂":
- 大小:0.2–0.5 μm
- 内部 pH:~5.0(酸性环境,由 V-ATPase(H⁺泵) 维持)
- 细胞质 pH:~7.2
- 含有约 40 种酸性水解酶:包括核酸酶、蛋白酶、糖苷酶、脂酶、磷酸酶、硫酸酶、磷脂酶等
- 膜特征:限制膜(limiting membrane)上有高度糖基化的膜蛋白(如 LAMP1, LAMP2, LAMP3)保护膜免受自身酶的消化;含有腔内囊泡(intraluminal vesicles, ILVs)和特殊脂质溶血双磷脂酸(lyso-bisphosphatidic acid)
4.2 M6P 是溶酶体酶的分选信号
问题:溶酶体的酸性水解酶是在 ER 中合成的,它们怎么知道要去溶酶体而不是被分泌出去?
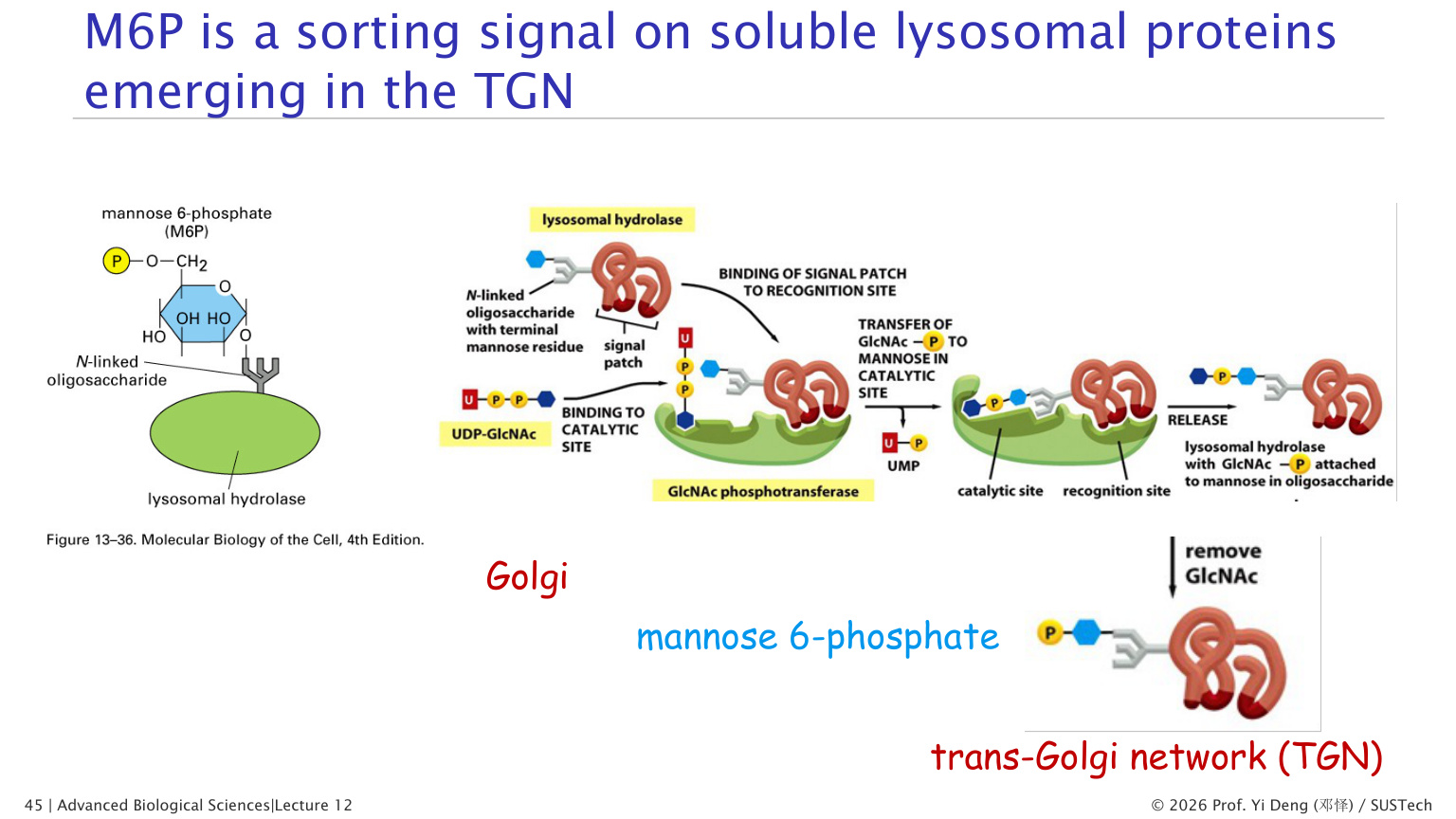
答案:甘露糖-6-磷酸(Mannose-6-Phosphate, M6P) 信号!
M6P 信号的产生过程(在 Golgi 中):
1. 溶酶体水解酶前体的三维结构上有一个信号补丁(signal patch)——不是线性序列,而是蛋白质折叠后在表面形成的三维构象 2. GlcNAc 磷酸转移酶识别这个信号补丁,将 GlcNAc-磷酸添加到酶上 N-聚糖的甘露糖残基上 3. 然后另一个酶将 GlcNAc 移除,暴露出磷酸基团,形成 M6P 标签
4.3 M6P 如何将蛋白质靶向溶酶体
1. 在 TGN 中,带有 M6P 标签的溶酶体水解酶前体与 M6P 受体(MPR, Mannose-6-Phosphate Receptor) 结合 2. MPR 的细胞质面被 clathrin 外套 识别(通过接头蛋白),形成 clathrin 包被囊泡 3. 囊泡被运输到早期内体 (early endosome) 4. 在内体的酸性 pH 中,M6P-水解酶与 MPR 解离 5. 水解酶前体继续前往晚期内体/溶酶体,在那里被激活(酸性 pH 下前肽被切除) 6. 空的 MPR 通过 retromer(逆转录复合体) 介导的囊泡被回收到 TGN,重复使用 7. 水解酶上的磷酸基团也被移除
retromer 是一个非常重要的蛋白复合物,负责将 MPR 从内体回收到 TGN。retromer 功能障碍与神经退行性疾病有关。
---
第五部分:分泌和胞吐 (Secretion and Exocytosis)
5.1 两种分泌途径
| 类型 | 存在细胞 | 特点 | 货物举例 |
|---|---|---|---|
| 组成型分泌(Constitutive) | 所有真核细胞 | 持续进行,不需要外部信号 | 质膜蛋白、脂质、ECM 蛋白 |
| 调控型分泌(Regulated) | 专职分泌细胞 | 需要外部信号触发 | 激素、组胺、神经递质、消化酶 |
5.2 分泌囊泡的形成过程
以胰腺 β 细胞为例:
1. 在 TGN 中,分泌蛋白(如胰岛素原)开始聚集浓缩 2. 形成未成熟分泌囊泡(immature secretory vesicle) 3. Clathrin 包被囊泡(CCVs) 从未成熟囊泡上出芽,将多余的膜和非分泌蛋白送回 TGN(逆行运输) 4. 通过不断移除膜,囊泡体积缩小,货物进一步浓缩 5. 形成成熟分泌囊泡(mature secretory vesicle)——货物高度浓缩的"弹药库"
5.3 Ca²⁺ 调控的神经递质释放
Thomas Südhof 的贡献——揭示 Ca²⁺ 如何触发突触囊泡释放。
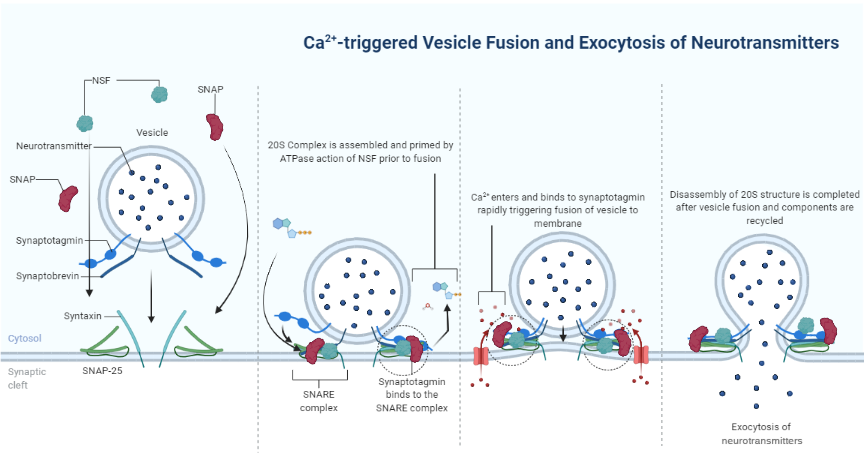
突触囊泡的融合机制(5 步):
1. 对接(Docking):突触囊泡靠近突触前膜,v-SNARE(synaptobrevin/突触小泡蛋白)与 t-SNARE(syntaxin 和 SNAP-25)开始组装 2. 启动 I(Priming I):SNARE 束部分组装 3. 启动 II(Priming II):Complexin(复合蛋白) 结合到 SNARE 束上,"锁住" 融合机器——囊泡处于"待发射"状态 4. 融合孔开放(Fusion pore opening):Ca²⁺ 流入 → 结合到 synaptotagmin(突触结合蛋白) 上 → synaptotagmin 与磷脂和 SNARE 蛋白相互作用 → 解除 complexin 的锁定 → 膜融合发生 5. 融合完成(Fusion complete):神经递质释放到突触间隙
关键蛋白:
| 蛋白 | 位置 | 功能 |
|---|---|---|
| Synaptobrevin | 囊泡膜(v-SNARE) | 与 t-SNARE 配对 |
| Syntaxin | 突触前膜(t-SNARE) | 与 v-SNARE 配对 |
| SNAP-25 | 突触前膜(t-SNARE) | 与上述两者组成四螺旋束 |
| Complexin | 细胞质 | 锁定 SNARE 束,防止自发融合 |
| Synaptotagmin | 囊泡膜 | Ca²⁺ 感受器,触发融合 |
5.4 胞吐后的膜平衡
胞吐(exocytosis)时,囊泡膜与质膜融合,增加了质膜面积。
三种需要快速增加质膜的场景:
1. 细胞分裂(卵裂沟形成) 2. 吞噬作用(巨噬细胞吞噬病菌时需要大量膜) 3. 伤口修复
膜的流量平衡:
| 前向流(Forward flow) | 逆向流(Retrograde flow) | 结果 |
|---|---|---|
| = 逆向流 | = 前向流 | 细胞大小不变 |
| > 逆向流 | < 前向流 | 细胞快速生长 |
| < 逆向流 | > 前向流 | 细胞缩小 |
---
第六部分:内吞和内体-溶酶体系统
6.1 两种主要的内吞方式
| 类型 | 特点 | 吞噬物大小 |
|---|---|---|
| 吞噬作用(Phagocytosis) | "细胞吃",主要是免疫细胞(巨噬细胞) | 大颗粒(细菌、细胞碎片等) |
| 胞饮作用(Pinocytosis) | "细胞喝",所有细胞都有 | 液体和溶质 |
Clathrin 介导的内吞(CME) 是最经典的胞饮机制。
6.2 Clathrin 的结构
Clathrin(网格蛋白)由 Barbara Pearse 于 1975 年命名(来自拉丁语 clathrates,意为"格子状的")。
结构层次:
1. 三脚架(Triskelion):由 3 条重链 + 3 条轻链组成的三条"腿"结构,是 clathrin 的基本单元 2. 笼状结构(Basket):多个三脚架进一步组装成由六边形和五边形组成的多面体笼子(类似足球的结构,通过五边形产生弯曲)
6.3 接头蛋白 (Adaptor Proteins, APs)
Clathrin 本身不直接结合货物,需要接头蛋白(AP)来连接。
AP 复合物是核心连接者,同时桥接三个组分:
1. 膜(通过结合特定的磷酸肌醇脂质) 2. 货物蛋白(识别货物的内吞信号) 3. Clathrin(招募 clathrin 三脚架)
AP 复合物家族(四亚基异四聚体):
| AP 复合物 | 定位 | 功能 |
|---|---|---|
| AP1 | TGN, 内体 | Clathrin 介导的运输 |
| AP2 | 质膜 | Clathrin 介导的内吞(最经典) |
| AP3 | TGN, 内体 | 溶酶体相关细胞器 |
| AP4 | TGN, 内体 | Clathrin 非依赖性运输 |
| GGA | TGN | 单体接头蛋白 |
6.4 AP2 的激活机制
AP2 有两种构象:
- 锁定态(Locked):AP2 呈紧凑构象,隐藏了货物结合位点和磷脂结合位点
- 开放态(Open):AP2 打开构象,暴露结合位点
激活需要双重信号:
1. PI(4,5)P₂(质膜上特有的磷酸肌醇)与 AP2 的 α 亚基结合 2. 货物蛋白的内吞信号与 AP2 的 μ2 亚基结合
两者协同作用使 AP2 从锁定态转变为开放态。这确保了 clathrin 包被囊泡主要在有货物的地方形成(虽然没有货物也可以形成空囊泡,但效率低很多)。
6.5 Clathrin 包被囊泡的组装与解聚
完整过程:
1. 外套组装和货物选择:AP2 结合 PI(4,5)P₂ 和货物 → 招募 clathrin 三脚架 2. 芽体形成:clathrin 笼子逐渐组装,膜弯曲 3. 囊泡形成:需要膜弯曲蛋白和剪切蛋白(dynamin) 4. 去被膜(Uncoating):囊泡从膜上剪切后,PI(5)P 磷酸酶水解 PI(4,5)P₂ → 失去了 AP2 与膜的结合力 → 外套蛋白脱落 → 形成裸露的运输囊泡
6.6 磷酸肌醇 (PIPs) 是膜身份的标签
核心概念:不同的细胞器膜含有不同种类的磷酸肌醇(PIPs),这些 PIPs 就像"邮编"一样标记了每个细胞器。
| 磷酸肌醇 | 主要分布 |
|---|---|
| PI(4,5)P₂ | 质膜 |
| PI(3)P | 早期内体 |
| PI(4)P | Golgi |
| PI(3,5)P₂ | 晚期内体 |
| PI(3,4,5)P₃ | 质膜(受信号调控) |
PIPs 通过招募含有特定PI 结合结构域(如 PH domain, FYVE domain, PX domain)的蛋白质,来实现膜身份识别和信号传导。
6.7 Dynamin——囊泡剪切的"剪刀"
发现:来自果蝇 Shibire 突变体("颤抖"突变体)的研究。这种突变体在高温下瘫痪,因为突触囊泡无法从质膜上剪切下来。电镜下可以看到,囊泡通过长长的"脖子"连在质膜上,无法释放。
Dynamin 的作用机制:
1. Dynamin 含有 PI(4,5)P₂ 结合域,被招募到囊泡颈部 2. Dynamin 还与 Amphiphysin(含 BAR 结构域的蛋白)结合——BAR 结构域像"香蕉形的夹子"一样感知和诱导膜弯曲 3. 多个 Dynamin 分子在囊泡颈部组装成螺旋环 4. Dynamin 的 GTPase 结构域水解 GTP → 构象改变 → 收缩 → 将囊泡颈部拧断
6.8 受体介导的 LDL 内吞——经典案例
LDL(低密度脂蛋白) 是血液中运输胆固醇的"快递包裹"(~22 nm 的颗粒,外面是磷脂和载脂蛋白,里面装满胆固醇和胆固醇酯)。
LDL 内吞的完整过程:
1. LDL 颗粒结合质膜上的 LDL 受体 2. LDL 受体-LDL 复合物被集中到 clathrin 包被的坑(coated pit) 中 3. 坑内陷形成 clathrin 包被囊泡 → dynamin 剪切 → 囊泡释放 4. 囊泡去被膜 → 与早期内体(early endosome)融合 5. 在内体的酸性环境(pH ~6)中,LDL 与 LDL 受体分离 6. LDL 受体被回收到质膜,重复使用 7. LDL 颗粒继续前往晚期内体和溶酶体 8. 在溶酶体中,LDL 被水解酶降解,释放出游离胆固醇供细胞使用
临床意义:LDL 受体基因突变导致家族性高胆固醇血症——LDL 无法被有效清除,血液中 LDL 水平升高,动脉粥样硬化和心血管疾病风险大增。
6.9 其他内吞方式
除了 clathrin 介导的内吞,还有:
1. Caveolae 介导的胞饮:Caveolae(小凹)是质膜上富含胆固醇和鞘磷脂的小型内陷,由 caveolin 蛋白形成 2. FEME(Fast Endophilin-Mediated Endocytosis,快速内吞蛋白介导的内吞):由 endophilin(含 BAR 结构域)和 dynamin 驱动,不依赖 clathrin 3. 巨胞饮(Macropinocytosis):细胞膜形成大的褶皱(ruffle),包裹大量细胞外液体,形成大的巨胞饮体(macropinosome)。由肌动蛋白(actin)重排驱动
6.10 内体-溶酶体系统
这是一个由多个动态互相转化的膜室组成的系统:
各组成部分:
| 膜室 | 标志蛋白 | pH | 形态特征 | 功能 |
|---|---|---|---|---|
| 早期内体 (EE) | Rab5, PI(3)P | ~6.5 | 含管状和空泡状结构域 | 分选站(sorting endosome) |
| 回收内体 (RE) | Rab11 | ~6.8 | 管状结构 | 将膜蛋白回收到质膜 |
| 多泡体/晚期内体 (MVB/LE) | Rab7 | ~5.5 | 含大量腔内囊泡 (ILVs) | 蛋白质降解的准备 |
| 内体溶酶体 (endolysosome) | — | — | 部分电子致密 | LE 与溶酶体融合的中间体 |
| 溶酶体 (LY) | LAMP 蛋白 | ~4.5-5.0 | 电子致密腔 | 最终降解站 |
6.11 早期内体 (EE) 是分选站
早期内体接收来自质膜的内吞货物后,可以有三种去向:
1. 回收(Recycling):受体被送回质膜重新使用(如 LDL 受体、转铁蛋白受体)→ 通过回收内体 2. 逆行运输:某些蛋白质被送回 TGN(如 M6P 受体)→ 通过 retromer 3. 降解(Degradation):信号分子/受体被送入 MVB/溶酶体降解 → 下调信号
6.12 晚期内体 (LE) / 多泡体 (MVB)
MVB 的形成:早期内体膜向内出芽(invagination),形成腔内囊泡(ILVs)。这样,原本在限制膜(外膜)上的膜蛋白就被包裹进了 ILV 内部。
为什么要形成 ILV? 为了真正降解膜蛋白!如果膜蛋白还在限制膜上,溶酶体的酶无法完全降解它。把它包进 ILV 后,整个 ILV(连同上面的蛋白)都在溶酶体腔内,可以被完全水解。
6.13 信号受体的下调——泛素化和 ESCRT
当一个信号受体(如 EGFR)需要被下调时:
1. 受体被泛素化(ubiquitination)标记 2. 泛素化的受体被内吞到早期内体 3. ESCRT 复合物识别泛素化的受体,将其分选到 ILV 中
ESCRT(Endosomal Sorting Complex Required for Transport):
| 复合物 | 功能 |
|---|---|
| ESCRT-0 | 识别泛素化的货物 + 结合 PI(3)P(内体的标志脂质) |
| ESCRT-I | 与 ESCRT-0 结合,招募 ESCRT-II |
| ESCRT-II | 启动膜弯曲 |
| ESCRT-III | 驱动膜剪切,完成 ILV 形成 |
注意:ILV 的形成是向腔内出芽,这与普通的囊泡出芽(向细胞质出芽)方向相反——这是一种"反向拓扑学"的膜出芽,不需要外套蛋白。
6.14 内体成熟:Rab 蛋白的"身份转换"
关键问题:早期内体(Rab5+)如何变成晚期内体(Rab7+)?
Rab 转换(Rab conversion)机制:
1. 早期内体膜上有 Rab5-GTP → 招募 Rab5 的效应蛋白(包括 PI3-kinase 产生 PI(3)P、系留因子等) 2. Rab5 的效应蛋白之一是 Rab7 的 GEF(RabB-GEF)→ 激活 Rab7 3. 同时,Rab7 的效应蛋白包含 Rab5 的 GAP(RabA-GAP)→ 失活 Rab5 4. 结果:Rab5 被换成 Rab7 → 膜的身份改变 → 早期内体变成晚期内体
核心概念:这是一个正反馈+负反馈的切换系统。RabA(Rab5)招募了 RabB(Rab7)的激活因子,而 RabB 又招募了 RabA 的抑制因子。这确保了切换是快速且彻底的——不会出现"半早期半晚期"的混合状态。
6.15 Rab5 膜结构域的形成
Rab5 域的建立是一个正反馈环路:
1. Rab5-GEF 将 Rab5 激活(GDP → GTP)→ Rab5-GTP 插入内体膜 2. Rab5-GTP 招募 PI3-激酶 → 在膜上生成 PI(3)P 3. PI(3)P 招募更多含 PI(3)P 结合域的蛋白(包括更多的 Rab5-GEF 和系留因子) 4. 更多 Rab5-GEF → 更多 Rab5 被激活 → 正反馈放大
域的大小由 GTP 水解速率控制——GAP 的活性设定了域的边界。
6.16 回收内体 (RE) 和葡萄糖转运体的调控运输
回收内体(RE)(Rab11 阳性)的功能:将内吞的质膜蛋白和脂质回收到细胞表面重新使用。
经典案例:胰岛素调控的葡萄糖摄取
| 状态 | GLUT4(葡萄糖转运体4)的位置 | 葡萄糖摄取 |
|---|---|---|
| 无胰岛素刺激 | 储存在专门的回收内体中 | 低 |
| 胰岛素刺激 | 信号触发 → RE 与质膜融合 → GLUT4 大量出现在细胞表面 | 高 |
这就是为什么胰岛素抵抗(GLUT4 无法被有效转运到质膜)会导致血糖升高的分子机制。
6.17 极性细胞中的定向分泌
极性细胞(如上皮细胞和神经细胞)面临一个额外挑战:蛋白质不仅要到达正确的细胞器,还要到达细胞的正确一面。
上皮细胞:
1. 直接分选:在 TGN 中就分别装入去往顶端或基底外侧的不同囊泡 2. 间接分选:先全部送到基底外侧面,再通过内吞-回收,将部分蛋白质转运到顶端面
- 有顶端面(apical domain)和基底外侧面(basolateral domain),由紧密连接(tight junction)分隔
- 两种分选方式:
神经细胞:
- 从树突和胞体接收信号
- 通过轴突和突触末端传出信号
- 不同的蛋白质需要被靶向到不同的区域
6.18 转胞吞 (Transcytosis)
转胞吞是一种特殊的运输方式:囊泡从细胞的一面内吞,穿过细胞,从另一面胞吐。
经典案例:新生儿肠道中 IgG 抗体的转运
1. 母乳中的 IgG 抗体在肠道的顶端面(apical, 面向肠腔)被 Fc 受体识别并内吞 2. IgG-Fc 受体复合物经过早期内体 → 回收内体 3. 从基底外侧面(basolateral)胞吐,释放到体液中 4. 这样,母亲的抗体就被传递给了婴儿,提供被动免疫保护
---
核心概念对照表
| 中文术语 | 英文术语 | 功能简述 |
|---|---|---|
| 囊泡 | Vesicle | 膜包裹的小泡,运输货物 |
| 外套蛋白 | Coat protein | 驱动囊泡形成,选择货物 |
| 顺行运输 | Anterograde transport | ER → Golgi → 质膜方向 |
| 逆行运输 | Retrograde transport | Golgi → ER 方向 |
| 系留 | Tethering | 远距离捕获囊泡 |
| 对接 | Docking | 囊泡与靶膜近距离接触 |
| 融合 | Fusion | 囊泡膜与靶膜合二为一 |
| 剪切 | Fission | 囊泡从供体膜上切下 |
| 去被膜 | Uncoating | 外套蛋白从囊泡上脱落 |
| 分选信号 | Sorting signal | 决定蛋白去向的短序列/结构 |
| 质量控制 | Quality control | ER中确保只有正确折叠的蛋白可以离开 |
| 多泡体 | Multivesicular body (MVB) | 含有腔内囊泡的晚期内体 |
| 腔内囊泡 | Intraluminal vesicle (ILV) | MVB 内部的小囊泡 |
| 转胞吞 | Transcytosis | 从细胞一面到另一面的运输 |
---
关键分子速查表
| 分子 | 类型 | 功能 |
|---|---|---|
| Sar1 | 小 GTPase | 控制 COPII 外套组装 |
| ARF | 小 GTPase | 控制 COPI 和 clathrin 外套组装 |
| Rab (1-11+) | 小 GTPase 家族 | 囊泡靶向、系留、膜室身份 |
| Sec12 | GEF | 激活 Sar1 |
| Sec23/24 | COPII 内层外套 | 货物识别 + Sar1 GAP |
| Sec13/31 | COPII 外层外套 | 形成笼状结构 |
| NSF | ATPase | 拆解 SNARE 复合物 |
| v-SNARE | 膜蛋白 | 囊泡上的融合机器 |
| t-SNARE | 膜蛋白 | 靶膜上的融合机器 |
| Clathrin | 外套蛋白 | 形成笼状结构(三脚架) |
| AP1-4, GGA | 接头蛋白 | 桥接 clathrin、膜和货物 |
| Dynamin | GTPase | 囊泡颈部剪切 |
| KDEL 受体 | 膜蛋白受体 | 识别并回收 ER 驻留蛋白 |
| MPR | 膜蛋白受体 | 识别 M6P 标签,运输溶酶体酶 |
| Retromer | 蛋白复合物 | 回收 MPR 到 TGN |
| ESCRT-0/I/II/III | 蛋白复合物 | 识别泛素化货物,形成 ILV |
| Synaptotagmin | Ca²⁺ 感受器 | 触发突触囊泡融合 |
| Complexin | 调节蛋白 | "锁定" SNARE 束 |