植物免疫全景
站在鸟瞰视角,先看清植物免疫的全貌
本章目录
- 植物面临的威胁图谱:细菌、真菌、卵菌、病毒、线虫
- 多层防御体系的基本架构
- 非宿主抵抗与宿主特异性抵抗
- 细胞自主免疫与组织水平协调
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
1961年,H. H. Flor 在亚麻锈病系统中提出"基因对基因假说"时,植物病理学还是一门以田间观察和遗传统计为主的学科。半个多世纪后的今天,我们已能在原子分辨率下观看免疫受体的构象跃迁,能在单细胞水平追踪防御信号的时空传播,能用 CRISPR 在几周内改写一个抗性位点。然而,一个根本问题始终悬而未决:植物免疫的"默认状态"究竟是什么?它是时刻保持高度戒备的哨兵系统,还是一台平时沉默、只在感知危险时才被唤醒的应答机器?
这个问题之所以重要,是因为它决定了我们理解整个防御体系的基本框架。如果默认状态是戒备,那么疾病的发生就意味着防线被突破;如果默认状态是沉默,那么有效防御的前提就是信号能被正确识别和传递。正如我们将在第2章看到的,PTI 与 ETI 这两个经典概念的关系——究竟是泾渭分明的两层还是协同耦合的整体——在很大程度上取决于我们对这一默认状态的假设 → 第2章。
本章的任务是提供一个鸟瞰视角。我们将从植物面对的威胁多样性出发,理解为什么进化出多层防御是必要的;然后审视这些防御层次的基本架构;接着讨论一个常被忽视却极为重要的现象——非宿主抵抗;最后探讨植物如何在没有循环免疫细胞的条件下实现组织水平的协调防御。这些问题的答案将为后续各章奠定概念基础。
1.1植物面临的威胁图谱:细菌、真菌、卵菌、病毒、线虫
要理解防御系统的设计逻辑,首先要理解威胁的多样性。植物在自然界中面对的病原体涵盖了几乎所有微生物类群,每一类都演化出了独特的入侵策略,而植物的应对方式也因此各有侧重。
细菌:从气孔到质外体的博弈
植物病原细菌大多为革兰氏阴性菌,以Pseudomonas syringae为代表。它们通常通过气孔或伤口进入叶片质外体空间,依赖 III 型分泌系统(T3SS)向宿主细胞内注射效应蛋白(effector),抑制免疫反应并重塑代谢环境以利于定殖 (Xin & He, 2013)。一个关键的进化洞察是:气孔不仅是气体交换的通道,也是免疫的第一道战场——拟南芥在感知细菌鞭毛蛋白 flg22 后,会在数分钟内触发气孔关闭,而P. syringae则通过冠菌素(coronatine)强制重开气孔 (Melotto et al., 2006)。这场"开-关博弈"是理解植物免疫动态对抗本质的一个缩影。
值得注意的是,同一属的细菌可以拥有截然不同的生活策略。Pseudomonas syringae是典型的半活体营养型(hemibiotrophic),先维持宿主细胞存活以获取营养,后期才导致组织坏死;而Erwinia amylovora(火疫病菌)则表现出更强的坏死营养倾向。这种策略差异直接影响植物选择何种防御路径——水杨酸(SA)通路更有效抵抗活体营养型病原,茉莉酸(JA)通路则偏向对抗坏死营养型和昆虫 → 第5章。
真菌:最古老也最多样的对手
真菌是造成农业损失最大的一类病原。根据营养策略,植物病原真菌可分为三大类:活体营养型(如锈菌Puccinia、白粉菌Blumeria)、坏死营养型(如灰霉菌Botrytis cinerea)和半活体营养型(如稻瘟菌Magnaporthe oryzae)(Dean et al., 2012)。
活体营养型真菌的入侵策略令人叹为观止。以大麦白粉菌Blumeria graminis f. sp. hordei为例:分生孢子着陆于叶表后,先形成附着胞(appressorium),产生巨大的穿透压力突破角质层和细胞壁,随后在活细胞内形成吸器(haustorium)——一种被宿主膜包裹的特化营养器官 (Hückelhoven, 2007)。吸器不仅是营养摄取界面,也是效应蛋白分泌的主要位点。植物细胞在吸器周围形成"质外体区室"(extrahaustorial matrix),这一微环境成为宿主与病原分子交锋的核心战场。
相比之下,坏死营养型真菌如B. cinerea采取"先杀后吃"的策略,分泌大量细胞壁降解酶、毒素和活性氧,主动杀死宿主细胞后从死亡组织中获取营养 (van Kan, 2006)。这意味着,植物对活体营养型和坏死营养型病原的防御逻辑截然不同——对前者有效的超敏反应(HR)式细胞死亡,反而可能助长后者的侵染。这一矛盾是植物免疫研究中反复出现的主题。
图 1.1 五类主要病原的入侵策略与生活方式比较。细菌主要通过气孔或伤口进入质外体并用 T3SS 注射效应子;真菌和卵菌形成附着胞或吸器界面;病毒依赖媒介或伤口进入细胞并与 RNA 沉默系统对抗;线虫通过口针重编程根细胞形成营养位点。
卵菌:趋同进化的典范
卵菌(Oomycetes)在形态上与真菌高度相似——都能形成菌丝和孢子——但在进化上却属于 SAR 超群(Stramenopiles),与硅藻和褐藻的亲缘关系更近 (Thines & Kamoun, 2010)。这是一个教科书级的趋同进化案例:面对相同的生态位(植物组织),卵菌独立演化出了与真菌相似的入侵工具包,包括附着胞、吸器和效应蛋白,但其分子机制有着根本差异。
以致病疫霉Phytophthora infestans为例——就是引发1845年爱尔兰大饥荒的马铃薯晚疫病病原——其基因组编码超过500个RXLR效应蛋白和约200个 CRN 效应蛋白 (Haas et al., 2009)。这个数字远超大多数细菌效应蛋白库(P. syringae通常携带20-30个效应子),暗示卵菌与宿主之间存在更为激烈的进化军备竞赛。RXLR 效应蛋白因其保守的 N 端 RXLR 基序得名,该基序介导蛋白质从吸器进入宿主细胞质的过程,尽管其具体转运机制至今仍有争议 (Whisson et al., 2007)。
病毒:劫持细胞的极简主义者
植物病毒是最极端的寄生者:它们没有自己的代谢机器,完全依赖宿主的翻译和复制系统。大多数植物 RNA 病毒的基因组仅编码4-10个蛋白质,却能系统性地重编程整个宿主细胞 (Garcia & Pallas, 2015)。与细菌和真菌不同,病毒不能主动穿透完整的植物细胞壁,而是依赖媒介昆虫(如蚜虫、飞虱、粉虱)的刺吸式口器或机械伤口进入细胞。一旦进入细胞质,病毒 RNA 直接利用核糖体进行翻译,随后通过胞间连丝(plasmodesmata)在细胞间移动,最终经维管束实现全株系统性侵染。
植物对病毒的防御有其独特之处。RNA 沉默(RNA silencing)是对抗 RNA 病毒最核心的防御机制:宿主 Dicer-like(DCL)蛋白将双链 RNA 复制中间体切割为21-24 nt的小干扰 RNA(siRNA),装载入 Argonaute(AGO)蛋白后靶向降解病毒 RNA (Ding & Voinnet, 2007)。作为回应,几乎所有植物病毒都编码至少一种 RNA 沉默抑制子(VSR),这是病毒侵染成功的关键因子 → 第7章。
线虫:地下的隐秘入侵者
植物寄生线虫每年造成全球超过1500亿美元的农业损失,却长期未获得与其重要性相称的研究关注 (Jones et al., 2013)。根结线虫(Meloidogyne spp.)和胞囊线虫(Heterodera / Globodera spp.)是两类最具经济重要性的类群。它们的入侵策略令人印象深刻:二龄幼虫通过口针穿刺根细胞壁,注入分泌自食道腺体的效应蛋白,诱导宿主根细胞发生戏剧性重编程——根结线虫诱导形成巨细胞(giant cell),胞囊线虫则诱导合胞体(syncytium)。这些特化营养位点通过持续的细胞周期和代谢重编程维持,是线虫完成生活史的必需结构 (Mitchum et al., 2013)。
有趣的是,线虫效应蛋白的功能与细菌和卵菌效应蛋白存在惊人的功能趋同:许多都靶向植物免疫信号通路的关键节点,如激素信号、细胞壁完整性监测和转录调控网络 (Hewezi & Baum, 2013)。这种跨界的趋同提示我们,植物免疫系统的核心弱点(或者说核心节点)在亿万年的进化中是相对保守的。
将五类病原并置观察,一个重要的模式浮现出来:无论入侵策略如何不同,所有成功的病原都必须解决三个基本问题——突破物理屏障、逃避或抑制免疫识别、重塑宿主代谢以获取营养。这种功能趋同意味着植物的防御体系也必须在多个层次上设置关卡,而不能依赖单一机制。这正是下一节要讨论的多层防御架构的进化理据。
1.2多层防御体系的基本架构
面对如此多样的威胁,植物进化出了一套多层、多模式的防御体系。这套体系的基本逻辑可以类比为中世纪城堡的防御设计:城墙(物理屏障)→护城河(化学防御)→哨兵(免疫识别)→烽火台(信号转导)→守军出动(效应输出)。但这个类比很快就会暴露其局限——与城堡不同,植物的防御是高度动态的,各层次之间存在密集的反馈和交叉调节。
第一层:预成性物理与化学屏障
植物的第一道防线是结构性的。角质层(cuticle)覆盖于叶片和茎干表面,由角质(cutin)和蜡质(wax)组成,构成一层疏水性屏障,能有效阻止大多数病原的直接穿透 (Yeats & Rose, 2013)。细胞壁则是第二道结构屏障:由纤维素、半纤维素、果胶和结构蛋白组成的复杂网络,不仅提供机械强度,其降解产物还可作为"损伤相关分子模式"(DAMPs)触发免疫反应 → 第3章。
除物理屏障外,植物还储备了大量预成性化学防御物质。例如,十字花科植物的硫代葡萄糖苷(glucosinolate)体系:完整的硫代葡萄糖苷本身无毒,但当组织受损时,与之空间隔离的黑芥子酶(myrosinase)被释放,迅速将前体水解为具有毒性的异硫氰酸酯(isothiocyanate),对病原和昆虫都具有强烈的抑制作用 (Halkier & Gershenzon, 2006)。这种"化学地雷"式的设计——储存无害前体,损伤时瞬间激活——是植物预成性化学防御的一个精妙范例。
第二层:模式触发免疫(PTI)
当病原突破物理屏障后,植物的主动免疫系统开始介入。第一个被激活的层次是模式触发免疫(Pattern-Triggered Immunity, PTI),也称为 PAMP/MAMP 触发免疫。其核心逻辑是"非我识别":位于细胞膜表面的模式识别受体(PRR)识别病原或微生物保守的分子模式(PAMP/MAMP),如细菌鞭毛蛋白的保守片段 flg22、延伸因子 EF-Tu 的 elf18 片段、真菌几丁质寡糖等 (Zipfel, 2014)。
PRR 主要包括两大类:受体激酶(Receptor-Like Kinase, RLK)和受体蛋白(Receptor-Like Protein, RLP)。以研究最为深入的 FLS2-flg22 系统为例:FLS2 识别 flg22 后,在数秒内与共受体 BAK1(BRI1-Associated Kinase 1)形成异源二聚体,随后启动胞内激酶级联 (Chinchilla et al., 2007)。PTI 的典型输出包括:质外体活性氧爆发(ROS burst,在数分钟内发生)、细胞质 Ca²⁺ 浓度升高、MAP 激酶级联激活、气孔关闭、胼胝质(callose)沉积以及防御基因的大规模转录重编程 (Boller & Felix, 2009)。
一个值得强调的概念是:PTI 并非只是简单的"开关"反应。近年来的研究表明,PRR 信号的强度和持续时间受到精密的正负反馈调控——包括受体内吞与降解、磷酸化/去磷酸化的动态平衡、以及多种负调控蛋白的抑制作用 (Couto & Zipfel, 2016)。这种调控的精密性提示我们,PTI 更像一个可调节的"变阻器"而非简单的"开关"。
图 1.2 PTI 信号传导的基本架构与时间序列。PTI 从秒级的 PRR 识别和共受体复合体组装开始,经由 Ca²⁺、ROS 与 MAPK 等分钟级信号模块放大,最终在小时级触发防御基因表达、细胞壁强化和抗菌代谢物积累。
第三层:效应子触发免疫(ETI)
为了克服 PTI,成功的病原进化出了效应蛋白(effector),通过分泌系统直接注入或释放到宿主细胞内,靶向 PTI 信号通路的关键节点进行抑制。作为反制,植物进化出了第二层免疫识别——效应子触发免疫(Effector-Triggered Immunity, ETI):细胞内的 NLR(Nucleotide-binding Leucine-rich Repeat)受体通过直接或间接方式识别效应蛋白的存在或活动,触发强烈且通常伴随超敏反应(HR)的免疫应答 (Jones & Dangl, 2006)。
经典的"Zigzag 模型"将 PTI 与 ETI 描述为一场持续升级的分子军备竞赛:植物通过 PRR 建立基础免疫(PTI)→ 病原用效应子抑制 PTI(ETS, Effector-Triggered Susceptibility)→ 植物用 NLR 识别效应子重建免疫(ETI)→ 病原进化新效应子逃避 NLR 识别 → 植物进化新 NLR……如此循环往复 (Jones & Dangl, 2006)。这一模型在概念上极具影响力,但正如我们将在第2章详细讨论的,近年来的证据表明 PTI 与 ETI 之间的关系远比"两个独立层次"复杂得多——它们共享大量信号组分,且 ETI 的完全激活实际上依赖于 PTI 通路的功能完整性 (Ngou et al., 2021; Yuan et al., 2021) → 第2章。
第四层:系统性获得抗性(SAR)与免疫启动(Priming)
局部免疫反应发生后,植物还能通过长距离信号将防御状态传递到未受感染的远端组织,建立全株范围的增强抗性——即系统性获得抗性(Systemic Acquired Resistance, SAR)。SAR 的建立依赖水杨酸信号通路和多种移动信号分子(包括甲基水杨酸、壬二酸、甘油醛-3-磷酸和pipecolic acid 衍生物等),其效应通过 NPR1 转录共激活因子和 WRKY 转录因子网络实现 (Fu & Dong, 2013) → 第5章。
与 SAR 紧密相关的是免疫启动(priming)现象:经历过初次刺激的植物在遭遇二次挑战时,能更快、更强地激活防御反应,而在没有挑战的情况下并不付出显著的代谢代价 (Mauch-Mani et al., 2017)。Priming 涉及表观遗传修饰(如组蛋白修饰)、信号蛋白的"待命"积累以及代谢物前体的预储备,某些情况下甚至可以跨代传递 → 第11章。这一机制的存在暗示,植物免疫并非简单的"刺激-反应"系统,而具有某种形式的"记忆"。
- 识别触发:PRR 感知保守分子模式(PTI)或 NLR 识别效应蛋白(ETI),将病原入侵信号转化为细胞内事件。关键时间窗口:秒至分钟级。
- 信号放大:MAPK 级联、Ca²⁺ 信号网络、ROS 爆发等核心中继模块将初始弱信号放大为可执行的强输出。关键时间窗口:分钟至小时级。
- 执行防御:转录重编程(数千基因的表达变化)、抗菌代谢物合成(植保素等)、细胞壁强化(胼胝质沉积)、以及可能的超敏细胞死亡协同启动。关键时间窗口:小时至天级。
- 反馈平衡:免疫系统在抗病收益与生长代价之间寻找新的平衡点。负调控机制关闭不再需要的防御反应,激素网络重新协调生长-防御资源分配 → 第9章。
图 1.3 植物多层防御体系的整体架构与信号流。物理屏障、PTI、ETI 与系统性免疫不是彼此孤立的层级,而是共同接入 Ca²⁺、ROS、MAPK、激素和转录网络等共享信号模块,再输出到细胞壁强化、抗菌代谢、HR 与远端 priming。
初学者容易将植物免疫理解为"PTI 挡不住就靠 ETI"的简单层级关系。但现实更像是一个高度互联的网络:PTI 和 ETI 共享下游信号模块(如 MAPK 级联和 ROS 产生),ETI 的完全表达依赖 PTI 组分的功能,而系统性信号和表观遗传记忆则为整个系统增加了时间维度。理解这种网络性质,是本书后续各章的基础。
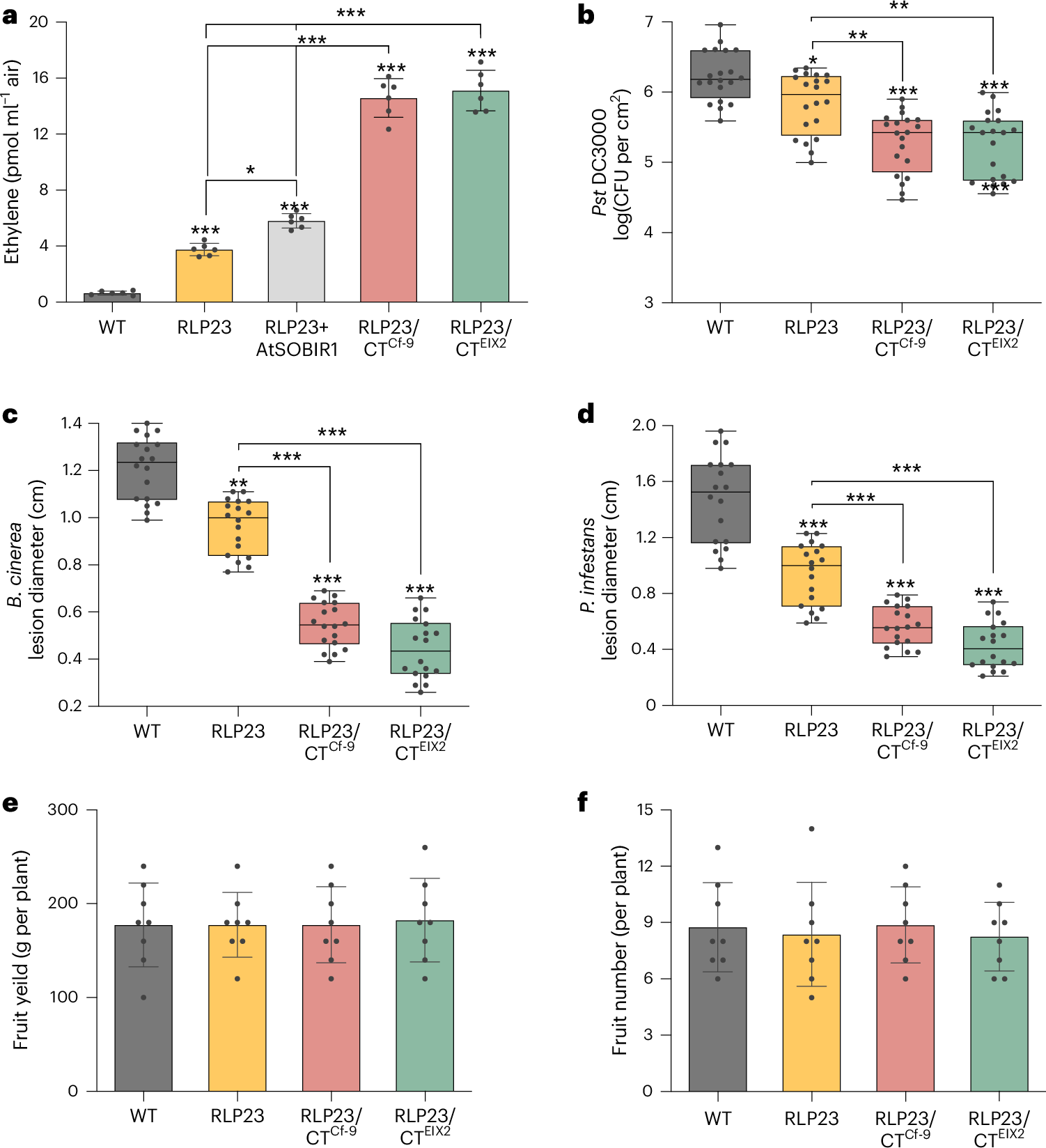
图 1.P1 论文原图:工程化 PRR 把植物免疫从解析推向部署。原图为 Yang et al. (2025) Nature Biotechnology Fig. 1,DOI: 10.1038/s41587-025-02858-8。该图展示细胞表面受体工程如何把 PRR 识别层转化为作物广谱抗性的设计入口,可作为本章“多层免疫系统如何走向应用”的最新 Nature 系列参照。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
1.3非宿主抵抗与宿主特异性抵抗
在讨论了植物免疫的多层架构后,我们需要面对一个更根本的问题:为什么绝大多数植物对绝大多数病原是免疫的?
这个问题看似显而易见,但其意义常被低估。自然界中已知的植物病原微生物物种以万计,而任何一种植物通常只被其中极少数物种成功侵染。换言之,抗病是常态,感病才是例外。这种广泛的基础抗性被称为非宿主抵抗(Non-Host Resistance, NHR),它可能是植物免疫中最重要、却研究最不充分的组成部分 (Mysore & Ryu, 2004; Lee et al., 2017)。
非宿主抵抗:沉默的多数
NHR 之所以研究困难,原因恰恰在于其高效性:因为非宿主植物不会发病,所以难以通过经典的遗传学方法(基于易感突变体的筛选)进行解析。直到分子遗传学工具的进步,研究者才逐步揭示了 NHR 的多层机制。
拟南芥对大麦白粉菌B. graminis f. sp. hordei的非宿主抵抗是研究最为深入的模型之一。通过正向遗传学筛选,Lipka 等人发现 PEN1(编码一个 syntaxin 蛋白)、PEN2(编码一个糖苷水解酶)和 PEN3(编码一个 ABC 转运体)的突变会部分削弱拟南芥对大麦白粉菌的 NHR,允许真菌形成初级菌丝 (Lipka et al., 2005; Stein et al., 2006)。但即使 pen 突变体允许了初始穿透,后续的防御层次(包括 SA 依赖性信号和 ETI 样反应)仍能限制真菌的进一步扩展。这一结果表明:NHR 不是由单一机制决定的,而是多层防御的叠加效应。
一个有启发性的概念框架将 NHR 视为一个连续谱(continuum)而非一个离散状态 (Schulze-Lefert & Panstruga, 2011)。在这个框架中:
- 类型 I NHR:不产生任何可见症状,由预成性屏障和基础 PTI 足以应对。这类抵抗可能涉及病原无法适应非宿主的化学环境或无法分泌有效的效应蛋白。
- 类型 II NHR:在微观水平可观察到细胞死亡反应,提示 ETI 样的识别机制参与。这类抵抗暗示非宿主植物的 NLR 恰好能识别该病原的某些效应蛋白。
这一分类框架的重要启示是:NHR 与宿主特异性抵抗之间可能不存在本质的机制差异,差异仅在于参与防御层次的数量和强度。
宿主特异性抵抗:基因对基因的经典与修正
当一个物种处于某个病原的宿主范围之内时,群体内个体间的抗性差异主要由宿主特异性抵抗决定。经典的解释框架是 Flor 的基因对基因假说(gene-for-gene hypothesis):植物的抗性基因(R 基因)产物特异性识别病原的无毒基因(Avr 基因)产物,识别成功则触发抗性反应 (Flor, 1971)。
这一假说在分子水平的验证经历了三个关键里程碑:
- 第一个 R 基因的克隆——1992年,Pto(番茄对P. syringae pv. tomato的抗性基因)和1994年的 RPS2(拟南芥)与 N(烟草)的克隆,证实了大多数 R 基因编码 NLR 蛋白 (Martin et al., 1993; Bent et al., 1994; Whitham et al., 1994)。
- "保卫假说"的提出——Van der Biezen 和 Jones (1998) 提出 NLR 可能并非直接识别 Avr 蛋白,而是监测(guard)效应蛋白的毒力靶标。这一假说被 Shao 等人 (2003) 在 RIN4 系统中优雅地验证:P. syringae 的效应蛋白 AvrRpm1 和 AvrRpt2 都靶向 RPM1-interacting protein 4(RIN4),而 NLR 蛋白 RPM1 和 RPS2 分别监测 RIN4 的磷酸化修饰和蛋白水解切割。
- "诱饵模型"的发展——进一步的概念扩展认为,一些被 NLR 监测的蛋白可能已经丧失了原始的信号功能,进化为专门的"诱饵"(decoy),其唯一功能就是充当效应蛋白活动的传感器 (van der Hoorn & Kamoun, 2008)。NLR 蛋白中"整合结构域"(integrated domain)的发现为这一概念提供了结构基础——某些 NLR 直接将效应蛋白靶标的结构域整合到自身蛋白中,作为诱饵检测效应蛋白的活性 (Cesari et al., 2014) → 第4章。
图 1.4 从基因对基因到保卫/诱饵模型的概念演进。早期模型强调 R 蛋白直接识别 Avr;保卫模型把识别对象转向效应蛋白对宿主靶标的修饰;诱饵和整合域模型进一步说明,植物可以把被攻击的靶标逻辑内置到 NLR 受体中。
NHR 与宿主特异性抵抗的边界在哪里?
一个日益受到关注的问题是:NHR 和宿主特异性抵抗之间是否存在清晰的界限?来自多个实验系统的证据表明,这一界限可能是模糊的。例如,水稻品种间对稻瘟菌不同小种的抗性差异,与水稻属对其他禾本科专化型稻瘟菌的 NHR,可能共享部分 NLR 家族成员 (Zhai et al., 2014)。这一认识具有重要的育种学意义:如果 NHR 的遗传基础可以被解析和转移,则有可能创造出比传统 R 基因更持久的广谱抗性 → 第14章。
传统教学往往把 NHR 一笔带过,直接进入"基因对基因"的讨论。但从进化视角看,NHR 才是植物免疫的"底色",宿主特异性抵抗只是这个背景上的"变奏"。理解这一点有助于重新思考抗病育种策略:与其不断追逐会被病原快速克服的单基因 R 基因抗性,能否模拟 NHR 的多层叠加效应来构建更持久的抗性?
1.4细胞自主免疫与组织水平协调
植物免疫研究中有一个常被忽视的基本约束:植物没有专职免疫细胞。动物拥有高度分化的免疫细胞群——巨噬细胞、T 细胞、B 细胞——通过血液循环快速到达感染部位。植物则不然:每一个细胞都必须是自己的"免疫战士"。这一约束深刻塑造了植物免疫系统的组织方式。
细胞自主免疫:每个细胞都是堡垒
植物的每个活细胞原则上都配备了完整的免疫感知和应答机器——表面 PRR、胞内 NLR、信号转导级联、防御基因表达系统。这种"细胞自主免疫"(cell-autonomous immunity)意味着,即使一个细胞的邻居已经被攻陷,该细胞仍有可能独立抵抗入侵 (Dodds & Rathjen, 2010)。
超敏反应(Hypersensitive Response, HR)是细胞自主免疫最戏剧性的表现。当 NLR 识别到效应蛋白后,感染位点的细胞经历快速的程序性死亡,形成一个坏死斑。对于活体营养型病原来说,这等于釜底抽薪——赖以生存的活细胞被主动摧毁 (Coll et al., 2011)。但 HR 的执行机制远比简单的"自杀"复杂。近年来的结构生物学突破揭示了其分子基础:激活的 NLR 寡聚化形成"抗病小体"(resistosome),直接在细胞膜上组装成孔道(pore),导致离子失衡和细胞死亡 (Wang et al., 2019a, 2019b) → 第4章。这一发现与动物固有免疫中的炎性小体(inflammasome)和 gasdermin 孔道形成了惊人的机制类比,提示两界免疫系统可能共享更古老的进化起源。
胞间连丝:防御信号的高速通道
尽管每个细胞都具有自主免疫能力,植物并不是由孤立的免疫单元堆砌而成。胞间连丝(plasmodesmata, PD)是贯穿植物细胞壁的纳米级通道,允许小分子、RNA 甚至蛋白质在相邻细胞间直接转运。在免疫响应中,PD 的调节具有双重角色:一方面,PD 是局部防御信号(如 ROS 和钙波)快速传播的通道;另一方面,病毒和某些真菌效应蛋白利用 PD 在细胞间扩散 (Lee, 2015)。
因此,植物免疫的一个关键动态就是 PD 通透性的调节:感染早期,PD 周围沉积胼胝质导致通道收缩,限制病原扩散("封锁策略");而 SA 信号需要通过 PD 和维管束传递到远端组织以建立 SAR("通讯需求")。这种封锁与通讯之间的张力,是植物组织水平免疫协调的核心矛盾之一。
系统性信号:无循环系统的长距离通讯
在没有血液循环系统的条件下,植物如何将局部感染信息传递到全株?这个问题的答案涉及多种长距离信号分子和传递机制:
- 水杨酸及其衍生物:甲基水杨酸(MeSA)作为 SAR 的移动信号之一,通过韧皮部从感染叶运输到远端叶片 (Park et al., 2007)。
- Pipecolic acid(Pip)及其衍生物 N-hydroxypipecolic acid(NHP):近年来被鉴定为 SAR 的关键移动信号,其合成依赖 ALD1 和 FMO1 (Hartmann et al., 2018; Chen et al., 2018)。NHP 的发现是近年 SAR 研究的重要突破,因为它能够在远端组织中同时激活 SA 依赖和 SA 非依赖的防御通路。
- 电信号和 ROS 波:伤害或病原侵染可以触发沿维管束快速传播(几厘米/分钟)的电位变化和 ROS 波,其速度远超代谢物的韧皮部运输 (Gilroy et al., 2014)。这种快速信号可能代表了植物"报警系统"的第一波,为后续化学信号的到来做准备。
- 挥发性有机化合物(VOCs):受侵染的植物释放挥发性信号(如甲基茉莉酸、绿叶挥发物),不仅能诱导自身远端组织的防御,还能"警告"邻近植株——尽管这种"植物间通讯"的生态学意义和分子机制仍存争议 (Heil & Karban, 2010)。
图 1.5 植物系统性免疫信号的传递途径与时间尺度。局部感染可通过 ROS/电信号形成快速报警,通过韧皮部运输 SA 衍生物、NHP、Pip、G3P 等化学信号建立 SAR,也可通过挥发物影响远端组织或邻近植株。
免疫的组织与器官特异性
一个越来越受到重视的维度是:免疫反应在不同组织和器官中表现出显著差异。根部和叶片的 PRR 表达谱、NLR 组成和激素信号网络配置各不相同 (Millet et al., 2010)。例如,根部更依赖于茉莉酸和乙烯通路,而叶片则更依赖水杨酸通路。这种差异反映了不同器官面对的主要威胁类型的不同:叶片主要应对空气传播的叶部病原和昆虫,根部则面对土壤微生物组的复杂互作 → 第15章。
更有意思的是发育阶段对免疫的影响。幼苗和成年植物对同一病原的抗性可能存在显著差异——即"年龄相关抗性"(Age-Related Resistance, ARR)(Kus et al., 2002)。这种现象提示免疫系统的配置不是固定的,而是与发育程序深度整合的。理解这种整合,是将实验室发现转化为田间应用的一个关键瓶颈 → 第14章。
没有循环免疫细胞并不意味着免疫是"分散无序"的。植物通过细胞自主免疫确保每个单元的独立防御能力,通过胞间连丝和维管束实现局部和长距离的信号协调,通过组织特异性配置优化防御资源分配,通过表观遗传记忆实现跨时间的防御优化。这套方案与动物免疫截然不同,但在效率上毫不逊色——事实上,植物在自然界中的成功远超大多数动物物种。
植物免疫的"默认状态"是什么?是全面戒备还是选择性激活?
这个问题的答案可能因组织、发育阶段和环境而异。来自转录组学的证据表明,即使在没有明显病原压力的条件下,植物也维持着相当水平的基础防御基因表达 (Tsuda & Somssich, 2015)。根际微生物组的存在持续地"训练"植物的免疫系统,类似于动物肠道菌群对免疫的调节作用 → 第10章。另一方面,免疫的过度激活会严重抑制生长——这正是"生长-防御权衡"(growth-defense trade-off)的核心 → 第9章。
一个更精准的表述可能是:植物的默认状态是"有准备的沉默"(prepared silence)——免疫系统处于低水平的监测状态,信号组分已经就位但尚未完全激活,能够在感知威胁后迅速切换到全面防御模式。这种策略在节省资源和快速响应之间取得平衡,而 priming 机制则允许植物根据过往经历微调这个"基线水平"。在后续章节中,我们将看到这一概念如何在不同的防御层次中具体体现。
1.5里程碑研究思路拆解
里程碑 1:Jones & Dangl (2006) — 植物免疫系统的 Zigzag 模型
面对的问题:2006年以前,植物抗病研究已经积累了大量关于 R 基因、Avr 基因、PAMP 识别和信号转导的碎片化知识,但缺乏一个统一的概念框架来解释这些发现之间的关系。基础抗性(basal resistance)和基因对基因抗性(gene-for-gene resistance)被视为两个相对独立的领域。
关键思路:Jones 和 Dangl 提出"Zigzag 模型",将植物免疫概括为四个阶段的动态对抗过程:PTI → ETS → ETI → 效应子进化。这一框架的核心创新在于:(1)将 PAMP 识别和效应子识别放入同一个连续的进化叙事中;(2)引入"幅度"(amplitude)的概念,用免疫反应强度的涨落来统一解释不同层次的防御;(3)明确提出效应子的双重角色——既是病原的毒力工具,又是免疫系统的识别靶标。
关键证据链:该论文是综述性质,其说服力来自对已有实验证据的系统整合:PRR 发现(FLS2 等)→ 效应子功能鉴定(T3SS 分泌组)→ NLR 结构与功能 → 保卫假说的实验验证。
影响与局限:Zigzag 模型成为植物免疫领域被引用最多的框架(>10,000 次引用),几乎所有后续研究都以此为参照展开。但该模型也遗留了一个关键假设——PTI 和 ETI 是独立运作的两层——这一假设在2021年被 Ngou 等人和 Yuan 等人的工作正式挑战 → 第2章。
里程碑 2:Flor (1971) — 基因对基因假说的奠基
面对的问题:20世纪上半叶,育种家观察到作物抗性与病原致病力之间存在高度特异性的对应关系,但缺乏遗传学解释。
关键思路:Flor 利用亚麻(Linum usitatissimum)和亚麻锈菌(Melampsora lini)的互作体系,通过大量杂交实验证明:宿主的抗性和病原的无毒性各由单基因控制,只有当宿主携带特定 R 基因且病原携带对应 Avr 基因时,才表现抗性。任何一方缺失,则表现感病。
关键证据链:(1)F2 群体中 R 基因的孟德尔分离比;(2)病原无毒性的遗传分析显示 Avr 基因也符合简单遗传;(3)R-Avr 配对的特异性:改变 R 或 Avr 基因型中的任一个都可改变互作结果。
影响:基因对基因假说为后续半个世纪的 R 基因克隆和功能研究奠定了概念基础。其"受体-配体"式的思维模式直接启发了后来的保卫假说和诱饵模型。但需要注意的是,Flor 的模型隐含着"R 蛋白直接识别 Avr 蛋白"的假设,这在很多系统中并不成立——间接识别可能是更为普遍的机制。
里程碑 3:Ngou et al. (2021) & Yuan et al. (2021) — PTI-ETI 协同模型
面对的问题:Zigzag 模型将 PTI 和 ETI 描绘为相互独立的两个免疫层次。但零散的证据暗示两者之间存在更深层的联系——例如,ETI 反应中许多标志性输出(ROS 爆发、MAPK 激活)与 PTI 的输出高度重叠。
关键思路:两个独立研究组几乎同时发表了关键实验:通过构建 PTI 信号组分缺失的遗传背景,测试 ETI 的激活是否受到影响。
关键证据链:(1)Ngou 等在拟南芥中发现,ETI 的完全表达(包括 ROS 爆发和胼胝质沉积)需要 PTI 共受体 BAK1/SERK4 的参与;(2)Yuan 等证明,在 PRR 信号完全缺失的突变体背景下,NLR 介导的 ETI 反应大幅减弱;(3)两组数据一致表明 ETI 通过上调 PRR 和共受体的表达来增强 PTI,形成正反馈环路。
影响:这两篇论文(分别发表于Nature和Science)从根本上修正了 Zigzag 模型中"PTI 与 ETI 独立运作"的假设,建立了"PTI-ETI 协同增效"的新范式。但争论并未结束:协同效应的定量程度在不同病理系统中是否一致?在自然群体中,这种协同是规则还是例外?这些问题仍待解答 → 第2章。
1.6当前争论与未解问题
- 广谱抗性与代价的解耦是否可能?传统观点认为,增强抗性必然伴随生长代价(growth-defense trade-off)。但最近的证据表明,某些特定的遗传改造(如修改 NLR 的自抑制结构域或优化激素信号的时空调控)可能在不显著影响产量的情况下提升抗性 (Ning et al., 2017; Deng et al., 2017)。这究竟是例外还是规律?抗性-产量的 Pareto 前沿在哪里?
- 免疫阈值的编码机制是什么?不同组织、不同发育阶段、不同环境条件下,植物免疫激活的阈值显著不同。这种阈值差异是如何在分子水平被编码的?是受体表达水平的差异,信号转导级联的配置不同,还是表观遗传状态的预设?
- 实验室到田间的"可翻译性"鸿沟如何弥合?大量在模式植物中发现的免疫机制在作物系统和田间条件下尚未得到验证。分子层面的 readout(如 ROS 爆发强度、防御基因表达量)与田间抗性表现之间的关系远不清楚 (Morris et al., 2019)。建立"分子标记→田间表型"的可靠映射是将基础研究转化为育种工具的关键瓶颈。
- 免疫 priming 能否被工程化?Priming 机制为植物提供了一种低代价的增强防御方式。如果 priming 的分子基础(如特定的表观遗传标记或信号蛋白积累)能被精确操控,理论上可以创造出"出厂即已预启动"的作物品种 → 第11章。但 priming 状态的稳定性、跨代传递的可靠性以及在不同环境下的表现,都还是未知数。
- PTI-ETI 协同是规则还是例外?Ngou 和 Yuan 的2021年工作在拟南芥中建立了 PTI-ETI 协同模型,但在其他物种和病理系统中,这种协同的普遍性如何?协同的定量程度是否依赖于具体的 PRR-NLR 组合?
1.7关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| PAMP 诱导的 ROS 爆发检测 | 用 flg22/chitin 等 PAMP 处理叶片/叶圆片,通过化学发光法(luminol + HRP)实时监测质外体 ROS 产生。是评估 PTI 强度的标准化方法之一。 | 注意叶龄一致性、处理浓度(flg22 通常 100 nM–1 μM)、时间窗口(通常5-60 min)。不同基因型间基础 ROS 水平可能不同。 | Boller & Felix, 2009, Annu Rev Plant Biol |
| 细菌生长曲线分析 | 将已知浓度的病原细菌(如Pst DC3000)喷洒或注射接种于叶片,在不同时间点取样匀浆、梯度稀释平板计数。是评估植物抗性的"金标准"。 | 接种浓度(通常 10⁵–10⁶ CFU/mL 用于注射)、取样时间(0, 2, 3 dpi 常用)、统计学重复(≥3 生物学重复)。喷洒法更接近自然感染但变异更大。 | Katagiri et al., 2002, Plant J |
| MAPK 磷酸化 Western blot | 用抗磷酸化 MAPK 抗体(如 anti-pERK)检测 flg22 处理后 MPK3/MPK6/MPK4 的激活动态。用于评估 PAMP 信号转导通路的完整性。 | 处理后5-30 min 取样;需要合适的阳性对照(野生型 + flg22)和阴性对照(fls2 突变体或 mock 处理)。 | Asai et al., 2002, Nature |
| 遗传互补/等位测试 | 将候选基因导入突变体背景验证功能。是建立基因-表型因果关系的核心方法。包括转基因互补、等位突变体比较和基因编辑验证。 | 注意启动子选择(天然启动子 vs 35S 过表达的差异)、T1 代 vs 纯合系的区别、位置效应。CRISPR 编辑的多等位验证更为可靠。 | Jones & Dangl, 2006, Nature |
| 转录组分析(RNA-seq) | 对病原处理和对照组织进行全转录组测序,鉴定差异表达基因。可结合时间序列设计揭示免疫响应动态。 | 实验设计需注意时间点选择、生物学重复(≥3)、批次效应控制。结合加权基因共表达网络分析(WGCNA)可鉴定免疫相关基因模块。 | Cui et al., 2015, Annu Rev Plant Biol |
1.8推荐阅读
🔴 必读
🟡 重要
🟢 拓展
1.9参考文献
- Asai T, Tena G, Plotnikova J, et al. MAP kinase signalling cascade in Arabidopsis innate immunity. Nature, 2002, 415: 977–983.
- Bent AF, Kunkel BN, Dahlbeck D, et al. RPS2 of Arabidopsis thaliana: a leucine-rich repeat class of plant disease resistance genes. Science, 1994, 265: 1856–1860.
- Boller T, Felix G. A renaissance of elicitors: perception of microbe-associated molecular patterns and danger signals by pattern-recognition receptors. Annu Rev Plant Biol, 2009, 60: 379–406.
- Cesari S, Bernoux M, Moncuquet P, et al. A novel conserved mechanism for plant NLR protein pairs: the "integrated decoy" hypothesis. Front Plant Sci, 2014, 5: 606.
- Chen YC, Holmes EC, Rajniak J, et al. N-hydroxy-pipecolic acid is a mobile metabolite that induces systemic disease resistance in Arabidopsis. Proc Natl Acad Sci USA, 2018, 115: E4920–E4929.
- Chinchilla D, Zipfel C, Robatzek S, et al. A flagellin-induced complex of the receptor FLS2 and BAK1 initiates plant defence. Nature, 2007, 448: 497–500.
- Coll NS, Epple P, Dangl JL. Programmed cell death in the plant immune system. Cell Death Differ, 2011, 18: 1247–1256.
- Couto D, Zipfel C. Regulation of pattern recognition receptor signalling in plants. Nat Rev Immunol, 2016, 16: 537–552.
- Cui H, Tsuda K, Parker JE. Effector-triggered immunity: from pathogen perception to robust defense. Annu Rev Plant Biol, 2015, 66: 487–511.
- Dean R, Van Kan JAL, Pretorius ZA, et al. The top 10 fungal pathogens in molecular plant pathology. Mol Plant Pathol, 2012, 13: 414–430.
- Deng Y, Zhai K, Xie Z, et al. Epigenetic regulation of antagonistic receptors confers rice blast resistance with yield balance. Science, 2017, 355: 962–965.
- Ding SW, Voinnet O. Antiviral immunity directed by small RNAs. Cell, 2007, 130: 209–222.
- Dodds PN, Rathjen JP. Plant immunity: towards an integrated view of plant–pathogen interactions. Nat Rev Genet, 2010, 11: 539–548.
- Flor HH. Current status of the gene-for-gene concept. Annu Rev Phytopathol, 1971, 9: 275–296.
- Fu ZQ, Dong X. Systemic acquired resistance: turning local infection into global defense. Annu Rev Plant Biol, 2013, 64: 839–863.
- Garcia JA, Pallas V. Viral factors involved in plant pathogenesis. Curr Opin Virol, 2015, 11: 21–30.
- Gilroy S, Suzuki N, Miller G, et al. A tidal wave of signals: calcium and ROS at the forefront of rapid systemic signaling. Trends Plant Sci, 2014, 19: 623–630.
- Haas BJ, Kamoun S, Zody MC, et al. Genome sequence and analysis of the Irish potato famine pathogen Phytophthora infestans. Nature, 2009, 461: 393–398.
- Halkier BA, Gershenzon J. Biology and biochemistry of glucosinolates. Annu Rev Plant Biol, 2006, 57: 303–333.
- Hartmann M, Zeier T, Bernsdorff F, et al. Flavin monooxygenase-generated N-hydroxypipecolic acid is a critical element of plant systemic immunity. Cell, 2018, 173: 456–469.
- Heil M, Karban R. Explaining evolution of plant communication by airborne signals. Trends Ecol Evol, 2010, 25: 137–144.
- Hewezi T, Baum TJ. Manipulation of plant cells by cyst and root-knot nematode effectors. Mol Plant-Microbe Interact, 2013, 26: 9–16.
- Hückelhoven R. Cell wall–associated mechanisms of disease resistance and susceptibility. Annu Rev Phytopathol, 2007, 45: 101–127.
- Jones JDG, Dangl JL. The plant immune system. Nature, 2006, 444: 323–329.
- Jones JT, Haegeman A, Danchin EGJ, et al. Top 10 plant-parasitic nematodes in molecular plant pathology. Mol Plant Pathol, 2013, 14: 946–961.
- Katagiri F, Thilmony R, He SY. The Arabidopsis thaliana–Pseudomonas syringae interaction. The Arabidopsis Book, 2002, 1: e0039.
- Kus JV, Zaton K, Sarber R, Cameron RK. Age-related resistance in Arabidopsis is a basal defense response mediated by SA. Plant Physiol, 2002, 128: 1052–1059.
- Lee JY. Plasmodesmata: a signaling hub at the cellular boundary. Curr Opin Plant Biol, 2015, 27: 133–140.
- Lee S, Whitaker VM, Hutton SF. Mini review: potential applications of non-host resistance for crop improvement. Front Plant Sci, 2017, 7: 2067.
- Lipka V, Dittgen J, Bednarek P, et al. Pre- and postinvasion defenses both contribute to nonhost resistance in Arabidopsis. Science, 2005, 310: 1180–1183.
- Martin GB, Brommonschenkel SH, Chunwongse J, et al. Map-based cloning of a protein kinase gene conferring disease resistance in tomato. Science, 1993, 262: 1432–1436.
- Mauch-Mani B, Baccelli I, Luna E, Flors V. Defense priming: an adaptive part of induced resistance. Annu Rev Plant Biol, 2017, 68: 485–512.
- Melotto M, Underwood W, Koczan J, et al. Plant stomata function in innate immunity against bacterial invasion. Cell, 2006, 126: 969–980.
- Millet YA, Danna CH, Clay NK, et al. Innate immune responses activated in Arabidopsis roots by microbe-associated molecular patterns. Plant Cell, 2010, 22: 973–990.
- Mitchum MG, Hussey RS, Baum TJ, et al. Nematode effector proteins: an emerging paradigm of parasitism. New Phytol, 2013, 199: 879–894.
- Morris CE, Monteil CL, Berge O. The life history of Pseudomonas syringae: linking agriculture to earth system processes. Annu Rev Phytopathol, 2019, 51: 85–104.
- Mysore KS, Ryu CM. Nonhost resistance: how much do we know? Trends Plant Sci, 2004, 9: 97–104.
- Ngou BPM, Ahn HK, Ding P, Jones JDG. Mutual potentiation of plant immunity by cell-surface and intracellular receptors. Nature, 2021, 592: 110–115.
- Ning Y, Liu W, Wang GL. Balancing immunity and yield in crop plants. Trends Plant Sci, 2017, 22: 1069–1079.
- Park SW, Kaimoyo E, Kumar D, et al. Methyl salicylate is a critical mobile signal for plant systemic acquired resistance. Science, 2007, 318: 113–116.
- Schulze-Lefert P, Panstruga R. A molecular evolutionary concept connecting nonhost resistance, pathogen host range, and pathogen speciation. Trends Plant Sci, 2011, 16: 117–125.
- Shao F, Golstein C, Ade J, et al. Cleavage of Arabidopsis PBS1 by a bacterial type III effector. Science, 2003, 301: 1230–1233.
- Stein M, Dittgen J, Sánchez-Rodríguez C, et al. Arabidopsis PEN3/PDR8, an ATP binding cassette transporter, contributes to nonhost resistance to inappropriate pathogens. Plant Cell, 2006, 18: 731–746.
- Thines M, Kamoun S. Oomycete–plant coevolution: recent advances and future prospects. Curr Opin Plant Biol, 2010, 13: 427–433.
- Tsuda K, Somssich IE. Transcriptional networks in plant immunity. New Phytol, 2015, 206: 932–947.
- van der Biezen EA, Jones JDG. Plant disease-resistance proteins and the gene-for-gene concept. Trends Biochem Sci, 1998, 23: 454–456.
- van der Hoorn RAL, Kamoun S. From guard to decoy: a new model for perception of plant pathogen effectors. Plant Cell, 2008, 20: 2009–2017.
- van Kan JAL. Licensed to kill: the lifestyle of a necrotrophic plant pathogen. Trends Plant Sci, 2006, 11: 247–253.
- Wang J, Hu M, Wang J, et al. Reconstitution and structure of a plant NLR resistosome conferring immunity. Science, 2019a, 364: eaav5870.
- Wang J, Wang J, Hu M, et al. Ligand-triggered allosteric ADP release primes a plant NLR complex. Science, 2019b, 364: eaav5868.
- Whisson SC, Boevink PC, Moleleki L, et al. A translocation signal for delivery of oomycete effector proteins into host plant cells. Nature, 2007, 450: 115–118.
- Whitham S, Dinesh-Kumar SP, Choi D, et al. The product of the tobacco mosaic virus resistance gene N: similarity to toll and the interleukin-1 receptor. Cell, 1994, 78: 1101–1115.
- Xin XF, He SY. Pseudomonas syringae pv. tomato DC3000: a model pathogen for probing disease susceptibility and hormone signaling in plants. Annu Rev Phytopathol, 2013, 51: 473–498.
- Yang Y, Steidele CE, Huang X, et al. Engineered pattern recognition receptors enhance broad-spectrum plant resistance. Nat Biotechnol, 2025. DOI: 10.1038/s41587-025-02858-8.
- Yeats TH, Rose JKC. The formation and function of plant cuticles. Plant Physiol, 2013, 163: 5–20.
- Yuan M, Jiang Z, Bi G, et al. Pattern-recognition receptors are required for NLR-mediated plant immunity. Nature, 2021, 592: 105–109.
- Zhai C, Lin F, Dong Z, et al. The isolation and characterization of Pik, a rice blast resistance gene which emerged after rice domestication. New Phytol, 2014, 201: 1352–1364.
- Zipfel C. Plant pattern-recognition receptors. Trends Immunol, 2014, 35: 345–351.