病原体宿主协同进化
攻防不是静态的,而是一场持续数百万年的进化博弈
本章目录
- "军备竞赛"的基因组学证据
- 从 boom-and-bust 到持久抗性的思考
- 宿主范围的决定因子
- 线虫与植物的协同进化特点
- 复合侵染场景下的协同进化
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
前面的章节分别讨论了植物的防御工具(PTI、ETI、激素网络)和病原的攻击工具(效应蛋白)。但这些工具不是凭空出现的——它们是植物与病原在数亿年共进化中相互塑造的产物。本章将视角从分子机制提升到进化动力学,探讨攻防博弈在时间维度上如何展开。
我们将看到,实验室中观察到的每一个 R-Avr 配对关系,都是一场漫长进化博弈的"快照";田间每一次 R 基因被"突破"的事件,都是这场博弈的最新一幕。理解这种动态,不仅是学术兴趣,更是设计持久抗病策略的前提——因为任何不考虑进化的抗性策略,都会被进化打败。
9.1"军备竞赛"的基因组学证据
第6章讨论了 NLR 进化和军备竞赛/堑壕战模型的概念框架 → 第6章。本节聚焦于基因组学层面的直接证据——共进化的"指纹"如何被刻写在基因组中。
效应蛋白与 NLR 的协同进化印记
共进化在基因组中留下了可辨识的分子印记:
- NLR 的 LRR 域正选择:全基因组扫描显示,NLR 蛋白的 LRR 域(决定识别特异性)具有显著高于基因组平均的 dN/dS 比值(>1),表明该区域处于持续的正选择压力之下——即有利于产生新变异的进化力量 (Mondragón-Palomino et al., 2002) → 第6章 6.1节。
- 效应蛋白基因的"两速"基因组:Phytophthora infestans 的基因组呈现惊人的"两速"(two-speed)结构——基因密集的保守区域和基因稀疏但转座子丰富的快速进化区域。效应蛋白基因(RXLR 和 CRN 家族)几乎全部位于快速进化区域,这使得效应蛋白的获取、丢失和多样化速率远高于其他基因 (Raffaele et al., 2010; Dong et al., 2015)。
- 稻瘟菌 AVR-Pik 与水稻 Pik 的对应进化:AVR-Pik 的多个等位变异(PikA-PikE)与 Pik 的多个等位(Pikp、Pikm、Pikh 等)之间存在精确的识别/逃逸对应关系——某些 AVR-Pik 变异能逃避特定 Pik 等位的识别但被其他等位识别。这种"棋盘式"的匹配/不匹配模式是分子军备竞赛的直接证据 (Kanzaki et al., 2012; De la Concepcion et al., 2021)。
图 9.1 分子军备竞赛的循环逻辑。植物 NLR 识别效应蛋白 → 病原效应蛋白突变逃逸 → 病原获取新效应蛋白恢复致病力 → 植物进化新 NLR 识别新效应蛋白。这一循环可以无限持续,直到一方的进化"弹药库"耗尽。
基因组级共进化的新证据
近年来,全基因组关联研究(GWAS)和泛基因组分析为共进化提供了群体水平的系统性证据。Karasov et al. (2014) 对拟南芥自然群体中免疫基因变异与本地病原群体毒力的关联分析显示:同一地理区域内的植物群体和病原群体之间存在局部适应(local adaptation)的信号——即各自"定制"的攻防配置。这种局部适应是共进化的生态学表现。
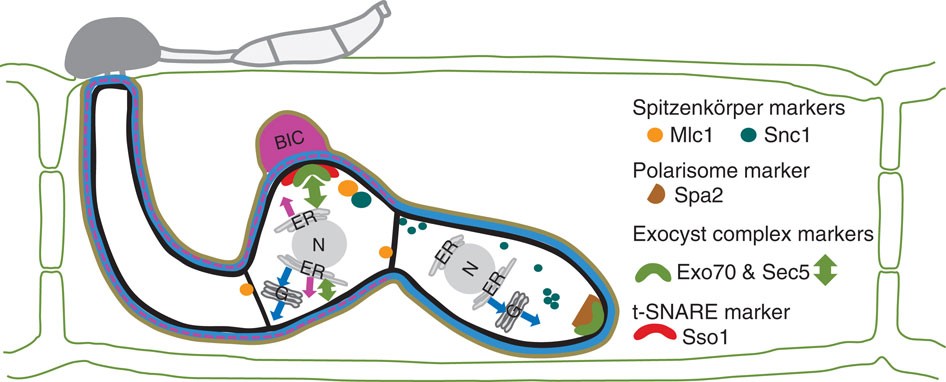
图 9.P1 论文原图:病原通过分泌系统分化扩大效应子进化空间。原图为 Giraldo et al. (2013) Nature Communications Fig. 8,DOI: 10.1038/ncomms2996。该模型图概括稻瘟菌把胞质效应子和质外体效应子分流递送的策略,适合作为本章“病原侧如何通过细胞生物学创新参与军备竞赛”的分子背景。依据 CC BY-NC-ND 3.0 原样复用;图片未作裁剪、改色或内容改动。
9.2从 Boom-and-Bust 到持久抗性的思考
共进化理论对农业实践最直接的冲击是:单基因 R 基因的大面积部署几乎必然会被突破。
Boom-and-Bust 循环
"繁荣-崩溃"(Boom-and-Bust)循环是农业中反复上演的故事:
- Boom(繁荣期):一个新的 R 基因品种被培育并大面积推广,对当前流行的病原小种表现出优异的抗性。
- 选择压力集中:数百万亩同一 R 基因的部署创造了巨大的定向选择压力——能够克服该 R 基因的病原突变体具有极大的适应度优势。
- Bust(崩溃期):在3-5年内(有时更快),能够逃避该 R 基因识别的病原新小种在群体中扩张,R 基因"失效",抗性品种变为感病品种。
- 新循环:育种家引入新的 R 基因品种,循环重新开始。
图 9.2 Boom-and-Bust 循环的典型时间线。单基因 R 基因部署后3-5年内通常被病原突破,需要引入新 R 基因替代,形成循环。绿色曲线代表田间有效抗性水平。
从单基因到持久抗性
如何打破 Boom-and-Bust 循环?主要策略包括:
- R 基因堆叠(gene stacking/pyramiding):将多个 R 基因同时导入一个品种。病原需要同时突变多个 Avr 基因才能克服所有 R 基因——概率随堆叠数量指数下降 (Zhu et al., 2023)。但堆叠也面临挑战:自身免疫风险(NLR 间不兼容性)、适应度代价积累、以及病原通过水平基因转移一次性获取多个新效应蛋白的可能 → 第6章 6.4节。
- 品种混播(cultivar mixture):在同一田块中混合种植携带不同 R 基因的品种。这在群体水平模拟了自然群体的遗传多样性,通过频率依赖效应减缓病原适应 (Zhu et al., 2000)。
- 定量抗性(quantitative resistance):由多个微效基因共同控制的抗性,每个基因单独效果小但叠加后显著。定量抗性因为没有单一的"突破靶标",通常比单基因抗性更持久 (Poland et al., 2009)。
- PRR 工程化:由于 PAMP 的高度保守性,PRR 介导的抗性在理论上比 NLR 抗性更持久——病原要逃避 PRR 识别就必须改变其核心保守分子 → 第14章。
9.3宿主范围的决定因子
为什么P. syringae的不同致病变种(pathovar)只能侵染特定的宿主?为什么M. oryzae的一些专化型只侵染水稻而另一些只侵染小麦?宿主范围——即一个病原能够成功侵染的宿主物种或品种范围——是共进化的直接产物。
宿主范围的分子基础
宿主范围的决定因子可以从两个方向理解:
- 从病原侧:一个病原的宿主范围取决于其效应蛋白组能否有效抑制目标宿主的免疫系统。如果目标宿主具有能识别该病原核心效应蛋白的 NLR(即非宿主抵抗 NHR),则该宿主不在其宿主范围内 → 第1章 1.3节。
- 从宿主侧:一个宿主对某个病原的易感性取决于其免疫网络是否有被该病原效应蛋白组有效抑制的"缺口"。如果宿主的 PRR 库、NLR 库和激素网络在面对该效应蛋白组时没有显著的未覆盖区域,则该病原难以建立感染。
Schulze-Lefert & Panstruga (2011) 提出了一个有影响力的连续谱模型:宿主范围不是一个二元属性(能/不能侵染),而是一个连续的量化指标,取决于"病原效应蛋白组的免疫抑制能力"与"宿主免疫网络的防御能力"之间的平衡。当效应蛋白组的抑制能力超过宿主免疫的防御阈值时,感染成功;反之则失败。这一模型的一个重要预测是:宿主范围的扩展可以通过获取少数关键的新效应蛋白(突破宿主的 NHR 瓶颈)实现——这已在多个实验系统中得到验证。
9.4线虫与植物的协同进化特点
植物寄生线虫与宿主的共进化有一些独特的特征,使其与微生物病原的共进化有所不同:
- 更长的世代时间:线虫的世代时间(数周到数月)远长于细菌(数小时),导致进化速率更慢。这可能是线虫效应蛋白的整体多样性低于细菌和卵菌的原因之一。
- 有性生殖的影响:胞囊线虫通常进行有性生殖,这加速了效应蛋白等位的重组和新组合的产生。但根结线虫的许多物种是孤雌生殖的,这限制了遗传多样性的产生但可能有利于通过基因复制快速扩展效应蛋白家族。
- 营养位点的依赖性:线虫对宿主巨细胞/合胞体的绝对依赖意味着,任何破坏营养位点维持的宿主突变都可能提供抗性——这创造了一个不同于微生物病原的选择压力格局 → 第7章 7.4节。
9.5复合侵染场景下的协同进化
自然环境中,植物通常同时面对多种病原——而非实验室中的"单一病原挑战"。这种复合侵染(co-infection / multiple infection)场景对共进化动力学有深刻影响。
竞争与促进:病原间的互作
共同侵染同一宿主的多种病原之间可能存在竞争或促进关系:
- 竞争:两种病原竞争相同的宿主资源(营养、空间),导致各自的增殖受到限制。
- 促进:一种病原通过抑制宿主免疫"铺平道路",使第二种病原更容易感染。例如,P. syringae 通过效应蛋白抑制 SA 通路后,对坏死营养型真菌B. cinerea的防御也被间接削弱——因为 SA-JA 拮抗被打破 → 第5章 5.3节。
微生物组背景下的共进化
更深层地说,植物面对的不是一个病原,而是一个包含数千物种的微生物群落。在微生物组背景下,共进化的单位可能不是"一种植物 vs 一种病原",而是"植物的免疫表型 vs 微生物群落的功能组成"。这一认识正在改变我们理解和管理植物健康的方式 → 第10章, 第15章。
能否通过监测病原群体的进化轨迹来预测 R 基因的"保质期"?
如果能实时监测田间病原群体中效应蛋白等位的频率变化(通过对病原群体的定期测序和效应蛋白组分析),理论上可以在 R 基因被大规模突破之前检测到"预警信号"——如能逃避识别的效应蛋白等位频率开始上升。这种"病原群体监测"策略类似于流感病毒的基因组监测,已在概念上被提出 (McDonald & Linde, 2002),但在农业场景中尚未系统实施。挑战包括:采样密度、基因型-表型映射的不完整性、以及病原群体进化的随机性。
9.6里程碑研究思路拆解
9.6里程碑研究思路拆解
里程碑 1:Burdon & Thrall (2009) — 自然群体中的植物-病原共进化
面对的问题:绝大多数植物免疫研究在实验室中进行。共进化理论在自然群体中是否成立?抗性和毒力频率的波动是否可以被直接观测到?
关键思路:在澳大利亚野生亚麻-亚麻锈菌自然群体中进行长期(>20年)纵向采样,追踪宿主 R 基因和病原 Avr 基因频率的时空变化。
关键证据链:(1)R 基因和 Avr 基因频率在不同群体间和不同年份间呈显著波动;(2)抗性和毒力的地理分布呈镶嵌式(mosaic)格局,支持局部适应;(3)频率动态与负频率依赖选择模型预测一致。
影响:首次在自然环境中提供了植物-病原共进化的长期群体遗传学证据,推动了病理学与进化生态学的深度融合。
里程碑 2:Raffaele et al. (2010) — 卵菌的"两速基因组"
面对的问题:Phytophthora 基因组异常庞大(~240 Mb),且效应蛋白基因数量惊人(>500 RXLR)。这种基因组结构是如何进化的?
关键思路:通过比较基因组学分析基因密度、转座子含量和进化速率在基因组不同区域的分布。
关键证据链:(1)基因组呈明显的"两速"分区:基因密集-进化缓慢区域 和 基因稀疏-转座子丰富-进化快速区域;(2)效应蛋白基因几乎全部位于快速进化区域;(3)快速区域的高重组率和转座子活性促进了效应蛋白的快速多样化。
影响:揭示了病原如何通过基因组架构"设计"加速效应蛋白进化,为理解病原侧的共进化机制提供了基因组学框架。"两速基因组"概念后来被推广到多种丝状病原中。
里程碑 3:Zhu et al. (2000) — 品种混播降低病害的田间证据
面对的问题:遗传多样性在理论上可以减缓病原适应,但在实际田间条件下效果如何?
关键思路:在中国云南省进行了大规模(3342公顷)田间试验:将感病的糯稻品种与抗病的杂交稻品种混合种植,与单一品种种植对照。
关键证据链:(1)混播处理中糯稻的稻瘟病发病率降低了94%;(2)混播使田间病原群体的小种组成更为多样化(减少了单一优势小种的定向选择);(3)到第二年,混播区域几乎不需要杀菌剂。
影响:首次在大田规模上证明品种多样性可以有效控制病害,为基于进化原理的抗病管理策略提供了实践验证。
9.7当前争论与未解问题
- 如何用分子参数预测 R 基因的田间"寿命"?给定一个 R 基因的分子机制(直接识别 vs 间接识别)和当前病原群体的效应蛋白组多样性,能否估计该 R 基因被突破的预期时间?
- 气候变化会如何改变共进化的速率和方向?温度升高可能加速病原世代周转、改变宿主范围、或影响免疫信号通路的效率 → 第12章。
- 多病原并存的"博弈论"最优策略是什么?当植物同时面对活体营养型和坏死营养型病原时,SA-JA 拮抗使其无法同时最优化两条防御通路。群体水平的最优策略是否是维持激素响应的多样性?
- 进化实验(experimental evolution)能否为共进化建模提供数据?在受控条件下长期培养植物-病原互作系统,追踪双方的基因型和表型变化,可以提供共进化动力学的"实时数据"——但技术挑战巨大。
9.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 纵向群体采样与基因分型 | 在自然群体或田间群体中进行多年连续采样,追踪 R 基因和 Avr 基因频率的时间变化。是验证共进化模型预测的核心方法。 | 采样间隔(每季或每年);群体样本量需足够检测频率变化(≥30个体/群体);需要高通量基因分型方法(扩增子测序或 SNP 阵列)。 | Burdon & Thrall, 2009, Science |
| 病原效应蛋白组(effectome)群体分析 | 对病原田间群体进行基因组测序,清点效应蛋白基因的存在/缺失变异和等位多态性。用于评估病原的"逃逸潜力"。 | 需要覆盖足够的地理和时间范围;效应蛋白的预测依赖已知基序(T3SS 信号、RXLR 等);需要区分假基因和功能基因。 | Yoshida et al., 2016, BMC Biol |
| 田间品种混播/轮作试验 | 在实际农田条件下测试品种多样性策略对病害控制的效果。包括混播(空间多样性)和轮作(时间多样性)。 | 需要大面积试验田(≥公顷级)以获得有统计意义的结果;需要多年数据排除年份效应;病害评估方法需标准化。 | Zhu et al., 2000, Nature |
| 实验进化(experimental evolution) | 在受控条件下长期繁殖植物-病原互作系统(通常数十到数百代),追踪双方基因型和表型的进化变化。 | 适用于短世代病原(细菌、真菌);需要严格的无菌转接和环境控制;基因组重测序追踪进化轨迹;注意"瓶颈效应"对遗传漂变的影响。 | Brockhurst & Koskella, 2013, Trends Ecol Evol |
9.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
9.10参考文献
- Brockhurst MA, Koskella B. Experimental coevolution of species interactions. Trends Ecol Evol, 2013, 28: 367–375.
- Burdon JJ, Thrall PH. Coevolution of plants and their pathogens in natural habitats. Science, 2009, 324: 755–756.
- De la Concepcion JC, Maidment JHR, Noman A, et al. The allelic rice immune receptor Pikh confers extended resistance to strains of the blast fungus through a single polymorphism in the effector binding interface. PLoS Pathog, 2021, 17: e1009368.
- Dong S, Raffaele S, Kamoun S. The two-speed genomes of filamentous pathogens: waltz with plants. Curr Opin Genet Dev, 2015, 35: 57–65.
- Giraldo MC, Dagdas YF, Gupta YK, et al. Two distinct secretion systems facilitate tissue invasion by the rice blast fungus Magnaporthe oryzae. Nat Commun, 2013, 4: 1996. DOI: 10.1038/ncomms2996.
- Kanzaki H, Yoshida K, Saitoh H, et al. Arms race co-evolution of Magnaporthe oryzae AVR-Pik and rice Pik genes driven by their physical interactions. Plant J, 2012, 72: 894–907.
- Karasov TL, Horton MW, Bergelson J. Genomic variability as a driver of plant-pathogen coevolution? Curr Opin Plant Biol, 2014, 18: 24–30.
- McDonald BA, Linde C. Pathogen population genetics, evolutionary potential, and durable resistance. Annu Rev Phytopathol, 2002, 40: 349–379.
- Mondragón-Palomino M, Meyers BC, Michelmore RW, Gaut BS. Patterns of positive selection in the complete NBS-LRR gene family of Arabidopsis thaliana. Genome Res, 2002, 12: 1305–1315.
- Mundt CC. Durable resistance: a key to sustainable management of pathogens and pests. Infect Genet Evol, 2014, 27: 446–455.
- Poland JA, Balint-Kurti PJ, Wisser RJ, et al. Shades of gray: the world of quantitative disease resistance. Trends Plant Sci, 2009, 14: 21–29.
- Raffaele S, Farrer RA, Cano LM, et al. Genome evolution following host jumps in the Irish potato famine pathogen lineage. Science, 2010, 330: 1540–1543.
- Raffaele S, Kamoun S. Genome evolution in filamentous plant pathogens: why bigger can be better. Nat Rev Microbiol, 2012, 10: 417–430.
- Schulze-Lefert P, Panstruga R. A molecular evolutionary concept connecting nonhost resistance, pathogen host range, and pathogen speciation. Trends Plant Sci, 2011, 16: 117–125.
- Yoshida K, Schuenemann VJ, Cano LM, et al. The rise and fall of the Phytophthora infestans lineage that triggered the Irish potato famine. eLife, 2013, 2: e00731.
- Zhu Y, Chen H, Fan J, et al. Genetic diversity and disease control in rice. Nature, 2000, 406: 718–722.