受体与信号转导
免疫从识别开始。植物用什么"眼睛"看见威胁,又如何将信息传入细胞内部?
本章目录
- PRR 的多样性与结构基础
- 早期信号事件的时空动态
- RLCK 枢纽与信号分流
- 转录重编程:从信号到基因表达
- 受体激酶超越免疫:FERONIA 的启示
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
免疫始于识别。无论后续的信号网络多么精密、防御输出多么强大,一切的前提是:植物必须首先"看见"入侵者。
植物用什么"看见"威胁?答案是一个庞大而多样的受体家族——模式识别受体(Pattern Recognition Receptor, PRR)。拟南芥基因组编码超过600个受体激酶(RLK)和约60个受体蛋白(RLP),其中至少数十个已被证实参与免疫识别 (Shiu & Bleecker, 2001)。但识别只是开始。从配体结合到防御基因激活,信号需要穿越细胞膜、胞质和细胞核三个空间区域,经历数秒到数小时的时间跨度——这中间涉及受体复合体组装、磷酸化级联、Ca²⁺ 振荡、ROS 爆发、MAPK 级联和转录因子激活等多个环节。
本章将从 PRR 的多样性和结构基础出发,追踪信号从膜到核的完整旅程。我们将特别关注三个关键节点:PRR-共受体复合体的动态组装、受体激酶型胞质激酶(RLCK)的信号分流枢纽功能,以及防御转录重编程的调控逻辑。最后,我们将通过 FERONIA 的故事,看到受体激酶如何超越经典免疫,在更广泛的植物-微生物互作中发挥作用。
3.1PRR 的多样性与结构基础
受体激酶(RLK)与受体蛋白(RLP):两大受体家族
植物表面免疫受体分为两大类:受体激酶(Receptor-Like Kinase, RLK)和受体蛋白(Receptor-Like Protein, RLP)。两者的胞外域都可以识别配体,关键差异在于胞内部分——RLK 自带激酶域,可以直接启动磷酸化级联;RLP 则缺乏胞内信号域,必须借助适配激酶(如 SOBIR1)才能传导信号 (Liebrand et al., 2014)。
2025 年的结构与工程研究进一步把 LRR-RP 的“识别逻辑”补齐。Snoeck et al. (2025) 通过 AI/结构分析表明,RLP23、RLP42 与 RLP32 等 LRR-RP 的 island domain 通过 β-sheet 稳定化完成配体结合和共受体招募;这意味着 LRR-RP 的工程化不仅要改配体口袋,还要保留 island domain 与 SOBIR1/BAK1 的几何耦合。
根据胞外域的类型,免疫相关 PRR 可分为几大类:
- LRR 型(Leucine-Rich Repeat):数量最多、研究最深入的一类。包括识别细菌鞭毛蛋白的 FLS2、识别延伸因子的 EFR、识别Xanthomonas Ax21 的 XA21 等。LRR 域形成弧形的螺线管结构,配体结合于其内凹面 (Sun et al., 2013)。
- LysM 型(Lysin Motif):识别含 N-乙酰葡萄糖胺骨架的碳水化合物配体,包括真菌几丁质(由 CERK1/LYK5 识别)和细菌肽聚糖。LysM 域直接结合糖链,且不同 LysM 受体之间存在复杂的共受体关系 (Cao et al., 2014)。
- Lectin 型:包括识别细菌脂多糖(LPS)和胞外 ATP 的受体。LORE(Lectin S-domain RLK)识别细菌的中链3-羟基脂肪酸代谢物 (Ranf et al., 2015);DORN1 识别损伤释放的胞外 ATP (Choi et al., 2014)——后者是一种 DAMP 受体,提示 PRR 的识别范围不局限于微生物分子。
- EGF-like / WAK 型:Wall-Associated Kinase(WAK)识别果胶片段——细胞壁降解产生的寡半乳糖醛酸(OGA)。这类 DAMP 识别将细胞壁完整性监测与免疫信号直接耦合 → 第6章。
图 3.1 主要 PRR 家族的结构类型与代表性成员。LRR-RLK 识别蛋白或肽类 PAMP,LysM-RLK 识别几丁质和肽聚糖等糖链,LRR-RLP 缺乏胞内激酶域而依赖 SOBIR1/BAK1,Lectin 与 WAK 类受体把脂类、eATP 和细胞壁损伤线索接入免疫网络。
共受体系统:BAK1/SERK 家族的核心角色
一个出乎意料但极为重要的发现是:大多数 LRR-RLK 型 PRR 并不独立工作,而是在配体结合后招募同一个或同一家族的共受体——BAK1/SERK(BRI1-Associated Kinase 1 / Somatic Embryogenesis Receptor Kinase)家族 (Chinchilla et al., 2007; Heese et al., 2007)。BAK1 最初被鉴定为油菜素内酯受体 BRI1 的共受体,后来发现它同时是 FLS2、EFR、PEPR1/2 等多种 PRR 的共受体。
这种"多受体共用一个共受体"的设计有什么进化意义?一种解释是信号汇聚效率:通过共享 BAK1,不同的 PRR 可以接入同一套下游信号模块,避免为每种识别事件各建一条专用通路。但这也带来了风险——病原只需靶向 BAK1 一个蛋白,就有可能同时瘫痪多条 PRR 通路。事实上,多种病原效应蛋白已被证明直接靶向 BAK1:P. syringae 的 AvrPto 和 AvrPtoB 均能抑制 BAK1 的激酶活性 (Shan et al., 2008; Cheng et al., 2011) → 第8章。
PRR 复合体的动态组装:从"开关"到"信号平台"
早期对 PRR 信号的理解是"开关模型"——配体结合,受体激活,信号输出。但过去十年的研究表明,PRR 复合体的实际行为远比"开关"复杂:
配体诱导的异源二聚化是 PRR 激活的核心事件。以 FLS2-flg22-BAK1 系统为例,flg22 结合于 FLS2 的 LRR 域后,创造出一个新的蛋白-蛋白界面,使 BAK1 的 LRR 域能够与之对接,形成三元复合体。这一过程在晶体结构层面已被精确解析 (Sun et al., 2013)。二聚化导致胞内激酶域的反式磷酸化(trans-phosphorylation),启动信号级联。
预组装复合体与纳米域组织也是近年来的研究热点。活细胞成像表明,FLS2 在未激活状态下并非随机分布于膜上,而是定位于特定的膜纳米域(nanodomain)。flg22 处理后,FLS2 从这些纳米域迁出,与 BAK1 形成复合体,随后经历网格蛋白介导的内吞(clathrin-mediated endocytosis)(Mbengue et al., 2016)。这一时空动态过程暗示:膜的组织结构本身就是信号调控的一个维度。
更进一步,PRR 复合体中还包含多种调控因子——如 BIR(BAK1-Interacting Receptor)蛋白在未激活状态下"占据" BAK1,防止其与 PRR 发生非特异性结合,从而设定了信号激活的阈值 (Halter et al., 2014)。这类负调控因子的存在,使得 PRR 信号系统更像一个可调节的"变阻器"而非简单的"开关" → 第1章 1.2节。
PRR 不是孤立的受体分子,而是一个动态组装的信号平台。平台的组成(哪些共受体参与)、组装效率(受纳米域组织和调控因子控制)和存续时间(受内吞和降解调控)共同决定了信号输出的强度和持续时间。理解这种平台动态,是理解 PTI 信号精密调控的基础。
3.2早期信号事件的时空动态
PRR 复合体激活后,信号需要在数秒到数分钟内传递到多个效应模块。这一阶段的信号事件可以按时间尺度分为三个层次:秒级的 Ca²⁺ 信号、分钟级的 ROS 爆发和 MAPK 级联激活。
Ca²⁺ 信号:免疫的"第一快递"
Ca²⁺ 浓度升高是 PRR 激活后最早的胞内事件之一。在 flg22 处理后2-5秒内,胞质 Ca²⁺ 浓度即开始上升,通常在1-2分钟内达到峰值 (Ranf et al., 2011)。Ca²⁺ 信号的来源包括质外体(通过膜上的 Ca²⁺ 通道内流)和胞内钙库(液泡和内质网释放)。
一个长期悬而未决的问题是:PTI 中的 Ca²⁺ 通道是什么?2019年,Tian 等人鉴定了 CNGC2/4(Cyclic Nucleotide-Gated Channel 2/4)异源四聚体作为 BIK1 下游的 Ca²⁺ 通道,由 BIK1 直接磷酸化激活 (Tian et al., 2019)。同年,Thor 等人发现 OSCA1.3(一种机械力敏感通道)也参与 PTI 的 Ca²⁺ 内流 (Thor et al., 2020)。这些发现表明,PTI 的 Ca²⁺ 信号不是由单一通道产生的,而是多种通道协同贡献——不同通道可能在时间和空间上形成特定的 Ca²⁺ 签名(Ca²⁺ signature)。
Ca²⁺ 签名的概念是理解 Ca²⁺ 信号特异性的关键:不同刺激可能产生不同的 Ca²⁺ 振荡模式(频率、幅度、持续时间),而下游 Ca²⁺ 解码器(如 CDPKs、CaM/CML)根据这些模式差异激活不同的效应通路 (DeFalco et al., 2010)。但植物中 Ca²⁺ 签名的生理意义——究竟是因果性的"编码"还是仅仅是伴随性的"相关"——仍有争议。
ROS 爆发:防御与信号的双重角色
PAMP 处理后,质外体中在数分钟内出现显著的活性氧爆发(主要是超氧阴离子 O₂⁻ 和 H₂O₂)。这一 ROS 爆发主要由 NADPH 氧化酶 RBOHD(Respiratory Burst Oxidase Homolog D)产生 (Torres et al., 2002)。
RBOHD 的激活机制已被精细解析:PRR 激活后,受体激酶型胞质激酶 BIK1 直接磷酸化 RBOHD 的 N 端调控域(Ser39、Ser339、Ser343 和 Ser347),解除自抑制并促进其酶活性 (Kadota et al., 2014; Li et al., 2014)。同时,Ca²⁺ 通过 EF-hand 基序结合到 RBOHD 的 N 端,进一步增强其活性——这创造了一个Ca²⁺-ROS 正反馈环路:Ca²⁺ 激活 RBOHD → RBOHD 产生的 ROS 激活邻近细胞的膜 Ca²⁺ 通道 → 新的 Ca²⁺ 入流又激活该细胞的 RBOHD (Dubiella et al., 2013)。这个正反馈环路是 ROS 波在组织间快速传播的分子基础 → 第1章 1.4节。
质外体 ROS 的功能是多重的:(1)直接杀伤微生物;(2)交联细胞壁蛋白,强化物理屏障;(3)作为信号分子,通过 RBOHD 介导的 ROS 波在细胞间和组织间传递防御信号;(4)调节气孔运动——H₂O₂ 在保卫细胞中激活 Ca²⁺ 通道,促进气孔关闭 (Qi et al., 2017)。
MAPK 级联:从信号到转录的桥梁
Mitogen-Activated Protein Kinase(MAPK)级联是将膜受体信号转化为转录输出的核心模块。植物中有两条主要的免疫 MAPK 级联:
- MEKK1–MKK4/5–MPK3/6 级联:这是 PTI 的主效应 MAPK 通路。flg22 处理后5-15分钟内,MPK3 和 MPK6 被强烈磷酸化激活。激活的 MPK3/6 进入细胞核,磷酸化 WRKY 转录因子(如 WRKY33),启动防御基因转录 (Asai et al., 2002; Mao et al., 2011)。
- MEKK1–MKK1/2–MPK4 级联:MPK4 在未激活状态下与 WRKY33 形成复合体,抑制 WRKY33 活性。PAMP 激活后,磷酸化的 MPK4 释放 WRKY33,使其能够激活下游靶基因(如植保素合成基因 PAD3)(Qiu et al., 2008)。有趣的是,MPK4 同时也是多种效应蛋白的靶标(如P. syringae的 HopAI1 直接灭活 MPK3/6),说明 MAPK 级联是免疫-反免疫的核心博弈战场 → 第8章。
图 3.2 PRR 激活后的早期信号分流。PRR-共受体复合体把配体识别转化为 RLCK 介导的信号拆分:一条支路推动 Ca²⁺ 内流与 ROS 爆发,另一条推动 MAPK 级联、内吞和转录重编程。该图强调的是“平台化分流”而非单线性传递。
Ca²⁺、ROS 和 MAPK 三条信号通路并非独立运作,而是通过多重交叉调控形成高度耦合的网络。例如:Ca²⁺ 依赖性蛋白激酶 CDPK 直接磷酸化 RBOHD,为 Ca²⁺-ROS 环路提供第二条激活路径 (Dubiella et al., 2013);MAPK 级联可以反馈调控 Ca²⁺ 通道活性;ROS 本身可以影响 MAPK 的氧化还原状态。这种高度耦合的网络结构可能赋予了信号系统更强的鲁棒性(robustness)——即使单一通路受到效应蛋白攻击,其他通路仍可部分维持输出。
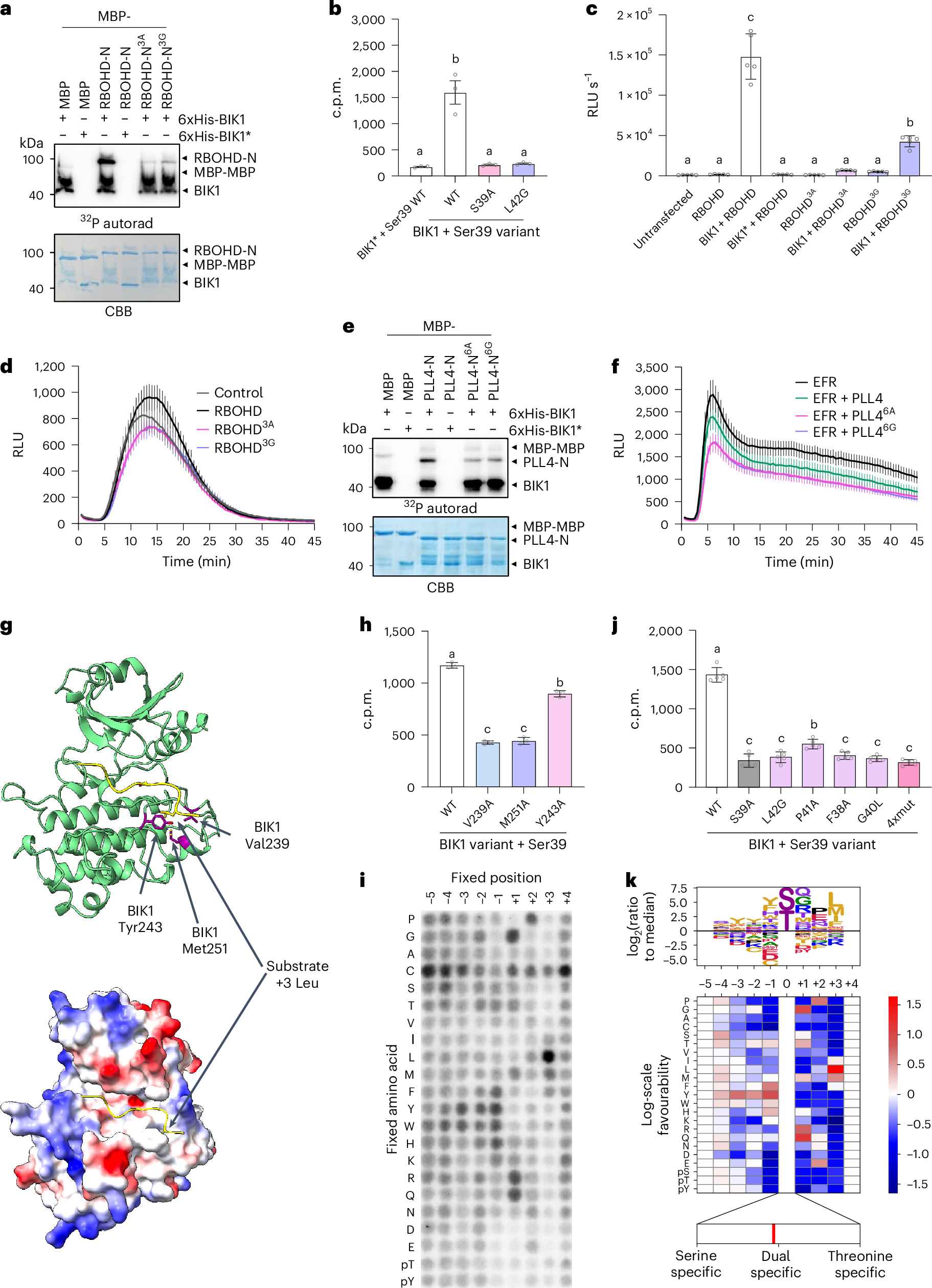
图 3.P1 论文原图:BIK1 底物图谱把早期免疫信号推向可测量网络。原图为 Toth et al. (2026) Nature Plants Fig. 1,DOI: 10.1038/s41477-025-02218-z。该图补充说明 PRR 相关 RLCK 不是单一线性中继,而是通过底物谱把 ROS、胞间连丝调控、NLR 寡聚化和转录输出等多层信号连接起来。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
3.3RLCK 枢纽与信号分流
在 PRR 和下游效应模块(ROS、Ca²⁺、MAPK)之间,存在一个关键的信号枢纽——受体激酶型胞质激酶(Receptor-Like Cytoplasmic Kinase, RLCK)。RLCK 是植物特有的一类激酶,缺乏胞外域和跨膜域,通过豆蔻酰化等脂修饰锚定在质膜内侧,与 PRR 复合体物理关联 (Lin et al., 2013)。
BIK1:最核心的免疫 RLCK
BIK1(Botrytis-Induced Kinase 1)是目前研究最为透彻的免疫 RLCK。在静息状态下,BIK1 与 FLS2 和 BAK1 均有物理互作。flg22 激活 FLS2-BAK1 复合体后,BAK1 磷酸化 BIK1,BIK1 随后从复合体解离,成为游离的活性激酶 (Lu et al., 2010; Zhang et al., 2010)。
解离后的 BIK1 同时执行多个任务,实现了信号的"分流":
- 磷酸化 RBOHD → ROS 爆发:BIK1 直接磷酸化 RBOHD 的 N 端 Ser 残基,是质外体 ROS 产生的关键步骤 (Kadota et al., 2014; Li et al., 2014)。
- 磷酸化 Ca²⁺ 通道 → Ca²⁺ 内流:BIK1 直接磷酸化 CNGC2/4 异源四聚体通道,触发 Ca²⁺ 从质外体进入胞质 (Tian et al., 2019)。
- 参与 MAPK 级联激活:虽然 BIK1 不直接磷酸化 MAPK 级联的最上层 MAPKKK,但通过磷酸化 MAPKKK 的调控因子(如 MEKK1 相关蛋白)间接促进级联激活。BIK1 同源蛋白 PBL(PBS1-Like Kinase)家族成员在这一层面有功能冗余 (Liang et al., 2018)。
- 调节气孔免疫:BIK1 在保卫细胞中磷酸化 SLAC1(S-type Anion Channel),促进阴离子外流和气孔关闭 (Liu et al., 2019)。
BIK1 的“一对多”信号分流设计使其成为 PTI 信号网络中的超级枢纽节点。这种设计的优势是效率高——单一激酶同时启动多条效应通路;但风险也很明显——BIK1 是效应蛋白攻击的首选靶标。P. syringae的效应蛋白 AvrAC 通过尿苷酰化修饰 BIK1(而非经典的磷酸化),直接灭活其激酶活性 (Feng et al., 2012)。拟南芥则通过 NLR 蛋白 ZAR1 监测 BIK1 同源物 PBL2 的修饰状态来"反制"这一攻击——当 AvrAC 修饰 PBL2 时,修饰后的 PBL2 触发 ZAR1 抗病小体的激活 → 第4章。
2026 年的底物图谱研究进一步把 BIK1 从“单一枢纽”改写为“可编程底物谱平台”。Toth et al. (2026) 通过高通量生化筛选与遗传验证,鉴定出一批此前未被重视的 BIK1 底物,包括参与胞间连丝关闭的 MCDTRP3、若干 CDKL 家族成员,以及多种 NLR 受体本身;这说明 BIK1 不只服务于 PTI 输出,还直接参与 ETI 的寡聚化门控。换言之,RLCK 层是 PTI 与 ETI 接合处的动态选择器,而不是固定的“下游执行器”。
RLCK 家族的功能冗余与分工
BIK1 属于 RLCK VII 亚家族,该亚家族还包括 PBL1-PBL40 等成员。不同 PBL 成员在不同 PRR 通路中的贡献权重不同:BIK1 和 PBL1 主要服务于 FLS2 和 EFR 通路;PBL27 参与几丁质受体 CERK1 通路的 MAPK 激活 (Shinya et al., 2014);PBL13 则以一种不寻常的方式参与——它磷酸化 RBOHD 的抑制性位点,充当负调控因子 (Lin et al., 2015)。
这种"同一家族中正负调控因子并存"的设计,使 RLCK 层成为精密调节信号输出的关键控制面板。理解这种调控逻辑,对于设计"低代价增强型"免疫改良策略至关重要 → 第14章。
3.4转录重编程:从信号到基因表达
PRR 激活后数小时内,植物基因组中数千个基因的表达发生剧变——这一"转录重编程"是免疫响应从信号事件转化为防御输出的关键步骤。在拟南芥中,flg22 处理1小时后约有1000-2000个基因显著上调或下调 (Zipfel et al., 2004)。
WRKY 转录因子:免疫转录网络的核心节点
WRKY 转录因子家族是植物免疫转录调控中研究最深入的家族。拟南芥编码74个 WRKY 成员,其中至少30个参与免疫调控 (Eulgem & Somssich, 2007)。WRKY 蛋白通过识别 W-box(TTGACC/T)基序结合靶基因启动子。
WRKY 网络的一个显著特征是广泛的自调控和互调控:WRKY33 激活 WRKY33 自身的转录(正反馈);WRKY18 与 WRKY40 形成异源二聚体,共同抑制一组防御基因(负调控);MAPK 磷酸化修饰不同 WRKY 蛋白的活性和稳定性。这种复杂的调控网络产生了"开关"和"计时器"两种行为模式——某些防御基因被快速、短暂地激活(脉冲式),另一些则被持续激活数天(阶梯式)(Birkenbihl et al., 2017)。
染色质层面的免疫调控
转录重编程不仅涉及转录因子的激活,还涉及染色质状态的改变。PAMP 处理后,防御基因位点的组蛋白修饰发生显著变化:H3K4me3(激活标记)和 H3K9ac(激活标记)在诱导基因上富集,而 H3K27me3(抑制标记)在某些防御基因上减少 (Jaskiewicz et al., 2011)。
更引人注目的是,这些表观遗传变化中有一些在刺激消除后可以持续存在——这为免疫"记忆"和 priming 提供了分子基础。例如,初次 PAMP 处理后,WRKY29 和 WRKY6 基因位点的 H3K4me3 和 H3K14ac 标记在刺激消除数天后仍保持升高水平,使这些基因在二次刺激时能更快被激活 (Jaskiewicz et al., 2011) → 第11章。
转录后调控:mRNA 稳定性与翻译控制
近年来越来越多的证据表明,免疫基因的表达不仅在转录水平被调控,mRNA 稳定性和翻译效率也是重要的调控层次。例如,RNA 结合蛋白 TZF(Tandem Zinc Finger)家族成员在 PAMP 处理后调控特定免疫 mRNA 的降解速率 (Maldonado-Bonilla, 2014)。翻译水平的调控则涉及上游开放阅读框(uORF)介导的翻译抑制——某些防御基因的 mRNA 在静息状态下已经存在但未被翻译,PAMP 信号通过改变翻译起始因子的活性迅速"释放"预存 mRNA 的翻译 (Xu et al., 2017)。这种"预制 mRNA + 信号触发翻译"的策略可能比"从头转录"更快,为最早期的防御响应提供了时间优势。
3.5受体激酶超越免疫:FERONIA 的启示
如果说前几节讨论的是"经典"免疫受体,那么 FERONIA(FER)的故事则展示了受体激酶世界的边界远比我们想象的模糊。
FER 最初被鉴定为花粉管-胚珠互作的调控因子(以罗马生育女神命名),后来被发现在植物发育、激素信号和胁迫响应中都有重要功能 (Escobar-Restrepo et al., 2007)。但真正让免疫研究者感到震惊的是一系列揭示 FER 在植物-微生物互作中功能的发现:
- FER 通过感知 RALF 肽调控免疫:FER 的配体是 RALF(Rapid Alkalinization Factor)肽——植物自身产生的内源性肽。RALF23 结合 FER 后,抑制 PRR 复合体的组装(通过干扰 FLS2-BAK1 的互作),负调控免疫 (Stegmann et al., 2017)。病原菌可能通过诱导 RALF 产生来"劫持"这一通路。
- FER 感知细胞壁完整性:FER 的胞外 malectin-like 域可以结合果胶——细胞壁的主要成分之一。这使 FER 能够监测细胞壁的完整性状态,将细胞壁损伤信号转化为胞内响应 (Feng et al., 2018)。
- FER 在根际微生物互作中的角色:FER 调控根毛的生长方向和根际微生物的定殖效率。fer 突变体的根际微生物组组成发生显著改变,提示 FER 可能是植物调节其微生物组的一个关键节点 → 第10章。
FER 的故事给我们的启示是深刻的:免疫受体和发育受体之间不存在清晰的边界。许多受体激酶"身兼数职",同时参与生长、发育和防御的调控。这种多功能性可能正是"生长-防御权衡"在分子水平的体现——当同一个受体既调控生长又调控免疫时,两者之间的竞争关系就在受体复合体层面被物理编码了 → 第9章。
PRR 信号网络的最优设计原则是什么——冗余优先还是效率优先?
PRR 信号系统展现了两种看似矛盾的设计原则:一方面,BIK1 等枢纽节点实现高效的"一对多"信号分流;另一方面,PBL 家族的广泛冗余确保单一节点的丧失不会导致系统崩溃。这两种原则如何在进化中被平衡?是否存在"最优"的枢纽数量和冗余度?从工程学角度看,PRR 网络的拓扑结构可能为设计鲁棒的人工信号系统提供启示。
一个值得注意的观察是:效应蛋白往往靶向枢纽节点(如 BIK1、BAK1),而植物的 NLR 监测系统也集中监控这些枢纽。这形成了一种"枢纽-攻击-保卫"的三方博弈,其进化稳定策略(ESS)可能决定了现有网络拓扑的形态 → 第8章。
3.6里程碑研究思路拆解
里程碑 1:Chinchilla et al. (2007) — FLS2-BAK1 共受体范式的建立
面对的问题:FLS2 如何将 flg22 的识别转化为胞内信号?单独的 FLS2 足够吗?
关键思路:通过免疫共沉淀(Co-IP)筛查 FLS2 激活后的互作蛋白,发现 BAK1 在 flg22 处理后数秒内即与 FLS2 形成复合体。结合遗传学验证(bak1 突变体的 PTI 缺陷),确立了"配体诱导的 PRR-共受体异源二聚化"模型。
关键证据链:(1)Co-IP 显示 flg22 依赖性的 FLS2-BAK1 互作;(2)bak1 突变体中 flg22 诱导的 ROS、胼胝质和防御基因表达均大幅减弱;(3)BAK1 也与 EFR 互作,提示共受体机制的普遍性。
影响:确立了 PRR-共受体模型作为植物表面免疫信号的基本范式。后续几乎所有 PRR 研究都遵循"寻找配体→鉴定受体→验证共受体→解析信号通路"的研究路线。
里程碑 2:Kadota et al. (2014) & Li et al. (2014) — BIK1-RBOHD 的直接连接
面对的问题:PRR 激活后的 ROS 爆发依赖 RBOHD,但 PRR 复合体如何激活 RBOHD?中间的信号连接是什么?
关键思路:两个独立实验室几乎同时发现 RLCK BIK1 是缺失的中间环节。通过体外激酶实验证明 BIK1 直接磷酸化 RBOHD 的 N 端特定 Ser 残基;通过磷酸化位点突变验证这些修饰对 ROS 产生的必要性。
关键证据链:(1)体外激酶实验:纯化的 BIK1 磷酸化 RBOHD-N 端;(2)质谱鉴定磷酸化位点(S39、S339、S343、S347);(3)磷酸化位点突变为 Ala 消除 ROS 爆发,突变为 Asp(磷酸化模拟)部分恢复;(4)bik1 突变体中 RBOHD 磷酸化水平降低。
影响:建立了 PRR→RLCK→RBOHD 的直接信号链条,是 PTI 信号转导中第一条被完整解析的"受体到效应器"通路。
里程碑 3:Tian et al. (2019) — BIK1 直接激活 Ca²⁺ 通道
面对的问题:PTI 的 Ca²⁺ 内流是最早的信号事件之一,但负责 Ca²⁺ 内流的通道蛋白身份一直不明。
关键思路:通过遗传筛选和蛋白互作分析,发现 CNGC2 和 CNGC4 形成异源四聚体通道,由 BIK1 直接磷酸化激活。利用电生理学(膜片钳)验证通道功能。
关键证据链:(1)cngc2/cngc4 双突变体的 flg22 诱导 Ca²⁺ 内流大幅减弱;(2)BIK1 体外磷酸化 CNGC4 的 C 端;(3)爪蟾卵母细胞异源表达系统中,CNGC2/4 + BIK1 共表达产生 Ca²⁺ 电流。
影响:解决了长达十余年的"PTI Ca²⁺ 通道身份"之谜,揭示了 BIK1 作为信号枢纽同时激活 ROS 和 Ca²⁺ 两条效应通路的机制。
3.7当前争论与未解问题
- 膜纳米域的功能意义有多大?PRR 在膜上的纳米域定位和动态迁移已被多项活细胞成像研究记录,但纳米域组织是否真正决定信号输出的速度和特异性,还是仅仅反映了膜蛋白的物理特性?目前缺乏直接操控纳米域组织的遗传工具来回答这一问题。
- Ca²⁺ 签名是因果性的还是相关性的?不同 PAMP 产生不同的 Ca²⁺ 振荡模式(签名),但这些差异是否真正编码了不同的信号信息?如果人工改变 Ca²⁺ 签名,能否改变下游输出?光遗传学工具(如 OptoSTIM1)可能为回答这一问题提供契机。
- PRR 信号的定量动力学能否预测抗病表型?早期信号事件(如 ROS 爆发峰值、MAPK 磷酸化强度)与最终的抗病表型(如细菌增殖量)之间的定量关系远不清楚。建立这种映射关系对于筛选和评估新的 PRR 改良策略至关重要。
- 效应蛋白为什么优先攻击信号终止机制?越来越多的证据显示,效应蛋白不仅抑制信号激活,还通过增强信号终止(如促进受体降解、增强去磷酸化酶活性)来抑制免疫。信号终止机制是否是 PTI 通路中最脆弱的环节?
- 能否通过受体工程低代价增强免疫?跨物种 PRR 转移(如将拟南芥 EFR 转入番茄/水稻)已被证明可以赋予新的 PAMP 识别能力 (Lacombe et al., 2010)。但转移受体后的信号接驳是否完整?是否会引发自身免疫?这些问题仍需逐一验证。
近两年的一个重要转向,是把 PRR 从“天然受体库”推向“可设计受体库”。Yang et al. (2025) 通过系统发现与工程化策略,展示了合成免疫受体可以被构建出来,用以重定向植物对特定分子的识别。这类工作改变了 PRR 研究的评价标准:过去我们主要问“植物天然能识别什么”,现在还必须问“哪些胞外识别模块、跨膜连接和胞内激酶输出可以被重新组合,并仍然接入稳定、低代价的 PTI 网络”。这也提示,本章讨论的受体复合体动态、共受体依赖和 RLCK 分流,不只是机制细节,而是未来受体工程的设计约束。
3.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| Co-IP / Split-luciferase / BiFC / FRET | 验证受体-受体和受体-激酶之间的蛋白互作。Co-IP 检测稳定复合体,Split-luc 和 BiFC 检测活细胞中的互作,FRET 提供纳米级距离信息。 | Co-IP 注意去垢剂选择(影响膜蛋白复合体稳定性);BiFC 有假阳性风险(不可逆互补);FRET 需要高质量的荧光蛋白标签。 | Chinchilla et al., 2007, Nature |
| ROS 爆发动力学检测(luminol 法) | 实时监测 PAMP 处理后质外体 ROS 产生。将叶圆片置于含 luminol 和 HRP 的溶液中,加入 PAMP 后用微孔板光度计连续读取化学发光信号。 | 叶龄统一(4-5周龄莲座叶常用);预平衡时间(叶圆片切割后过夜恢复减少伤害背景);每个基因型 ≥12个叶圆片;注意不同批次 HRP 活性差异。 | Kadota et al., 2014, Mol Cell |
| Ca²⁺ 活体成像(aequorin / GCaMP) | 用 Ca²⁺ 敏感探针实时追踪胞质 Ca²⁺ 动态。Aequorin 系统提供群体水平发光读数;GCaMP 系统可结合显微镜实现单细胞分辨率成像。 | Aequorin 需要腔肠素(coelenterazine)重构;GCaMP 的动态范围和 Kd 需匹配预期 Ca²⁺ 浓度变化;注意自发荧光背景。 | Tian et al., 2019, Nature; Thor et al., 2020, Nature |
| 受体内吞追踪(FM4-64 / BFA / 活体成像) | 追踪 PRR 激活后的受体内吞、泛素化和降解动态。FM4-64 标记内吞途径;BFA(布雷菲德菌素 A)阻断内体运输;GFP 标签受体的活体共聚焦成像。 | BFA 处理时间和浓度需优化;注意 GFP 标签是否影响受体功能和内吞行为;配合蛋白酶体抑制剂 MG132 区分内吞 vs 降解。 | Beck et al., 2012, PNAS; Mbengue et al., 2016, Curr Biol |
| 体外激酶实验 + 磷酸化位点质谱 | 用纯化的重组激酶在体外磷酸化底物蛋白,通过 ³²P 标记或 LC-MS/MS 鉴定磷酸化位点。结合磷酸化位点突变体验证功能意义。 | 注意激酶自磷酸化 vs 底物磷酸化的区分;体外条件可能引入非生理性磷酸化;建议用磷酸化特异性抗体在体内验证。 | Li et al., 2014, Cell Host Microbe |
3.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
3.10参考文献
- Asai T, Tena G, Plotnikova J, et al. MAP kinase signalling cascade in Arabidopsis innate immunity. Nature, 2002, 415: 977–983.
- Beck M, Zhou J, Faulkner C, et al. Spatio-temporal cellular dynamics of the Arabidopsis flagellin receptor reveal activation status-dependent endosomal sorting. Plant Cell, 2012, 24: 4205–4219.
- Bigeard J, Colcombet J, Hirt H. Signaling mechanisms in pattern-triggered immunity (PTI). Mol Plant, 2015, 8: 521–539.
- Birkenbihl RP, Liu S, Somssich IE. Transcriptional events defining plant immune responses. Curr Opin Plant Biol, 2017, 38: 1–9.
- Cao Y, Liang Y, Tanaka K, et al. The kinase LYK5 is a major chitin receptor in Arabidopsis and forms a chitin-induced complex with related kinase CERK1. eLife, 2014, 3: e03766.
- Cheng W, Munkvold KR, Gao H, et al. Structural analysis of Pseudomonas syringae AvrPtoB bound to host BAK1 reveals two similar kinase-interacting domains in a type III effector. Cell Host Microbe, 2011, 10: 616–626.
- Chinchilla D, Zipfel C, Robatzek S, et al. A flagellin-induced complex of the receptor FLS2 and BAK1 initiates plant defence. Nature, 2007, 448: 497–500.
- Choi J, Tanaka K, Cao Y, et al. Identification of a plant receptor for extracellular ATP. Science, 2014, 343: 290–294.
- Couto D, Zipfel C. Regulation of pattern recognition receptor signalling in plants. Nat Rev Immunol, 2016, 16: 537–552.
- DeFalco TA, Bender KW, Snedden WA. Breaking the code: Ca²⁺ sensors in plant signalling. Biochem J, 2010, 425: 27–40.
- DeFalco TA, Zipfel C. Molecular mechanisms of early plant pattern-triggered immune signaling. Mol Cell, 2021, 81: 3449–3467.
- Dubiella U, Seybold H, Durian G, et al. Calcium-dependent protein kinase/NADPH oxidase activation circuit is required for rapid defense signal propagation. Proc Natl Acad Sci USA, 2013, 110: 8744–8749.
- Escobar-Restrepo JM, Huck N, Kessler S, et al. The FERONIA receptor-like kinase mediates male-female interactions during pollen tube reception. Science, 2007, 317: 656–660.
- Eulgem T, Somssich IE. Networks of WRKY transcription factors in defense signaling. Curr Opin Plant Biol, 2007, 10: 366–371.
- Feng F, Yang F, Rong W, et al. A Xanthomonas uridine 5'-monophosphate transferase inhibits plant immune kinases. Nature, 2012, 485: 114–118.
- Feng W, Kita D, Peaucelle A, et al. The FERONIA receptor kinase maintains cell-wall integrity during salt stress through Ca²⁺ signaling. Curr Biol, 2018, 28: 666–675.
- Halter T, Imkampe J, Mazzotta S, et al. The leucine-rich repeat receptor kinase BIR2 is a negative regulator of BAK1 in plant immunity. Curr Biol, 2014, 24: 134–143.
- Heese A, Hann DR, Gimenez-Ibanez S, et al. The receptor-like kinase SERK3/BAK1 is a central regulator of innate immunity in plants. Proc Natl Acad Sci USA, 2007, 104: 12217–12222.
- Jaskiewicz M, Conrath U, Peterhänsel C. Chromatin modification acts as a memory for systemic acquired resistance in the plant stress response. EMBO Rep, 2011, 12: 50–55.
- Kadota Y, Sklenar J, Derbyshire P, et al. Direct regulation of the NADPH oxidase RBOHD by the PRR-associated kinase BIK1 during plant immunity. Mol Cell, 2014, 54: 43–55.
- Lacombe S, Rougon-Cardoso A, Sherber E, et al. Interfamily transfer of a plant pattern-recognition receptor confers broad-spectrum bacterial resistance. Nat Biotechnol, 2010, 28: 365–369.
- Li L, Li M, Yu L, et al. The FLS2-associated kinase BIK1 directly phosphorylates the NADPH oxidase RbohD to control plant immunity. Cell Host Microbe, 2014, 15: 329–338.
- Liang X, Ding P, Lian K, et al. Arabidopsis heterotrimeric G proteins regulate immunity by directly coupling to the FLS2 receptor. eLife, 2016, 5: e13568.
- Liebrand TWH, van den Burg HA, Joosten MHAJ. Two for all: receptor-associated kinases SOBIR1 and BAK1. Trends Plant Sci, 2014, 19: 123–132.
- Lin W, Li B, Lu D, et al. Tyrosine phosphorylation of protein kinase complex BAK1/BIK1 mediates Arabidopsis innate immunity. Proc Natl Acad Sci USA, 2013, 111: 3632–3637.
- Lin ZJD, Liebrand TWH, Gust AA, et al. A receptor-like cytoplasmic kinase phosphorylates the host target RIN4, leading to the activation of a plant innate immune receptor. Cell Host Microbe, 2015, 17: 532–544.
- Liu Z, Wu Y, Yang F, et al. BIK1 interacts with PEPRs to mediate ethylene-induced immunity. Proc Natl Acad Sci USA, 2013, 110: 6205–6210.
- Lu D, Wu S, Gao X, et al. A receptor-like cytoplasmic kinase, BIK1, associates with a flagellin receptor complex to initiate plant innate immunity. Proc Natl Acad Sci USA, 2010, 107: 496–501.
- Macho AP, Zipfel C. Plant PRRs and the activation of innate immune signaling. Mol Cell, 2014, 54: 263–272.
- Maldonado-Bonilla LD. Composition and function of P bodies in Arabidopsis thaliana. Front Plant Sci, 2014, 5: 201.
- Mao G, Meng X, Liu Y, et al. Phosphorylation of a WRKY transcription factor by two pathogen-responsive MAPKs drives tobacco systemic acquired resistance. Plant Cell, 2011, 23: 1639–1653.
- Mbengue M, Bourdais G, Gervber F, et al. Clathrin-dependent endocytosis is required for immunity mediated by pattern recognition receptor kinases. Proc Natl Acad Sci USA, 2016, 113: 11034–11039.
- Qi J, Wang J, Gong Z, Zhou JM. Apoplastic ROS signaling in plant immunity. Curr Opin Plant Biol, 2017, 38: 92–100.
- Qiu JL, Fiil BK, Petersen K, et al. Arabidopsis MAP kinase 4 regulates gene expression through transcription factor release in the nucleus. EMBO J, 2008, 27: 2214–2221.
- Ranf S, Eschen-Lippold L, Pecher P, et al. Interplay between calcium signalling and early signalling elements during defence responses to microbe- or damage-associated molecular patterns. Plant J, 2011, 68: 100–113.
- Ranf S, Gisch N, Schäffer M, et al. A lectin S-domain receptor kinase mediates lipopolysaccharide sensing in Arabidopsis thaliana. Nat Immunol, 2015, 16: 426–433.
- Shan L, He P, Li J, et al. Bacterial effectors target the common signaling partner BAK1 to disrupt multiple MAMP receptor-signaling complexes and impede plant immunity. Cell Host Microbe, 2008, 4: 17–27.
- Shinya T, Yamaguchi K, Desaki Y, et al. Selective regulation of the chitin-induced defense response by the Arabidopsis receptor-like cytoplasmic kinase PBL27. Plant J, 2014, 79: 56–66.
- Shiu SH, Bleecker AB. Plant receptor-like kinase gene family: diversity, function, and signaling. Sci STKE, 2001, 2001: re22.
- Snoeck S, Johanndrees O, Nürnberger T, et al. Plant pattern recognition receptors: from evolutionary insight to engineering. Nat Rev Genet, 2025, 26: 268–278. DOI: 10.1038/s41576-024-00793-z.
- Snoeck S, Zhang L, Studer V, et al. β-sheet stabilization of the island domain underlies ligand-induced LRR-RP activation of plant immune signaling. Nat Commun, 2025, 16: 10958. DOI: 10.1038/s41467-025-66119-7.
- Stegmann M, Monaghan J, Smakowska-Luzan E, et al. The receptor kinase FER is a RALF-regulated scaffold controlling plant immune signaling. Science, 2017, 355: 287–289.
- Sun Y, Li L, Macho AP, et al. Structural basis for flg22-induced activation of the Arabidopsis FLS2-BAK1 immune complex. Science, 2013, 342: 624–628.
- Thor K, Jiang S, Miber E, et al. The calcium-permeable channel OSCA1.3 regulates plant stomatal immunity. Nature, 2020, 585: 569–573.
- Tian W, Hou C, Ren Z, et al. A calmodulin-gated calcium channel links pathogen patterns to plant immunity. Nature, 2019, 572: 131–135.
- Toth R, Choi S, Le Naour-Vernet M, et al. Motif-based substrate mapping of the receptor-like cytoplasmic kinase BIK1 reveals novel components and regulatory nodes of plant immunity. Nat Plants, 2026, 12: 465–480. DOI: 10.1038/s41477-025-02218-z.
- Torres MA, Dangl JL, Jones JDG. Arabidopsis gp91phox homologues AtrbohD and AtrbohF are required for accumulation of reactive oxygen intermediates in the plant defense response. Proc Natl Acad Sci USA, 2002, 99: 517–522.
- Xu G, Greene GH, Yoo H, et al. Global translational reprogramming is a fundamental layer of immune regulation in plants. Nature, 2017, 545: 487–490.
- Yang Y, Steidele CE, Huang X, et al. Engineered pattern recognition receptors enhance broad-spectrum plant resistance. Nat Biotechnol, 2025. DOI: 10.1038/s41587-025-02858-8.
- Zhang J, Li W, Xiang T, et al. Receptor-like cytoplasmic kinases integrate signaling from multiple plant immune receptors and are targeted by a Pseudomonas syringae effector. Cell Host Microbe, 2010, 7: 290–301.
- Zipfel C, Robatzek S, Navarro L, et al. Bacterial disease resistance in Arabidopsis through flagellin perception. Nature, 2004, 428: 764–767.