未解决的问题与未来方向
以精炼的开放问题清单作为全书的收束,为读者指向未来
本章目录
- 从还原到系统:范式转换的必要性
- 新技术带来的概念突破
- 计算生物学与 AI 的前景
- 跨学科融合的必要性
- 本领域的十大开放问题
- 回到起点:免疫的"默认状态"是什么?
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
回顾全书十五章的旅程,一个矛盾的图景浮现出来:我们对植物免疫的分子细节知道得越多,就越清楚地意识到自己不理解的东西有多少。我们能在冷冻电镜下以3 Å分辨率观看 ZAR1 抗病小体的组装过程 → 第4章,却无法可靠预测一个新 NLR 在田间的耐久性;我们能在无菌系统中精确重建7株细菌的合成群落 → 第15章,却无法预测这个群落在真实土壤中的行为;我们能绘制出 SA-JA-ET 激素网络的精美信号图 → 第5章,却无法解释为什么同一信号网络在不同环境条件下产生截然不同的输出。
这种矛盾不是失败,而是领域走向成熟的标志——真正的深入理解始于认识到问题的复杂性远超已有答案的覆盖范围。本章的任务不是列出一份"购物清单"式的未来研究方向,而是尝试提炼出那些能够重塑我们理解框架的根本性开放问题——回答这些问题不仅需要新数据,更需要新的概念工具和研究范式。
16.1从还原到系统:范式转换的必要性
认知演变
过去:植物免疫学的黄金时代(1990-2010)以还原主义为主导——克隆单基因、鉴定单一互作、解析单一通路。这一范式产生了大量里程碑发现(R 基因克隆、PRR 鉴定、Zigzag 模型)。
转折:2010年代以来,多组学技术、结构生物学和微生物组学的交汇揭示了免疫系统的网络性质——PTI 和 ETI 不是独立层次而是耦合系统 → 第2章;免疫不仅对抗病原也管理共生微生物 → 第10章;防御与生长不是简单的零和博弈而是复杂的动态优化 → 第11章。
现在:领域正处于范式转换的关键节点——从"发现组分和通路"转向"理解系统行为和实现可预测工程"。这一转换需要新的研究方法(系统扰动、定量建模、多尺度整合)和新的思维模式(从因果链到因果网络,从定性到定量)。
还原主义方法的局限性在几个层面特别明显:
- 组分发现 ≠ 系统理解:我们已经鉴定了数百种 PRR、NLR、激酶、转录因子和代谢酶,但将它们组装成一个能预测系统行为的定量模型——比如预测"给定基因型 × 环境 × 病原组合下的抗性水平"——仍然遥不可及。
- 模式植物 ≠ 作物系统:约70%的植物免疫机制研究来自拟南芥,但拟南芥是一种自花授粉的短生命周期一年生草本,其免疫系统的进化约束与多年生果树、异花授粉的禾本科作物或热带块根作物截然不同。关键机制在作物中的保守性和变异性仍大量未知。
- 实验室条件 ≠ 田间现实:标准免疫实验在22°C恒温、人工光照、单一病原接种的条件下进行。田间的植物同时面对温度波动、多种病原、昆虫取食、水分胁迫和微生物组互作——这些因素的组合效应远非各自单独效应的简单叠加 → 第12章。
16.2新技术带来的概念突破
突破当前瓶颈最有希望的路径之一是新技术驱动的"提问方式革新"——不是用新工具回答老问题,而是让新工具催生出以前无法提出的新问题。
单细胞组学:揭示免疫的细胞异质性
传统的转录组分析对整个组织进行混合取样,丢失了细胞间的异质性信息。单细胞 RNA-seq(scRNA-seq)正在揭示一个被忽视的维度:不同细胞类型的免疫响应截然不同。初步的植物单细胞研究已经发现,根表皮细胞、皮层细胞和维管束细胞在面对病原时激活的基因集合高度分化——免疫不是一个均匀的全组织反应,而是一个空间组织化的协调过程 (Ryu et al., 2021)。
这一发现直接挑战了我们基于"bulk"数据建立的许多信号通路模型——那些模型中的"上调"和"下调"可能是不同细胞类型中相反变化的平均效应。单细胞分辨率的免疫图谱将可能重新定义"免疫信号通路"的概念本身。
空间转录组学:免疫的地图
比单细胞更进一步的是空间转录组技术(如 MERFISH、Visium、Slide-seq),它在保留组织空间结构的同时获取基因表达信息。这对于理解免疫信号的空间传播模式特别有价值——例如:HR 细胞死亡是如何精确限定在感染位点而不扩散到整个叶片?SA 信号如何从感染点向远端传播?不同细胞层对同一病原的响应如何在空间上协调?
活体成像:实时观看免疫
光片荧光显微镜(Light Sheet Microscopy)和多光子成像技术允许在活体植物中实时追踪免疫事件的动态过程。通过荧光标记的 Ca²⁺ 传感器、ROS 探针和蛋白质互作报告系统,研究者已能在亚秒级时间分辨率下观察免疫信号在细胞间传播的波形、速度和方向——这些动态信息是静态的"快照式"实验无法获取的 (Toyota et al., 2018)。
结构生物学与 AlphaFold 革命
冷冻电镜和 AlphaFold 的结合正在以前所未有的速度产生 NLR、PRR 和效应蛋白的结构信息。AlphaFold2/3 对植物免疫领域的潜在影响是深远的:
- 预测新 NLR 的结构,推断其可能的配体和激活机制。
- 预测效应蛋白与宿主靶标的互作界面,为识别新的效应子靶标提供线索。
- 指导 NLR 工程化的合理设计——在计算机上模拟结构域交换或 ID 修改的后果 → 第14章。
但必须注意:AlphaFold 预测的是静态结构,而 NLR 的功能高度依赖于其构象动力学(自抑制态 → 激活态 → 寡聚态的转换)。结合分子动力学模拟和 cryo-EM 的多构象分析,才能真正理解结构-功能关系。
16.3计算生物学与 AI 的前景
数据密集型研究的快速增长呼唤计算方法的同步升级。AI/机器学习在植物免疫中的潜在应用至少包括三个层面:
微生物组预测
利用机器学习从"宿主基因型 + 土壤参数 + 气候数据"预测根际微生物组的组成和保护功能——这是微生物组工程产业化的关键基础设施 → 第15章。初步工作已显示,随机森林和深度学习模型可以在一定精度内预测特定环境下的微生物群落组成,但泛化能力(跨地点、跨年份)仍然有限。
蛋白质功能预测
从 NLR 的序列/结构预测其识别特异性和信号输出——这相当于在计算机上进行"虚拟 R 基因克隆"。目前的挑战是训练数据的不足——已被功能验证的 NLR-效应子配对仅有数十对,远不足以训练可靠的预测模型。但随着高通量效应子文库筛选技术的发展,训练数据有望快速增长。
疾病预测与精准植保
整合气象数据、遥感图像、田间传感器数据和病原监测数据,构建"植物疾病早期预警系统"——在病害大规模暴发前预测风险并触发预防性措施。这一方向已在部分商业化平台(如 Syngenta 的 Cropwise、BASF 的 xarvio)中初步实现,但其底层模型仍以经验统计为主,缺乏对免疫机制的整合。
对 AI 在免疫研究中的应用需要保持审慎的态度:预测能力不等于理解。一个能准确预测抗性表型的"黑箱"模型在实用层面有价值,但不能替代对因果机制的真正理解——而后者是进行rational design 和创新的基础。最理想的路线是"可解释的AI"(interpretable AI)——模型不仅给出预测,还揭示预测背后的生物学特征,从而生成可验证的新假说。
16.4跨学科融合的必要性
植物免疫学正在经历一个从"独立学科"向"交叉学科"的深刻转变。下一个十年的突破很可能来自与相邻领域的意外碰撞:
- 生态学 × 免疫学:在自然生态系统中,免疫不是孤立运作的——它嵌入在植物-昆虫-微生物-环境的多方互作网络中。生态免疫学(eco-immunology)的视角可以揭示实验室研究中看不到的免疫系统设计逻辑——例如为什么自然群体中维持着大量"弱抗性"等位基因,而不是收敛到少数"强抗性"等位基因?
- 进化生物学 × 免疫学:比较基因组学和群体遗传学正在揭示免疫基因的进化动力学——NLR 基因的快速诞生/死亡动态、频率依赖选择的证据、以及基因流对抗性多样性的维持 → 第6章、→ 第9章。
- 化学生物学 × 免疫学:化学生物学提供了一套正交于遗传学的工具——通过小分子探针特异性地干扰信号通路中的单一步骤,在时间精度和靶标特异性上可能超越遗传突变体。化学遗传学筛选已在鉴定新的免疫信号节点方面展示了价值。
- 物理学/工程学 × 免疫学:定量物理学的思维方式——测量、建模、预测——正是植物免疫学从定性描述走向定量理解所需要的。此外,微流控和生物传感器技术为田间实时监测免疫状态提供了新的工程可能。
16.5本领域的十大开放问题
以下十个问题不是简单的"知识空白",而是回答任何一个都可能重塑我们对植物免疫理解框架的根本性问题:
- 植物免疫是否存在真正的"记忆"?Priming 和跨代免疫效应暗示植物具有某种形式的免疫记忆,但其分子基础(表观遗传修饰、代谢物积累、信号蛋白预置)、持续时间和可靠性仍不清楚。为什么是根本性的:如果植物确实拥有可编程的免疫记忆,那将从根本上改变我们对"植物免疫"概念的定义——免疫不再是每次独立的应答事件,而是一个具有学习能力的动态系统。同时,这也将为育种开辟"免疫训练"的全新策略。→ 第11章、→ 第13章
- 微生物组的可预测性边界在哪里?给定宿主基因型和环境参数,微生物组的组成在多大程度上是可预测的?哪些群落特征(多样性、功能冗余、关键种丰度)最能预测保护效果?为什么是根本性的:微生物组工程从"艺术"升级为"科学"的前提是预测能力。如果不能回答这个问题,微生物组育种将永远是试错——而非设计。→ 第10章、→ 第15章
- 化学防御与物理屏障的资源分配规则是什么?植物如何"决定"在不同器官、不同发育阶段和不同环境下的化学防御 vs 物理屏障的投资比例?这一"决策"是否遵循可形式化的最优理论?为什么是根本性的:回答这个问题等于揭示免疫资源配置的"经济学原理"——为什么植物没有选择"无限防御"?代价和收益是如何被内部权衡的?这是连通免疫学与进化生态学的关键接口。
- 细胞类型特异的免疫编程如何实现?同一个叶片中,表皮细胞、叶肉细胞和维管束细胞的免疫配置显著不同——这种细胞类型特异性是如何在发育过程中被编程的?为什么是根本性的:当前的免疫模型绝大多数建立在"平均细胞"的概念上。细胞类型分辨率的免疫图谱将重新定义"免疫信号通路"的含义——那些我们认为的"通路上调"可能只是少数细胞类型的极端变化,而大多数细胞根本没有响应。
- 植物能否"训练"自己的微生物组?除了被动地"筛选"微生物组,植物是否主动通过免疫信号和根分泌物来"训练"根际群落的功能?为什么是根本性的:如果植物可以"训练"微生物组,那么宿主-微生物组的互作就不再是简单的"招募",而是一个双向教育的过程——宿主学习识别有益微生物,微生物学习适应宿主环境。这将要求我们从根本上重新概念化"免疫系统"的功能范围。
- 跨界 RNA 转移在生态中的真实角色有多大?实验室中证明的跨界 RNA 转移在自然生态系统中的频率、效率和生态影响是什么?为什么是根本性的:如果跨界 RNA 转移是普遍的生态现象,那么"基因组"的边界将变得模糊——RNA 成为物种间共享的调控资源。这不仅改变我们对物种独立性的理解,也为开发跨界 RNAi 策略提供了生态学依据。→ 第13章
- 气候变化将如何重塑植物-病原互作格局?温度升高、CO₂ 浓度增加和极端天气事件对免疫效率、病原分布和进化速率的三重叠加影响是什么?为什么是根本性的:绝大多数抗病育种是基于"过去的气候"进行的。如果未来的气候系统地改变了免疫-病原的力量对比,那么当前所有抗性部署的有效期都可能比预期的短得多——这不仅是科学问题,更是粮食安全的核心关切。→ 第12章
- NLR 工程能否实现"按需设计"的免疫?我们能否建立一套规则,使得给定一个效应蛋白的结构,就能设计出识别它的 NLR?为什么是根本性的:如果成功,这将是植物免疫学从"发现"到"设计"的范式飞跃——意味着我们可以在病原出现之前预制抗性,而不是在病害暴发后才匆忙寻找抗性基因。→ 第14章
- 微生物组工程在田间尺度是否可行?合成群落在受控条件下工作良好,但在田间复杂环境中是否能定殖、维持和发挥预期功能?为什么是根本性的:如果微生物组工程在田间不可靠,那么"从基础到应用"的转化链条将在最后一公里断裂。这个问题的答案将决定微生物组研究是留在学术圈内还是走向产业化。→ 第15章
- 植物免疫的统一理论框架是什么?是否可能建立一个统一的定量框架,将 PTI、ETI、激素信号、微生物组互作、环境调控和进化动力学整合到一个可预测的模型中?为什么是根本性的:这是整个领域的"终极问题"。如果答案是"可以",植物免疫学将成为一门真正的精密科学——像物理学一样能够做出可检验的定量预测。如果答案是"不可以"——因为免疫本质上是一个复杂适应系统——那么我们的目标可能需要重新定义为"理解系统的行为规律"而非"精确预测每一次互作的结果"。这两种答案将引领领域走向截然不同的未来路径。
16.6回到起点:免疫的"默认状态"是什么?
我们在第1章以一个问题开篇:植物免疫的"默认状态"究竟是什么?——是时刻高度戒备的哨兵系统,还是平时沉默、只在感知危险时才被唤醒的应答机器?
经过十五章的深入探索,我们现在能给出怎样的答案?
Ch01 的开场假设:植物免疫的默认状态可能是一个简单的二选一——"戒备"或"沉默"。
经过 ch02-15 的学习后,我们认识到:免疫系统的默认状态不是二选一,而是一个多层级的、梯度化的、环境调谐的"准备谱":
- 在受体层(ch03):PRR 和 NLR 蛋白在无病原时以自抑制构象存在于细胞中——它们不是"关闭"的,而是"待机"的,随时准备在感知配体或效应子扰动后进行构象转换。这是最接近"戒备"的一层。
- 在信号层(ch05):激素网络在无病原时维持着低水平的基础活性——SA 通路在根际维持微生物组筛选(ch10),JA 通路在发育性调控中持续起效(ch11)。这不是"沉默",而是持续的低强度"嗡嗡声"。
- 在转录层(ch13):miRNA 维持着 NLR 和信号蛋白的基线表达水平——防御基因的信使 RNA 被持续产生但迅速降解,形成一种"转录就绪"状态:翻译被抑制,但转录机器始终停驻在启动子附近(表观遗传 priming)。
- 在时间维度(ch12):免疫的"默认状态"甚至不是一个静态值,而是一个节律振荡的函数——在清晨高风险时段"预设"为较高响应性,在夜间降低到基线。
因此,更准确的描述是:植物免疫是一个"梯度化准备系统"(graded readiness system)——它不是开关,而是调光器。不同层次的防御始终维持着低水平、可调节的准备态,具体的"输出强度"由环境输入(病原信号、温度、光照、微生物组信号)的整合来决定。
回答"默认状态"问题的意义超过了学术好奇——它直接决定了我们的育种策略:如果免疫是开关,我们会追求"最强激活";如果免疫是调光器,我们应该追求"最佳调光范围"——既能快速响应,又能适时回落。后一种理解更接近真实,也要求更精细的工程化策略。
在这个意义上,ch01 的问题并没有"被回答"——它是"被深化了"。我们从一个简单的二分问题出发,经过全书的探索,走到了一个更丰富的理解:"默认状态"不是一个状态,而是一个系统属性——持续准备、多层调节、环境调谐。这也许是本书最重要的认知旅程:好的问题不会消失,它们会在知识增长的过程中变形为更深层的问题。
植物免疫学是否即将从"自然历史"阶段进入"精密科学"阶段?
物理学在18-19世纪经历了从定性描述到定量预测的转变;分子生物学在20世纪后半叶完成了从观察到工程化的跨越。植物免疫学是否正处于类似的临界点——从"发现新基因和新通路"的自然历史模式,转向"定量预测和理性设计"的精密科学模式?上述十大问题的回答将决定这一转变的方向和速度。
2024–2026 年的前沿进展让这个判断更紧迫。合成 PRR 和可激活 NLR 的出现,说明免疫系统已不只是被动解析的对象,而开始成为可重构的设计对象 (Yang et al., 2025; Wang et al., 2025)。2026 年的 BIK1 底物图谱和 helper NLR 抗病小体簇则进一步提示,所谓“免疫输出”本身也由可测量、可调控的底物网络和寡聚状态决定 (Toth et al., 2026; Ge et al., 2026)。与此同时,JA 系统免疫和根分泌物驱动的微生物组记忆研究表明,远端信号与群落状态同样可以被具体分子链路连接起来 (Gaikwad et al., 2026; Wu et al., 2025; Zeng et al., 2026)。因此,未来十年的关键不只是发现更多受体、效应子或菌株,而是建立能够跨尺度连接“分子识别—信号动力学—群落生态—田间表型”的预测框架。
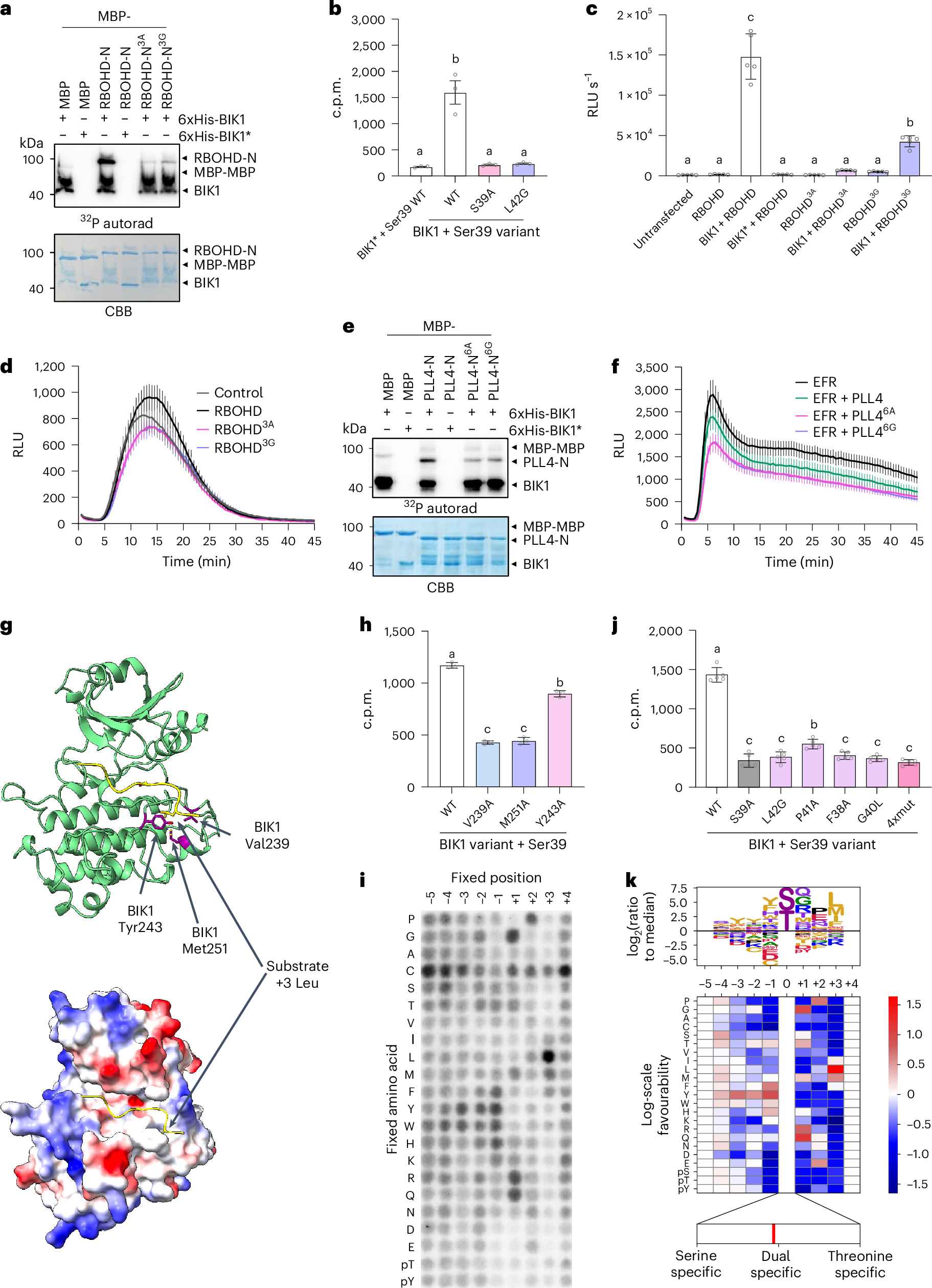
图 16.P1 论文原图:BIK1 底物图谱把早期免疫信号推向可测量网络。原图为 Toth et al. (2026) Nature Plants Fig. 1,DOI: 10.1038/s41477-025-02218-z。该图代表未来方向中的一个关键趋势:从“某个激酶很重要”走向“底物网络、调控节点和可预测输出”的系统层解析。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
16.7里程碑研究思路拆解
Ngou et al. (2021) & Yuan et al. (2021) — 新范式如何驱动研究转向
面对的问题:Zigzag 模型将 PTI 和 ETI 描述为独立的免疫层次已有15年。但零散的证据暗示两者之间可能存在深层关联——如何系统地检验这一假设?
关键思路:构建关键 PTI 信号组分(如 BAK1/SERK4、BIK1、RBOHD)的缺失突变体,然后在这些遗传背景下测试 ETI 的激活是否受到影响——如果 ETI 独立于 PTI 运作,那么 PTI 组分的缺失不应影响 ETI;反之则证明两者存在功能耦合。
关键证据链:(1)ETI 的关键输出(持续的 ROS 爆发、胼胝质沉积、PR 基因高水平表达)在 PTI 信号突变体背景下显著减弱;(2)ETI 通过上调 PRR 和 RBOHD 等 PTI 组分的表达来增强 PTI 输出,形成正反馈;(3)PTI 和 ETI 的"互相增效"(mutual potentiation)是有效免疫的基础。
影响:从根本上修正了领域对 PTI-ETI 关系的理解——从"独立两层"到"耦合系统"。这不仅是一个概念性的进步,还直接影响了育种策略:同时增强 PTI 和 ETI 的组合策略可能比只增强其中一层更有效。这两篇论文也展示了"利用极端遗传背景检验系统假说"的强大方法论 → 第2章。
16.8当前争论与未解问题
- 能否建立跨物种可迁移的免疫状态空间模型?在拟南芥中建立的信号网络模型在多大程度上可以直接映射到水稻、小麦或番茄?物种间的网络拓扑是保守的(仅节点身份不同)还是根本重组的?
- 哪些免疫节点是低代价高收益的工程化入口?不是所有免疫节点都适合作为育种靶标——理想的靶标应该能以最小的生长代价产生最大的抗性增益。识别这些"杠杆点"(leverage points)需要定量的代价-收益分析框架。
- 如何量化并验证"耐久抗性"而非"短期高抗"?当前的抗性评价体系偏重于短期(单个生长季)的高水平抗性。但田间最有价值的是跨多年仍不被克服的中等水平持久抗性。如何建立评价耐久性的实验和统计框架?
- AI 在免疫预测中如何避免黑箱与伪相关?当训练数据有限且特征空间巨大时,机器学习模型极易拟合虚假模式。植物免疫领域如何建立"可证伪的AI"标准——确保模型的预测是基于真实的生物学关联而非统计噪声?
16.9关键实验方法
| 实验方法 | 用途 | 经典文献 |
|---|---|---|
| 单细胞 RNA-seq / 空间转录组 | 解析免疫响应的细胞类型特异性和空间组织 | Ryu et al., 2021, Dev Cell |
| 跨层多组学联合(蛋白质组+代谢组+转录组) | 构建系统状态变量,连接不同分子层次 | Zhou & Zhang, 2020, Cell |
| 可证伪建模框架(ODE/Boolean 网络) | 将机制主张转化为可检验的定量预测 | Tsuda et al., 2009, PLoS Pathog |
| 系统扰动实验矩阵(组合突变体 × 多环境) | 从相关走向因果,鉴定网络中的关键节点 | Mine et al., 2017, Science |
| 长期田间监测(多年 × 多地点) | 评估抗性策略的耐久性和突破动力学 | Mundt, 2018, Phytopathology |
16.10推荐阅读
🔴 必读
🟡 重要
🟢 拓展
16.11参考文献
- Barragan AC, Weigel D. Plant NLR diversity: the known unknowns of pan-NLRomes. Curr Opin Plant Biol, 2021, 62: 102013.
- Dong OX, Ronald PC. Genetic engineering for disease resistance in plants: recent progress and future perspectives. Plant Physiol, 2019, 180: 26–38.
- Gaikwad T, Zhang L, Oates ME, et al. Rapid local and systemic jasmonate signalling drives the initiation and establishment of plant systemic immunity. Nat Plants, 2026, 12: 152–163. DOI: 10.1038/s41477-025-02178-4.
- Ge D, Ortiz-Morea FA, Xie Y, et al. Assembly of helper NLR resistosome clusters upon activation of a coiled-coil NLR. Nature, 2026, 652: 251–258. DOI: 10.1038/s41586-026-10215-1.
- Niu B, Kolter R. Quantifying host-microbiota interactions in plant disease outcomes. Annu Rev Phytopathol, 2024, 62: 273–294. DOI: 10.1146/annurev-phyto-021622-103318.
- Karasov TL, Chae E, Herman JJ, Bergelson J. Mechanisms to mitigate the trade-off between growth and defense. Plant Cell, 2017, 29: 666–680.
- Mine A, Seyfferth C, Kracher B, et al. The defense phytohormone signaling network enables rapid, high-amplitude transcriptional reprogramming during effector-triggered immunity. Plant Cell, 2018, 30: 1199–1219.
- Ngou BPM, Ahn HK, Ding P, Jones JDG. Mutual potentiation of plant immunity by cell-surface and intracellular receptors. Nature, 2021, 592: 110–115.
- Ryu KH, Huang L, Kang HM, Schiefelbein J. Single-cell RNA sequencing resolves molecular relationships among individual plant cells. Plant Physiol, 2019, 179: 1444–1456.
- Savary S, Willocquet L, Pethybridge SJ, et al. The global burden of pathogens and pests on major food crops. Nat Ecol Evol, 2019, 3: 430–439.
- Toyota M, Spencer D, Sawai-Toyota S, et al. Glutamate triggers long-distance, calcium-based plant defense signaling. Science, 2018, 361: 1112–1115.
- Toth R, Choi S, Le Naour-Vernet M, et al. Motif-based substrate mapping of the receptor-like cytoplasmic kinase BIK1 reveals novel components and regulatory nodes of plant immunity. Nat Plants, 2026, 12: 465–480. DOI: 10.1038/s41477-025-02218-z.
- Trivedi P, Leach JE, Tringe SG, et al. Plant–microbiome interactions: from community assembly to plant health. Nat Rev Microbiol, 2020, 18: 607–621.
- Tsuda K, Sato M, Stoddard T, et al. Network properties of robust immunity in plants. PLoS Genet, 2009, 5: e1000772.
- Wang X, Ji C, Wang L, et al. Remodelling autoactive NLRs for broad-spectrum immunity in plants. Nature, 2025, 645: 737–745. DOI: 10.1038/s41586-025-09252-z.
- Weiner BG, Märkle H, Laderman E, et al. A physical model links structure and function in the plant immune system. Proc Natl Acad Sci USA, 2025, 122: e2423142122. DOI: 10.1073/pnas.2423142122.
- Wu J, Hu S, Chen J, et al. Soil microbial legacy mediated by buckwheat flavonoids enhances cabbage resistance to clubroot disease. Microbiome, 2025, 13: 176. DOI: 10.1186/s40168-025-02166-y.
- Yang Y, Steidele CE, Huang X, et al. Engineered pattern recognition receptors enhance broad-spectrum plant resistance. Nat Biotechnol, 2025. DOI: 10.1038/s41587-025-02858-8.
- Yuan M, Jiang Z, Bi G, et al. Pattern-recognition receptors are required for NLR-mediated plant immunity. Nature, 2021, 592: 105–109.
- Zeng J, Wen T, Zhao J, et al. Rice roots recruit Bacillus via the secretion of heptadecanoic acid. Nat Plants, 2026. DOI: 10.1038/s41477-026-01965-x.
- Zhou JM, Zhang Y. Plant immunity: danger perception and signaling. Cell, 2020, 181: 978–989.