免疫与发育的权衡
抵抗不是免费的。植物必须在生长与防御之间做出持续的权衡
本章目录
- Growth–defense trade-off 的分子基础
- 免疫激活的发育代价
- 细胞类型特异性的权衡策略
- 发育阶段与免疫能力的动态变化
- 育种中的权衡难题:抗病与产量能否兼得
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
如果免疫没有代价,自然选择早就将每一株植物武装到牙齿。但现实是,世界上没有一种植物对所有病原都免疫,也没有一种作物在增强抗性后不付出任何产量代价。生长-防御权衡(growth-defense trade-off)是植物生物学中最基本的约束之一——它不是可以被"克服"的技术障碍,而是资源有限条件下的热力学必然。
但权衡不等于宿命。近年来的研究表明,权衡的强度高度依赖于分子机制的具体配置——某些遗传改造可以在几乎不降低产量的情况下显著提升抗性。理解权衡的分子基础,就是理解如何在"免疫"和"产量"这两个看似矛盾的目标之间找到更优的平衡点。
本章将从三个层面解析权衡:资源层面(防御消耗什么?)、信号层面(哪些分子节点是权衡的"开关"?)、以及策略层面(如何通过时空精准调控降低防御代价?)。
11.1Growth-Defense Trade-off 的分子基础
资源竞争:防御的”账单”
免疫反应的激活需要大量的代谢资源。定量估计表明,一次完整的 PTI 响应在数小时内可以将植物初级代谢的碳流重定向10-30%——从生长相关的蔗糖合成和氨基酸合成转向防御代谢物(如植保素、木质素前体、PR 蛋白)的合成 (Bolton, 2009)。
具体的代价来源包括:
- 碳骨架转移:植保素(phytoalexin)合成需要大量的苯丙烷类和萜类前体,这些前体同时也是木质素、黄酮和生长素合成的原料。合成植保素就意味着减少生长相关代谢物的供应。
- 氮的重分配:PR 蛋白(如 PR1、几丁质酶、β-1,3-葡聚糖酶)的大量合成需要显著的氮投入。在氮限制条件下,防御蛋白合成与光合蛋白(特别是 RuBisCO)的维持形成直接竞争 (Huot et al., 2014)。
- 能量消耗:ROS 的产生(RBOHD 消耗 NADPH)、细胞壁强化(胼胝质合成消耗 UDP-葡萄糖)和大规模转录重编程(RNA 聚合酶和核糖体的资源占用)都需要 ATP 和还原力投入。
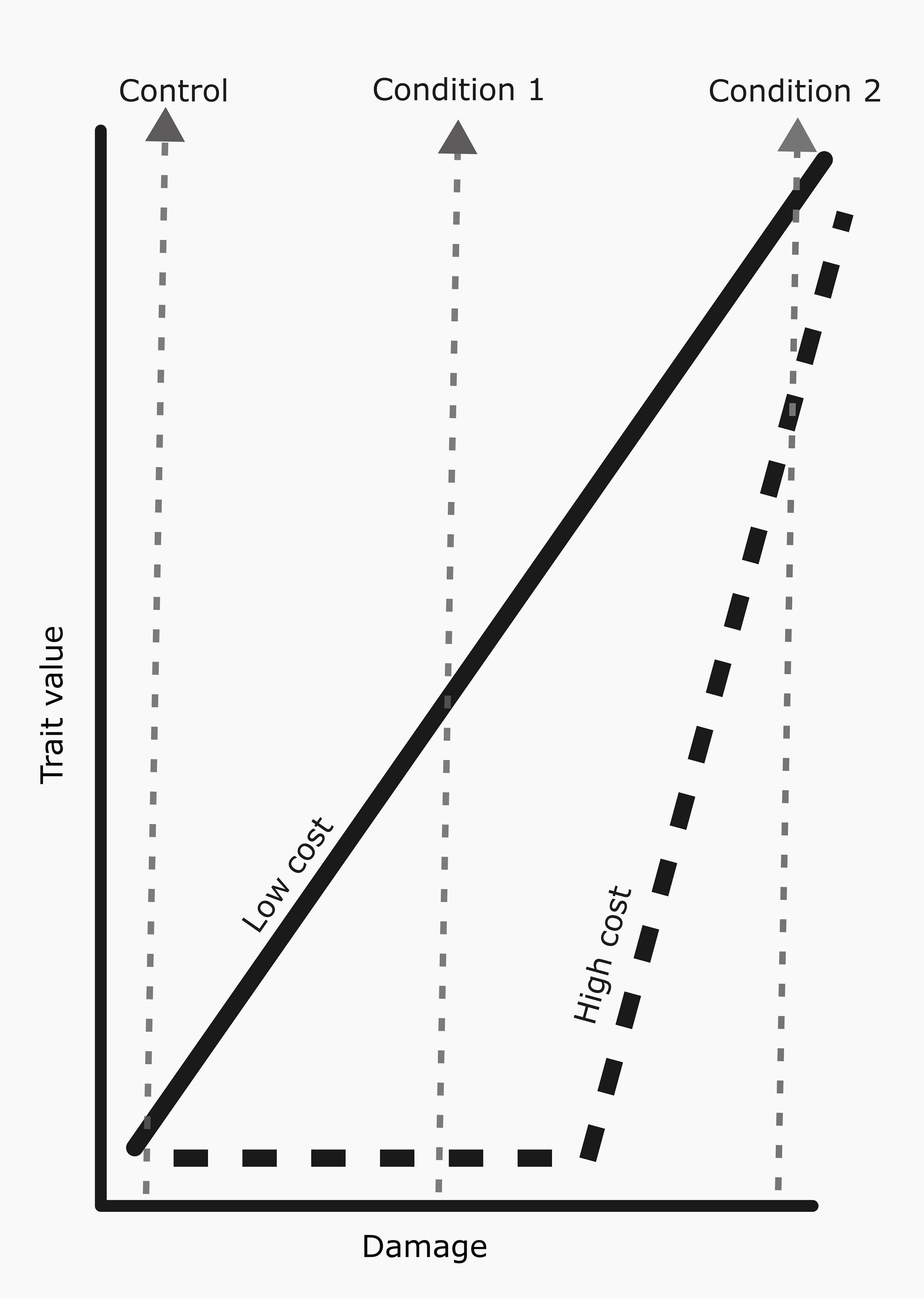
图 11.P1 论文原图:诱导抗性的防御预算与分配成本。原图为 Bass (2025) PLOS Biology Fig. 1,DOI: 10.1371/journal.pbio.3003317。该图把“防御收益”和“生长代价”放在同一预算框架下,有助于理解本章的资源权衡逻辑。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
信号拮抗:BR-免疫的”跷跷板”
除了纯粹的资源竞争外,生长和防御信号通路之间还存在直接的信号拮抗。最经典的例子是油菜素内酯(BR)信号与 PTI 信号的拮抗:
BR 受体 BRI1 和免疫受体 FLS2 共享共受体 BAK1。当 BR 信号激活时,BAK1 被优先招募到 BRI1 复合体中,减少了其参与 FLS2 信号的可用量——这在分子水平创造了”生长 vs 免疫”的直接竞争 (Lozano-Durán et al., 2013; Belkhadir et al., 2012) → 第3章 3.1节。
在转录因子水平,BZR1(BR 信号的核心转录因子)和 WRKY 防御转录因子之间存在拮抗互作。BZR1 直接结合 WRKY 基因的启动子并抑制其转录;反过来,高水平的 WRKY 活性可以抑制 BR 响应基因 (Lozano-Durán & Zipfel, 2015)。
GA(赤霉素)信号通过 DELLA 蛋白与免疫信号交叉。DELLA 蛋白是 GA 的负调控因子——GA 促进 DELLA 降解以促进生长。但 DELLA 同时也是 JA 信号的正调控因子——DELLA 与 JAZ 蛋白竞争结合 MYC2,释放 MYC2 以激活防御基因。因此,GA 促进生长(降解 DELLA)同时抑制 JA 防御(减少 DELLA-JAZ 竞争)(Hou et al., 2010; Navarro et al., 2008)。
11.2免疫激活的发育代价
组成性免疫的代价:autoimmune 突变体的教训
如果人为地将免疫系统置于”始终开启”状态,代价会有多大?拟南芥中多种自身免疫突变体提供了答案:
- snc1(suppressor of npr1-1, constitutive 1):编码一个获得功能(gain-of-function)突变的 TNL 蛋白,导致 SA 和 PR 基因的组成性激活。snc1 植物极度矮化,几乎不产生种子,但对多种病原高度抗性 (Li et al., 2001)。
- acd(accelerated cell death)系列突变体:在无病原条件下出现自发的 HR 样细胞死亡和 SA 积累,伴随严重的生长抑制 (Rate et al., 1999)。
这些突变体清楚地表明:组成性免疫激活的代价是毁灭性的——抗病性和产量不是线性权衡,而是一旦免疫超过某个阈值,生长就急剧崩溃。这暗示权衡曲线可能是非线性的(凸形),在低免疫水平时增加免疫的代价较小,但在高免疫水平时代价急剧上升。
Priming:低代价免疫增强的优雅方案
如果组成性激活代价太高,有没有”只准备不激活”的低代价方案?Priming(免疫启动/预致敏)正是这样的方案 (Mauch-Mani et al., 2017)。
经过 priming 的植物在没有病原挑战时几乎不表现防御反应(因此代价极低),但在遭遇病原时能比未经 priming 的植物更快、更强地激活防御。Priming 的分子基础包括:
- 信号蛋白的”待命”积累:MPK3/MPK6 等激酶在 priming 植物中的蛋白水平略高于基础水平,但未被磷酸化激活。一旦 PAMP 刺激到来,更多的蛋白”原料”可以被迅速激活 (Beckers et al., 2009)。
- 表观遗传标记:防御基因位点的 H3K4me3(激活标记)在 priming 后持续维持在升高水平,使这些基因处于”准备转录”的染色质状态 (Jaskiewicz et al., 2011) → 第3章 3.4节。
- 代谢物前体预储备:pipecolic acid(Pip)和 N-hydroxypipecolic acid(NHP)在 SAR 建立后积累到一定水平并维持,为下次防御响应提供”快速启动”的原料 (Hartmann et al., 2018) → 第5章 5.1节。
Priming 的代价在实验中被测量为:在无病原条件下,primed 植物相比未 primed 植物的种子产量降低约5-10%——远低于组成性免疫激活的30-50%产量损失 (van Hulten et al., 2006)。如果环境中确实存在病原压力,priming 带来的抗性增益远超其代价——这使 priming 成为进化上和农业上都极具吸引力的策略。
11.3细胞类型特异性的权衡策略
权衡不是全株均匀发生的——不同细胞类型和组织对免疫激活的响应和代价截然不同。
保卫细胞:免疫与气体交换的前线
气孔保卫细胞是免疫-生长权衡的一个微缩战场。PAMP 信号触发气孔关闭以阻止细菌入侵,但气孔关闭同时减少了 CO₂ 进入——直接抑制光合作用 (Melotto et al., 2006)。植物通过时间调控部分缓解这一矛盾:气孔在感知 PAMP 后快速关闭(数分钟),但在数小时后重新开放,即使在持续的 PAMP 存在下——这种"适应性重开"可能是一种妥协策略。病原(如P. syringae)则通过冠菌素强制重开气孔,"利用"了植物的这一妥协 → 第1章 1.1节。
维管束组织:系统性信号的高速通道
维管束不仅是水分和营养的运输通道,也是 SAR 移动信号的传播路径。维管束组织中 SA 合成酶 ICS1 的表达水平高于叶肉组织,暗示维管束是 SA 信号产生的重要位点。但 SA 在维管束中的高浓度积累可能影响韧皮部的正常运输功能——这是维管束特异性权衡的一个潜在机制。
根部 vs 地上部:不同的权衡配置
根部和叶片面对不同的威胁(土壤微生物 vs 空气传播病原/昆虫),因此权衡的配置也不同。根部更依赖 JA/ET 通路(与微生物组互作更兼容),叶片更依赖 SA 通路(对活体营养型病原更有效)→ 第5章 5.4节, 第10章。这种器官特异性的激素配置本身就是一种空间分工策略——在不同组织上应用不同的权衡解决方案。
11.4发育阶段与免疫能力的动态变化
免疫能力不是恒定的,而是随发育阶段显著变化。
年龄相关抗性(Age-Related Resistance, ARR)
许多植物物种表现出随年龄增长而抗性增强的现象——即年龄相关抗性(ARR)。在拟南芥中,5-6周龄的成年植物比2-3周龄的幼苗对P. syringae的抗性显著更强,这种增强依赖 SA 信号但独立于已知的 R 基因 (Kus et al., 2002)。
ARR 的分子基础可能涉及:
- PRR 和 NLR 表达水平随发育上调。
- SA 合成的基础能力在成年组织中更高。
- 成年植物的"免疫记忆"——可能经历了更多次的低水平 PAMP 刺激,处于 primed 状态。
开花转型与免疫的关系
开花是植物从营养生长转向生殖生长的关键转型。这一转型伴随着免疫配置的系统性调整:开花后的植物通常将更多资源转向种子发育,免疫投入可能下降。SA 信号通路的某些组分(如 NPR1)在花器官中的功能可能与叶片不同——NPR1 在花粉发育中也有角色,进一步说明免疫和发育共享分子机器。
11.5育种中的权衡难题:抗病与产量能否兼得
对育种家来说,权衡不是学术问题而是实际障碍:引入一个新的 R 基因是否会降低产量?增强 SA 信号是否会抑制生长?
打破权衡的成功案例
令人振奋的是,近年来出现了多个在不显著降低产量的情况下提升抗性的案例:
- 水稻 Pigm 位点:Deng et al. (2017) 发现,水稻抗稻瘟病基因 Pigm 位点包含两个串联的 NLR 基因——PigmR(提供广谱抗性)和 PigmS(一种不完全功能的 NLR,通过与 PigmR 异源二聚化来抑制其过度激活)。PigmS 通过表观遗传调控在花粉中特异性高表达,确保结实率不受影响。这种"内置减压阀"的设计实现了抗性与产量的平衡 → 第6章 6.4节。
- IPA1/OsSPL14 的双重功能:水稻的 IPA1(Ideal Plant Architecture 1)转录因子同时调控株型(少分蘖、大穗)和免疫(直接激活 WRKY45 的表达)。磷酸化修饰决定其在两种功能之间的切换——未磷酸化的 IPA1 促进生长,磷酸化的 IPA1 激活防御 (Wang et al., 2018)。
- 条件性启动子策略:将防御基因置于病原诱导型启动子(如 PR1 启动子)而非组成性启动子(如 35S)控制下,确保防御基因只在病原存在时被激活——这在概念上模拟了 priming,在实践中显著降低了"空闲时代价"。
权衡不是一个固定的物理定律,而是一个可以被工程优化的设计参数。关键不是"消除权衡"(这在热力学上不可能),而是"优化权衡曲线"——在相同的抗性水平下降低代价,或在相同的代价下提升抗性。Pigm 的"内置减压阀"和 IPA1 的"磷酸化开关"展示了自然进化已经找到的两种优雅解决方案。
权衡曲线的形状是什么——线性、凸形还是存在"甜蜜点"?
如果权衡是严格线性的(每1%的抗性增益对应固定的产量损失),那么优化空间有限。但如果权衡曲线是凸形的(在低免疫水平增加抗性的代价很小,但在高免疫水平代价急剧上升),那么就存在一个"甜蜜点"——在这个点上抗性/代价的比值最优。来自 autoimmune 突变体的证据暗示曲线确实是非线性的。定量刻画这条曲线的形状,是将权衡从定性描述转化为定量优化的关键一步 → 第14章。
11.6里程碑研究思路拆解
里程碑 1:Deng et al. (2017) — Pigm 的"抗性-产量平衡"设计
面对的问题:广谱抗性 NLR 通常伴随严重的产量惩罚。能否找到天然的"低代价广谱抗性"位点?
关键思路:从野生稻资源中克隆广谱稻瘟病抗性位点 Pigm,发现它包含两个串联 NLR——PigmR(广谱抗性)和 PigmS(通过异源二聚化抑制 PigmR 过度激活)。PigmS 的表观遗传调控使其在花粉中高表达,确保结实率。
关键证据链:(1)PigmR 单独过表达导致矮化和减产;(2)PigmR + PigmS 共表达恢复正常产量同时保持广谱抗性;(3)PigmS 通过 DNA 甲基化在营养组织中沉默但在花粉中去甲基化激活。
影响:揭示了自然进化找到的"内置减压阀"策略,为工程化设计低代价 NLR 提供了范式。
里程碑 2:Lozano-Durán et al. (2013) — BR-免疫拮抗的分子基础
面对的问题:BR 促进生长,PTI 抑制生长——两者在分子水平是否直接拮抗?
关键思路:测试 BR 处理对 flg22 诱导的免疫输出的影响,以及 BR 信号组分(BRI1、BAK1、BZR1)与 PTI 组分的互作关系。
关键证据链:(1)BR 处理抑制 flg22 诱导的 ROS 爆发和防御基因表达;(2)BRI1 和 FLS2 竞争 BAK1——BR 信号激活时 BAK1 优先参与 BRI1 复合体;(3)BZR1 直接抑制 PTI 相关 WRKY 基因的转录。
影响:在分子水平揭示了生长-免疫拮抗的具体机制——从共受体竞争到转录因子拮抗的多层拮抗网络。
里程碑 3:van Hulten et al. (2006) — Priming 的适应度代价定量
面对的问题:Priming 被认为是低代价的免疫增强方式,但其代价究竟有多大?在有病原和无病原条件下,priming 的净适应度效应如何?
关键思路:用 β-氨基丁酸(BABA)处理拟南芥诱导 priming,在有病原和无病原条件下分别测量种子产量作为适应度指标。
关键证据链:(1)无病原条件下,primed 植物比对照产量降低约5-10%;(2)有病原条件下,primed 植物因为抗性增强而避免了更大的产量损失,净适应度显著高于对照;(3)priming 的代价远低于组成性防御激活(SA 类似物 BTH 处理导致约30%产量降低)。
影响:首次定量证明 priming 是一种"低成本保险策略"——在病原风险存在的环境中,priming 的适应度收益远超其代价。
11.7当前争论与未解问题
- 哪些分子节点可以在不降产的条件下提升抗病?Pigm 和 IPA1 是个案还是代表了一种普遍可利用的设计原则?系统性筛选具有"低代价高抗性"特征的天然变异体是一个重要的未来方向。
- 组织特异性免疫增强是否会引发系统代偿?如果在叶片中增强免疫,根部是否会被动降低免疫投入("代偿性减弱")?全株水平的资源重分配可能使局部改良的效果大打折扣。
- 多胁迫田间条件下的权衡如何应对?实验室的单一胁迫实验与田间的多胁迫现实之间存在巨大差距。当植物同时面对病原、干旱、高温和营养缺乏时,权衡的配置可能完全不同 → 第12章。
- Priming 的跨代传递是否可靠?一些证据暗示 priming 状态可以通过表观遗传机制传递给后代。但这种"跨代免疫记忆"的稳定性、可遗传代数和环境依赖性尚不清楚。
11.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 抗病-产量双终点评估 | 同时测量免疫表型(病原增殖/病斑面积)和生长/产量表型(生物量/种子产量/千粒重),定量刻画权衡曲线。 | 两种终点需在同一批植物上测量(避免批次效应);产量测量需要足够的重复(≥20株/处理);注意生长条件对权衡强度的影响。 | Huot et al., 2014, Mol Plant |
| 激素/转录因子扰动实验 | 通过基因突变、过表达或化学处理操控特定激素/转录因子的活性,测试其对权衡平衡的影响。鉴定权衡的"开关节点"。 | 注意过表达水平的生理相关性;化学处理的浓度和时间需要优化;需要同时测量多个生长和免疫指标。 | Lozano-Durán & Zipfel, 2015, Trends Plant Sci |
| Priming 代价的适应度测量 | 在有/无病原条件下比较 primed 和未 primed 植物的种子产量,计算 priming 的净适应度效应。 | 需要在田间或模拟田间条件下进行才有生态学意义;Priming 诱导方法(化学/生物/遗传)的选择影响结果;多世代实验可评估跨代效应。 | van Hulten et al., 2006, PNAS |
| 条件性启动子/诱导系统 | 将防御基因置于病原诱导型或组织特异型启动子控制下,测试条件性表达是否降低权衡代价。 | 启动子泄漏(leakiness)是关键问题——即使微量的基础表达也可能导致可检测的代价;诱导动态需匹配防御需求。 | Ning et al., 2017, Trends Plant Sci |
11.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
11.10参考文献
- Beckers GJM, Jaskiewicz M, Liu Y, et al. Mitogen-activated protein kinases 3 and 6 are required for full priming of stress responses in Arabidopsis thaliana. Plant Cell, 2009, 21: 944–953.
- Belkhadir Y, Jaillais Y, Epple P, et al. Brassinosteroids modulate the efficiency of plant immune responses to microbe-associated molecular patterns. Proc Natl Acad Sci USA, 2012, 109: 297–302.
- Bass E. Cutting the defense budget: How allocation costs shape induced resistance in plants. PLOS Biol, 2025, 23: e3003317. DOI: 10.1371/journal.pbio.3003317.
- Bolton MD. Primary metabolism and plant defense — fuel for the fire. Mol Plant-Microbe Interact, 2009, 22: 487–497.
- Deng Y, Zhai K, Xie Z, et al. Epigenetic regulation of antagonistic receptors confers rice blast resistance with yield balance. Science, 2017, 355: 962–965.
- Hartmann M, Zeier T, Bernsdorff F, et al. Flavin monooxygenase-generated N-hydroxypipecolic acid is a critical element of plant systemic immunity. Cell, 2018, 173: 456–469.
- Hou X, Lee LYC, Xia K, et al. DELLAs modulate jasmonate signaling via competitive binding to JAZs. Dev Cell, 2010, 19: 884–894.
- Huot B, Yao J, Montgomery BL, He SY. Growth-defense tradeoffs in plants: a balancing act to optimize fitness. Mol Plant, 2014, 7: 1267–1287.
- Jaskiewicz M, Conrath U, Peterhänsel C. Chromatin modification acts as a memory for systemic acquired resistance in the plant stress response. EMBO Rep, 2011, 12: 50–55.
- Karasov TL, Chae E, Herman JJ, Bergelson J. Mechanisms to mitigate the trade-off between growth and defense. Plant Cell, 2017, 29: 666–680.
- Kus JV, Zaton K, Sarber R, Cameron RK. Age-related resistance in Arabidopsis is a basal defense response mediated by SA. Plant Physiol, 2002, 128: 1052–1059.
- Li X, Clarke JD, Zhang Y, Dong X. Activation of an EDS1-mediated R-gene pathway in the snc1 mutant leads to constitutive, NPR1-independent pathogen resistance. Mol Plant-Microbe Interact, 2001, 14: 1131–1139.
- Lozano-Durán R, Macho AP, Boutrot F, et al. The transcriptional regulator BZR1 mediates trade-off between plant innate immunity and growth. eLife, 2013, 2: e00983.
- Lozano-Durán R, Zipfel C. Trade-off between growth and immunity: role of brassinosteroids. Trends Plant Sci, 2015, 20: 12–19.
- Mauch-Mani B, Baccelli I, Luna E, Flors V. Defense priming: an adaptive part of induced resistance. Annu Rev Plant Biol, 2017, 68: 485–512.
- Melotto M, Underwood W, Koczan J, et al. Plant stomata function in innate immunity against bacterial invasion. Cell, 2006, 126: 969–980.
- Navarro L, Bari R, Achard P, et al. DELLAs control plant immune responses by modulating the balance of jasmonic acid and salicylic acid signaling. Curr Biol, 2008, 18: 650–655.
- Ning Y, Liu W, Wang GL. Balancing immunity and yield in crop plants. Trends Plant Sci, 2017, 22: 1069–1079.
- Rate DN, Cuenca JV, Bowman GR, et al. The gain-of-function Arabidopsis acd6 mutant reveals novel regulation and function of the salicylic acid signaling pathway in controlling cell death, defenses, and cell growth. Plant Cell, 1999, 11: 1695–1708.
- van Hulten M, Pelser M, van Loon LC, et al. Costs and benefits of priming for defense in Arabidopsis. Proc Natl Acad Sci USA, 2006, 103: 5602–5607.
- Wang J, Zhou L, Shi H, et al. A single transcription factor promotes both yield and immunity in rice. Science, 2018, 361: 1026–1028.