效应子的攻击策略
病原体不是被动的入侵者,它们有精密的攻击计划
本章目录
- 分泌系统的多样性
- 效应子的免疫抑制策略
- 效应子的营养劫持策略
- 线虫效应子:发育重编程而非简单杀死
- 效应子组学与功能冗余
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
在前几章中,我们从植物的视角审视了免疫系统的识别、信号和防御机制。现在是时候转换视角了——站在病原的一侧,看看它们如何系统性地瓦解这套防御体系。
效应蛋白(effector)不是随机的"毒素",而是经过亿万年共进化精炼的分子工具箱。一个成功的病原通常同时分泌数十种效应蛋白,每种靶向宿主免疫网络的不同节点,形成协同的、分层的、时序化的攻击程序。理解这种攻击的逻辑——而非仅仅记录单个效应蛋白的功能——是本章的核心目标。
一个关键的洞察是:不同进化起源的效应蛋白反复收敛到相同的宿主靶标 (Mukhtar et al., 2011)。这种"枢纽收敛"现象告诉我们,植物免疫网络中确实存在结构性的脆弱点——它们既是病原攻击的首选目标,也是育种加固的优先对象。
7.1分泌系统的多样性
效应蛋白要发挥功能,首先必须到达宿主细胞内部。不同类群的病原进化出了截然不同的效应蛋白递送系统。
细菌的 III 型分泌系统(T3SS)
T3SS 是革兰氏阴性植物病原细菌(如Pseudomonas、Xanthomonas、Ralstonia)递送效应蛋白的主要通道。T3SS 结构上类似一个"分子注射器"——由基体(basal body)、外膜环、内膜环和延伸至宿主细胞质的针状结构(pilus)组成。效应蛋白通过 N 端信号肽被识别并经 T3SS 孔道直接注入宿主细胞质 (Büttner, 2016)。
P. syringae pv. tomato DC3000 携带约30种 T3SS 效应蛋白,不同菌株间的效应蛋白组成差异很大(核心组约10-15种 + 可变组)。T3SS 本身由 hrp/hrc 基因簇编码,受温度和宿主信号调控——在28°C和植物质外体环境中被强烈诱导 (Xin et al., 2018)。
真菌和卵菌的效应蛋白递送
真菌和卵菌没有 T3SS,但同样能将效应蛋白递送到宿主细胞内。卵菌 RXLR 效应蛋白通过保守的 N 端 RXLR 基序从吸器界面进入宿主细胞——但这一转运的确切机制(是否需要病原自身的转运体,还是利用宿主的内吞途径)至今仍有激烈争议 (Whisson et al., 2007; Wawra et al., 2017)。
真菌效应蛋白的递送更为多样化:部分通过吸器分泌(如M. oryzae 的 BAS 和 AVR 蛋白经特化界面复合体 BIC 释放);部分在质外体发挥功能而不进入细胞(如 LysM 效应蛋白 Ecp6 在质外体中螯合几丁质片段,阻止被 PRR 识别)(de Jonge et al., 2010; Giraldo et al., 2013)。
病毒的效应蛋白——RNA 沉默抑制子(VSR)
病毒不需要复杂的分泌系统——它们的基因组在宿主细胞内直接翻译。RNA 沉默抑制子(Viral Suppressor of RNA silencing, VSR)是病毒最重要的"效应蛋白"。几乎所有植物病毒都编码至少一种 VSR,靶向 RNA 沉默通路的不同步骤 → 第1章 1.1节。例如,番茄丛矮病毒的 P19 蛋白通过结合21 nt siRNA 双链体阻止其装载入 RISC 复合体 (Silhavy et al., 2002);马铃薯 Y 病毒的 HC-Pro 则干扰 siRNA 甲基化 (Lakatos et al., 2006)。
图 7.1 不同类群病原的效应蛋白递送机制比较。细菌依赖 T3SS 直接注射,真菌和卵菌通过吸器或特化分泌界面递送,病毒在宿主细胞内直接翻译 VSR,线虫则用口针和食道腺分泌物重编程根细胞。
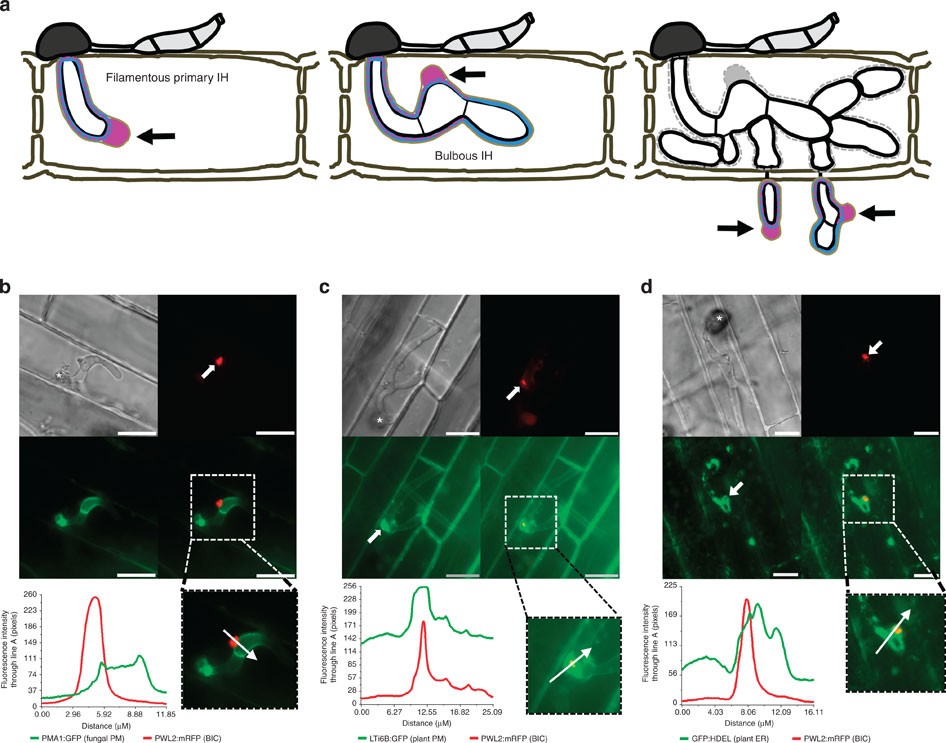
图 7.P1 论文原图:稻瘟菌效应子递送的细胞生物学证据。原图为 Giraldo et al. (2013) Nature Communications Fig. 1,DOI: 10.1038/ncomms2996。该图展示侵入菌丝、宿主膜界面和生物营养界面复合体(BIC)中效应蛋白的定位,是理解真菌效应子递送路径的经典高影响研究图。依据 CC BY-NC-ND 3.0 原样复用;图片未作裁剪、改色或内容改动。
7.2效应子的免疫抑制策略
效应蛋白对免疫网络的攻击不是随机的,而是遵循一定的策略规律。从网络生物学的角度看,攻击可以按靶标层次分类。
第一层攻击:靶向受体和共受体
受体层是免疫网络的入口,攻击受体可以同时切断多条下游通路。
- AvrPto/AvrPtoB:P. syringae 的 AvrPto 直接结合 FLS2 和 EFR 的激酶域,竞争性抑制其与 BAK1 的互作 (Xiang et al., 2008)。AvrPtoB 更为"狡猾"——其 N 端与 BAK1 互作抑制其激酶活性,C 端则具有 E3 泛素连接酶活性,直接泛素化 FLS2 导致其降解 (Göhre et al., 2008; Gimenez-Ibanez et al., 2009)。
- AvrAC:Xanthomonas campestris 的 AvrAC 是一种尿苷酰转移酶,将 UMP 基团转移到 BIK1 和 RIPK 等 RLCK 的激酶域关键残基上,直接灭活这些信号枢纽 (Feng et al., 2012) → 第3章 3.3节。
第二层攻击:靶向 MAPK 和 Ca²⁺ 信号
- HopAI1:是一种磷苏氨酸裂解酶(phosphothreonine lyase),通过不可逆地消除 MPK3/MPK6 激活环上的磷酸化修饰来灭活 MAPK 信号 (Zhang et al., 2007)。
- AvrRps4 的双功能:在抑制免疫信号的同时,AvrRps4 的 C 端结构域在细胞核中与 WRKY 转录因子互作,干扰防御基因转录 (Sohn et al., 2014)。
第三层攻击:靶向转录和蛋白稳态
- XopD(Xanthomonas):是一种 SUMO 蛋白酶,去 SUMO 化修饰 DELLA 蛋白等免疫-生长调控因子,重编程激素响应 (Kim et al., 2013)。
- PopP2(Ralstonia):乙酰转移酶,乙酰化 WRKY 转录因子的 DNA 结合域,阻止其激活防御基因 → 第4章 4.6节。当 PopP2 修饰整合在 RRS1 中的 WRKY 域时,反而触发了 ETI——这是"效应蛋白的攻击反被利用"的典型案例 (Le Roux et al., 2015)。
- 冠菌素(Coronatine):并非蛋白质效应子,而是P. syringae合成的 JA-Ile 结构类似物。冠菌素"劫持" JA 通路来拮抗对其不利的 SA 防御,是激素操纵策略的经典案例 → 第5章 5.3节 (Zheng et al., 2012)。
效应蛋白的攻击不是"一人一靶"的简单映射。许多效应蛋白是多功能的(一个蛋白靶向多个宿主蛋白),而许多宿主靶标被多种效应蛋白冗余性攻击。这种"多对多"的关系暗示:(1)攻击的目标不是消灭单个蛋白,而是瘫痪整个网络模块;(2)冗余性攻击确保即使宿主通过突变"加固"了一个节点,其他攻击路径仍然有效。
Zigzag 模型中的 ETS(Effector-Triggered Susceptibility,效应子触发感病性)常被简化为"PTI 被抑制后的默认状态",但越来越多的证据表明,ETS 不是 PTI 的简单缺失,而是效应子主动建立的、具有独特转录和代谢特征的细胞状态。例如,P. syringae 的效应子不仅关闭防御基因,还激活一系列宿主糖转运体和氨基酸代谢基因——这些基因在 PTI 被简单敲除(如 fls2 突变体)时并不会被诱导。换句话说,ETS 是病原"定制"的细胞环境,而非仅是防御失效后留下的空白 → 第1章 默认状态问题。这一认知对育种有直接启示:仅仅增强 PTI 不足以完全抵消 ETS——因为 ETS 包含了 PTI 抑制之外的新功能获得。有效的抗病策略需要同时加固被攻击的节点(恢复 PTI 输出)和阻断 ETS 特异建立的感病代谢程序。
7.3效应子的营养劫持策略
成功的病原不仅需要关闭宿主防御,还需要重编程宿主代谢以获取营养。这两个目标常常由同一套效应蛋白协同实现。
糖转运的劫持
植物的糖分主要通过 SWEET 转运体在组织间分配。多种病原利用 TAL(Transcription Activator-Like)效应蛋白直接激活宿主 SWEET 基因的转录,增加感染位点的糖分供应。Xanthomonas oryzae 的 TAL 效应蛋白 PthXo1 激活水稻 OsSWEET11,将蔗糖从维管束漏出到质外体,为细菌生长提供碳源 (Chen et al., 2010; Chen et al., 2012)。这一机制如此重要,以至于水稻中 SWEET 基因启动子的自然变异(阻止 TAL 效应蛋白结合)成为了白叶枯病抗性育种的关键靶标 → 第14章。
氨基酸和氮源获取
活体营养型病原对氮源的需求尤为突出。锈菌在吸器界面表达大量氨基酸转运体,从宿主细胞"抽取"氨基酸。某些效应蛋白还通过促进宿主蛋白的泛素化降解,间接增加游离氨基酸池——同时也破坏了防御相关蛋白的稳定性,实现"一石二鸟"(Dodds & Rathjen, 2010)。
细胞器劫持
某些效应蛋白直接靶向宿主细胞器以重编程代谢流。P. syringae 的 HopN1 定位于叶绿体并抑制光合作用相关蛋白的功能,可能既减少了 ROS 的产生(减弱防御),又将叶绿体代谢物重定向到病原可利用的形式 (Rodríguez-Herva et al., 2012)。稻瘟菌效应蛋白 MoHTR1/MoHTR2 则进入宿主细胞核,直接结合和调控宿主基因的启动子 (Kim et al., 2020)。
7.4线虫效应子:发育重编程而非简单杀死
植物寄生线虫的效应蛋白策略与细菌和真菌有一个根本区别:它们的目标不仅是抑制防御和获取营养,还要从根本上重编程宿主细胞的发育命运。
根结线虫(Meloidogyne)诱导根细胞形成巨细胞——一种多核的、代谢极度活跃的营养位点。这一过程涉及:
- 细胞周期的重编程:线虫效应蛋白(如 MiEFF1)操纵宿主的细胞周期调控因子,诱导内有丝分裂(endomitosis)而非正常的有丝分裂,产生多核细胞 (Jaouannet et al., 2012)。
- 生长素信号的劫持:线虫通过效应蛋白调控宿主的 PIN 生长素转运体和 ARF 转录因子,在感染位点创造局部的高生长素环境,驱动细胞膨大和营养汇集 (Gheysen & Mitchum, 2011)。
- 免疫的精确抑制:线虫效应蛋白(如胞囊线虫的10A06)靶向宿主的抗氧化系统和 SA 信号通路,确保巨细胞/合胞体不会被宿主的防御反应摧毁 (Hewezi & Baum, 2013) → 第1章 1.1节。
线虫效应蛋白策略的精妙之处在于:它们不是破坏宿主细胞,而是将其改造成一个专为线虫服务的"营养工厂"。这种策略需要对宿主发育和代谢网络的极其精准的操控,也使得线虫-植物互作成为研究细胞命运重编程的一个独特模型。
7.5效应子组学与功能冗余
枢纽收敛:不同效应蛋白攻击相同的宿主靶标
Mukhtar et al. (2011) 的开创性工作利用酵母双杂交系统,构建了拟南芥免疫蛋白与P. syringae效应蛋白以及H. arabidopsidis效应蛋白之间的互作网络。这项研究的核心发现是:来自不同病原、序列完全不同的效应蛋白,反复靶向同一小组宿主蛋白——这些蛋白恰好是免疫网络中的高连通度"枢纽"(hub)。
这种"枢纽收敛"(hub convergence)意味着:
- 免疫网络中确实存在结构性的脆弱点——这些枢纽蛋白如果被攻陷,将同时影响多条下游通路。
- 不同进化谱系的病原独立发现了这些脆弱点,说明枢纽的位置由网络拓扑决定,而非偶然。
- 这些枢纽蛋白同时也是 NLR 监测的重点对象——它们越是被效应蛋白攻击,植物越有选择压力进化 NLR 来保护它们("保卫假说"的网络解读)。
功能冗余与最小效应蛋白组
如果一个病原携带30种效应蛋白,它们是否都是必需的?系统性基因敲除实验表明,许多效应蛋白单独删除对毒力影响很小——因为有其他效应蛋白在功能上冗余 (Cunnac et al., 2011)。但当删除多个效应蛋白时,毒力急剧下降。Xin et al. (2018) 的"最小效应蛋白组"实验发现,P. syringae 只需要约8-10种核心效应蛋白即可在拟南芥上实现完全毒力——前提是这些效应蛋白覆盖了所有关键的宿主靶标模块。
这一发现对理解病原进化有重要意义:效应蛋白组中的"核心组"(靶向关键枢纽,不可替代)和"可变组"(功能冗余,可以在进化中被获取或丢弃)的区分,可能解释了为什么同一物种的不同菌株可以携带差异很大的效应蛋白组,却都能成功致病。
能否通过加固免疫网络的枢纽来实现广谱抗性?
如果效应蛋白的攻击收敛到少数枢纽蛋白,那么保护这些枢纽就可能获得对多种病原的广谱抗性。策略包括:(1)在枢纽蛋白上引入不影响功能但阻止效应蛋白结合的突变("枢纽加固");(2)增加枢纽蛋白的基因拷贝数或表达水平,确保即使部分蛋白被效应蛋白灭活,仍有足够功能性蛋白维持信号;(3)部署监测枢纽状态的 NLR("保卫假说"的工程化实现)。但这些策略都面临代价问题——枢纽蛋白通常也参与生长和发育功能,改变其表达或互作可能有未预期的副作用 → 第14章。
7.6里程碑研究思路拆解
里程碑 1:Mukhtar et al. (2011) — 效应蛋白-宿主互作网络与枢纽收敛
面对的问题:不同病原的效应蛋白靶标之间是否存在共性?还是各自随机攻击?
关键思路:用酵母双杂交(Y2H)系统,系统性地测试拟南芥免疫网络蛋白与来自两种进化上不相关的病原(P. syringae 细菌和 H. arabidopsidis 卵菌)的效应蛋白之间的互作。构建蛋白-蛋白互作网络,分析网络拓扑属性。
关键证据链:(1)两类病原的效应蛋白虽然序列无关,但靶向同一组高连通度宿主蛋白(枢纽收敛);(2)被效应蛋白靶向的宿主蛋白在免疫网络中具有显著高于随机预期的连通度;(3)这些枢纽蛋白同时也是 NLR 监测的高频靶标。
影响:首次在系统层面揭示了效应蛋白攻击的网络逻辑,将效应蛋白研究从"一个一个做"推向了"网络规律发现"。
里程碑 2:Chen et al. (2010) — TAL 效应蛋白劫持 SWEET 转运体
面对的问题:Xanthomonas oryzae 的 TAL 效应蛋白 PthXo1 是白叶枯病的关键毒力因子,但其宿主靶标基因未知。
关键思路:利用 TAL 效应蛋白-DNA 结合的可预测编码规则(每个 TAL 重复单元识别一个特定碱基),预测 PthXo1 在水稻基因组中的结合位点,鉴定到 OsSWEET11 启动子。
关键证据链:(1)PthXo1 直接结合 OsSWEET11 启动子并激活其转录;(2)SWEET11 是糖转运体,其激活增加了质外体的蔗糖可用性;(3)SWEET11 启动子中 TAL 结合位点的突变赋予白叶枯病抗性。
影响:揭示了病原如何通过转录劫持获取营养的完整逻辑链。SWEET 基因启动子编辑成为水稻抗病育种的实用策略。
里程碑 3:de Jonge et al. (2010) — LysM 效应蛋白螯合几丁质
面对的问题:真菌的细胞壁含有几丁质,植物的 PRR 可以识别几丁质片段。真菌如何在植物体内生长而不被持续识别?
关键思路:Cladosporium fulvum 的分泌蛋白 Ecp6 含有 LysM 结构域,可能在质外体中结合几丁质片段,阻止其被植物 PRR(CERK1/LYK5)识别。
关键证据链:(1)Ecp6 以极高亲和力(pM 级)结合几丁质寡糖;(2)Ecp6 的结合使几丁质片段不再被 CERK1 识别;(3)Ecp6 沉默导致真菌毒力显著降低。后续晶体结构揭示 Ecp6 通过两个 LysM 域的分子内二聚化"夹持"几丁质链 (Sánchez-Vallet et al., 2013)。
影响:揭示了一种全新的免疫逃避策略——不是直接攻击 PRR,而是在质外体中"截获"PAMP 配体,从源头阻断识别。这一策略在多种真菌中保守存在。
7.7当前争论与未解问题
- 哪些宿主枢纽最适合作为广谱防御加固点?枢纽收敛的证据主要来自拟南芥-丁香假单胞菌系统。在其他作物-病原系统中,枢纽蛋白是否保守?枢纽加固后的适应度代价有多大?
- 效应蛋白的时序部署有多重要?病原在感染过程中是否按特定顺序分泌不同效应蛋白?如果是,这种时序是否是攻击成功的关键?目前缺乏足够的感染时程蛋白质组数据。
- 效应蛋白之间是否存在协同攻击?某些效应蛋白可能只有在其他效应蛋白预先改变了宿主状态后才能发挥功能。这种"条件依赖性"协同如何被系统性地研究?
- 病原如何"决定"携带哪些效应蛋白?效应蛋白的获取和丢失在进化中是随机的还是受到宿主免疫构型的选择?如果是后者,能否通过监测病原群体的效应蛋白组来预测即将到来的毒力变化?
7.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 效应蛋白库筛选(Y2H / IP-MS) | 系统性鉴定效应蛋白与宿主蛋白的互作。Y2H 适合高通量初筛;IP-MS 在体内条件下验证并发现新互作。 | Y2H 假阳性率较高,需要正交验证(如 Co-IP、BiFC);IP-MS 需要优化裂解和富集条件;注意效应蛋白在植物细胞内的正确折叠。 | Mukhtar et al., 2011, Science |
| 异源表达 + 免疫表型检测 | 在植物中表达单个效应蛋白(通过农杆菌瞬时表达或转基因),检测其对 PTI 标志输出(ROS、MAPK、防御基因)的影响。 | 注意表达水平需在生理范围内(过表达可能产生非特异性毒性);需要与 GFP 等对照蛋白平行比较。 | Macho & Zipfel, 2015, Curr Opin Microbiol |
| 组合效应蛋白删除实验 | 通过系统性删除病原中的多个效应蛋白基因,构建"最小效应蛋白组",评估单个和组合删除对毒力的影响。 | 高阶多重删除的构建技术挑战大;需要考虑效应蛋白间的冗余性和补偿效应;表型变化可能只在特定条件下显现。 | Cunnac et al., 2011, Proc Natl Acad Sci USA; Xin et al., 2018, Nat Rev Microbiol |
| TAL 效应蛋白靶标预测 | 利用 TAL 效应蛋白的 DNA 结合编码规则(RVD 密码),计算预测其在宿主基因组中的结合位点和靶基因。 | 预测需要考虑 RVD 效率和位置效应;需要实验验证(ChIP-qPCR、转录激活实验);同一 TAL 可能有多个靶标。 | Chen et al., 2010, Science |
7.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
7.10参考文献
- Büttner D. Behind the lines — actions of bacterial type III effector proteins in plant cells. FEMS Microbiol Rev, 2016, 40: 894–937.
- Chen LQ, Hou BH, Lalonde S, et al. Sugar transporters for intercellular exchange and nutrition of pathogens. Nature, 2010, 468: 527–532.
- Chen LQ, Qu XQ, Hou BH, et al. Sucrose efflux mediated by SWEET proteins as a key step for phloem transport. Science, 2012, 335: 207–211.
- Cunnac S, Chakravarthy S, Kvitko BH, et al. Genetic disassembly and combinatorial reassembly identify a minimal functional repertoire of type III effectors in Pseudomonas syringae. Proc Natl Acad Sci USA, 2011, 108: 2975–2980.
- de Jonge R, van Esse HP, Kombrink A, et al. Conserved fungal LysM effector Ecp6 prevents chitin-triggered immunity in plants. Science, 2010, 329: 953–955.
- Dodds PN, Rathjen JP. Plant immunity: towards an integrated view of plant–pathogen interactions. Nat Rev Genet, 2010, 11: 539–548.
- Feng F, Yang F, Rong W, et al. A Xanthomonas uridine 5'-monophosphate transferase inhibits plant immune kinases. Nature, 2012, 485: 114–118.
- Gheysen G, Mitchum MG. How nematodes manipulate plant development pathways for infection. Curr Opin Plant Biol, 2011, 14: 415–421.
- Gimenez-Ibanez S, Hann DR, Ntoukakis V, et al. AvrPtoB targets the LysM receptor kinase CERK1 to promote bacterial virulence on plants. Curr Biol, 2009, 19: 423–429.
- Giraldo MC, Dagdas YF, Gupta YK, et al. Two distinct secretion systems facilitate tissue invasion by the rice blast fungus Magnaporthe oryzae. Nat Commun, 2013, 4: 1996.
- Göhre V, Spallek T, Häweker H, et al. Plant pattern-recognition receptor FLS2 is directed for degradation by the bacterial ubiquitin ligase AvrPtoB. Curr Biol, 2008, 18: 1824–1832.
- Hewezi T, Baum TJ. Manipulation of plant cells by cyst and root-knot nematode effectors. Mol Plant-Microbe Interact, 2013, 26: 9–16.
- Jaouannet M, Magliano M, Arguel MJ, et al. The root-knot nematode calreticulin Mi-CRT is a key effector in plant defense suppression. Mol Plant-Microbe Interact, 2013, 26: 97–105.
- Kim JG, Taylor KW, Hotson A, et al. XopD SUMO protease affects host transcription, promotes pathogen growth, and delays symptom development in Xanthomonas-infected tomato. Plant Cell, 2008, 20: 1915–1929.
- Kim S, Kim CY, Park SY, et al. Two nuclear effectors of the rice blast fungus modulate host immunity via transcriptional reprogramming. Nat Commun, 2020, 11: 5845.
- Lakatos L, Csorba T, Pantaleo V, et al. Small RNA binding is a common strategy to suppress RNA silencing by several viral suppressors. EMBO J, 2006, 25: 2768–2780.
- Le Roux C, Huet G, Jauneau A, et al. A receptor pair with an integrated decoy converts pathogen disabling of transcription factors to immunity. Cell, 2015, 161: 1074–1088.
- Macho AP, Zipfel C. Targeting of plant pattern recognition receptor-triggered immunity by bacterial type-III secretion system effectors. Curr Opin Microbiol, 2015, 23: 14–22.
- Mukhtar MS, Carvunis AR, Dreze M, et al. Independently evolved virulence effectors converge onto hubs in a plant immune system network. Science, 2011, 333: 596–601.
- Rodríguez-Herva JJ, González-Melendi P, Cuartas-Lanza R, et al. A bacterial cysteine protease effector protein interferes with photosynthesis to suppress plant innate immune responses. Cell Microbiol, 2012, 14: 669–681.
- Sánchez-Vallet A, Saleem-Batcha R, Kombrink A, et al. Fungal effector Ecp6 outcompetes host immune receptor for chitin binding through intrachain LysM dimerization. eLife, 2013, 2: e00790.
- Silhavy D, Molnár A, Lucioli A, et al. A viral protein suppresses RNA silencing and binds silencing-generated, 21- to 25-nucleotide double-stranded RNAs. EMBO J, 2002, 21: 3070–3080.
- Sohn KH, Segonzac C, Rallapalli G, et al. The nuclear immune receptor RPS4 is required for RRS1SLH1-dependent constitutive defense activation in Arabidopsis thaliana. PLoS Genet, 2014, 10: e1004655.
- Toruño TY, Stergiopoulos I, Coaker G. Plant-pathogen effectors: cellular probes interfering with plant defenses in spatial and temporal manners. Annu Rev Phytopathol, 2016, 54: 419–441.
- Wawra S, Trusch F, Matena A, et al. The RxLR motif of the host targeting effector AVR3a of Phytophthora infestans is cleaved before secretion. Plant Cell, 2017, 29: 1184–1195.
- Whisson SC, Boevink PC, Moleleki L, et al. A translocation signal for delivery of oomycete effector proteins into host plant cells. Nature, 2007, 450: 115–118.
- Xiang T, Zong N, Zou Y, et al. Pseudomonas syringae effector AvrPto blocks innate immunity by targeting receptor kinases. Curr Biol, 2008, 18: 74–80.
- Xin XF, Kvitko B, He SY. Pseudomonas syringae: what it takes to be a pathogen. Nat Rev Microbiol, 2018, 16: 316–328.
- Zhang J, Shao F, Li Y, et al. A Pseudomonas syringae effector inactivates MAPKs to suppress PAMP-induced immunity in plants. Cell Host Microbe, 2007, 1: 175–185.
- Zheng XY, Spivey NW, Zeng W, et al. Coronatine promotes Pseudomonas syringae virulence in plants by activating a signaling cascade that inhibits salicylic acid accumulation. Cell Host Microbe, 2012, 11: 587–596.