植物的识别智慧
植物如何"看穿"病原的伪装?识别策略的多样性展示了进化的创造力
本章目录
- 直接识别:最简单也最古老的策略
- 间接识别与 guard model
- Integrated decoy:将诱饵嵌入免疫受体
- 从特异性到广谱性:识别策略的谱系
- 植物如何区分敌友:免疫识别的"阈值"问题
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
第7章从病原的视角展示了效应蛋白如何系统性地瓦解植物防御。本章则从植物的视角出发,追问一个更根本的问题:面对不断进化的攻击者,植物的识别策略如何保持有效性?
如果植物只能识别效应蛋白本身("你是谁?"),那么效应蛋白的一个点突变就可能逃避识别。但如果植物识别的是效应蛋白的活动("你在做什么?"),那么效应蛋白想逃避识别就必须放弃其毒力功能——这是一个进化上的两难困境。从"识别身份"到"监测行为"的这一概念跃迁,是过去二十年植物免疫学最深刻的智识进步之一。
本章将系统梳理植物识别效应蛋白的多种策略——从最简单的直接结合,到保卫模型的间接监测,再到整合诱饵的"钓鱼"策略——并讨论每种策略的进化优劣势。我们还将探讨两个常被忽视但极为重要的问题:识别的广谱性如何实现?植物如何区分真正的敌人和无害的微生物?
8.1直接识别:最简单也最古老的策略
最直观的识别方式是 NLR 直接结合效应蛋白——类似于抗体-抗原的"锁-钥"配合。这种模式在概念上最简单,也是 Flor 基因对基因假说的原始预测 → 第1章 1.3节。
经典案例
- 水稻 Pi-ta 与 AVR-Pita:Pi-ta 的 LRR 域直接结合M. oryzae效应蛋白 AVR-Pita 的加工形式。Y2H 和体外结合实验均支持直接互作 (Jia et al., 2000)。
- 亚麻 L 与 AvrL567:亚麻锈菌的 AvrL567 效应蛋白被 L5 和 L6 NLR 直接识别。晶体结构显示 AvrL567 直接结合 L6 的 LRR 域,且结合界面的单个氨基酸替换即可改变识别特异性 (Dodds et al., 2006; Wang et al., 2007)。
- 水稻 Pik-1 与 AVR-PikD:Pik-1 的整合 HMA 域直接结合 AVR-PikD——虽然这也可以被归类为"整合诱饵"识别(见8.3节),但在分子层面,识别事件本身是直接的蛋白-蛋白结合 (Maqbool et al., 2015)。
直接识别的进化局限
直接识别虽然概念清晰,但在进化上面临一个严峻的挑战:效应蛋白可以通过结合面的点突变逃避识别,同时保持其毒力功能(因为识别面和功能面通常不完全重叠)。这导致了一种"配体逃逸"(ligand escape)动态——NLR 不断进化以追踪效应蛋白的变异,效应蛋白又进一步变异以逃避新的 NLR。这正是经典军备竞赛模型所描述的情景 → 第6章 6.3节。
实际上,纯粹的直接识别在已克隆的 R-Avr 系统中只占少数(估计不到30%)。大多数系统更符合间接识别模型——这暗示自然选择更偏好间接识别策略的进化稳定性。
8.2间接识别与 Guard Model
保卫模型(Guard Model)是植物免疫识别概念史上最重要的智识突破之一。它的核心洞见是:NLR 不需要直接识别效应蛋白本身,只需要监测效应蛋白对宿主蛋白的修饰 (Dangl & Jones, 2001; van der Biezen & Jones, 1998)。
模型的逻辑
设想一个效应蛋白 E 靶向宿主免疫蛋白 G(guardee)进行修饰(磷酸化、切割、泛素化等)以抑制免疫。在保卫模型中:
- NLR(guard)与 G(guardee)在细胞中预先形成复合体。
- E 修饰 G → G 的构象或修饰状态发生变化。
- NLR 感知到 G 状态的变化 → NLR 被激活。
- NLR 激活后触发 ETI(HR、防御基因表达等)。
经典案例:RIN4 的三方博弈
拟南芥的 RIN4(RPM1-Interacting Protein 4)是保卫模型最经典的验证案例。RIN4 是一个参与 PTI 调控的膜定位蛋白,被两种不同的P. syringae效应蛋白靶向:
- AvrRpm1 磷酸化 RIN4 → 磷酸化 RIN4 被 NLR 蛋白 RPM1 识别 → ETI 激活 (Mackey et al., 2002)。
- AvrRpt2 切割 RIN4(AvrRpt2 是一种半胱氨酸蛋白酶)→ RIN4 的消失被 NLR 蛋白 RPS2 识别 → ETI 激活 (Axtell & Staskawicz, 2003; Mackey et al., 2003)。
这个系统精妙地展示了保卫模型的核心优势:一个 guardee 可以被多个 guard 监测不同类型的修饰。RPM1 监测的是 RIN4 的磷酸化,RPS2 监测的是 RIN4 的蛋白水解——两种不同的效应蛋白攻击 RIN4 的不同方式,都会被各自对应的 NLR 捕获。
ZAR1-RKS1-PBL2 系统:保卫模型的结构生物学验证
ZAR1 抗病小体系统 → 第4章 4.4节 为保卫模型提供了原子分辨率的结构验证。在这个系统中:
- PBL2(RLCK 家族成员)是效应蛋白 AvrAC 的靶标——AvrAC 对 PBL2 进行 UMP 修饰。
- RKS1(假激酶)是 ZAR1 复合体中的"适配器",负责识别被修饰的 PBL2^UMP^。
- ZAR1 是 guard NLR,感知 RKS1-PBL2^UMP^ 复合体的形成后激活。
这个三元系统的结构解析 (Wang et al., 2019) 使保卫模型从"概念推测"升级为"原子级机制"。它还揭示了一个重要的设计原则:guard NLR 的灵活性——ZAR1 不仅通过 RKS1 监测 PBL2 的修饰,还可以通过其他适配器(如 ZED1)监测其他效应蛋白的活动。这意味着一个 guard NLR 可以通过更换适配器来监测不同的效应蛋白攻击。
保卫模型的进化优势
为什么自然选择偏好间接识别?关键在于进化稳定性:
- 效应蛋白难以逃逸:效应蛋白如果想逃避 guard NLR 的识别,就必须改变其修饰 guardee 的方式——但这往往会导致毒力功能的丧失。效应蛋白陷入了"修饰 guardee 就会被识别,不修饰 guardee 就失去毒力"的两难困境。
- 一个 guard 可以监测多种攻击:如 RIN4 的例子所示,不同效应蛋白可能以不同方式攻击同一个 guardee,每种攻击方式都可以被对应的 guard NLR 捕获——实现了"一点多重保卫"。
- Guard NLR 本身不需要快速进化:Guard NLR 识别的是 guardee 的状态变化,而非效应蛋白本身。因此 guard NLR 可以保持相对保守,减少自激活突变的风险。
保卫模型的哲学精髓是:识别"行为"比识别"身份"更有效。这与人类安全系统的设计思路不谋而合——银行不检查每个进门的人的身份,而是监测金库门锁的状态变化。这种基于"异常活动检测"的策略在进化上更稳定,因为攻击者可以改变身份(序列变异),但很难改变其必须执行的攻击行为(修饰靶标)。
8.3Integrated Decoy:将诱饵嵌入免疫受体
保卫模型的一个限制是:guardee 蛋白自身的进化受到双重约束——它既需要保持其正常功能(如 RIN4 在 PTI 调控中的角色),又需要被 guard NLR 有效监测。诱饵模型(Decoy Model)部分解决了这一问题:如果被监测的蛋白逐渐丧失其原始功能,专门演化为"诱饵",那么它的进化约束就只剩下"被效应蛋白攻击"和"被 NLR 监测"这两条 (van der Hoorn & Kamoun, 2008)。
整合诱饵模型(Integrated Decoy)则将这一逻辑推向了极致:诱饵结构域被直接整合进 NLR 蛋白自身,成为 NLR 的一个结构域 → 第4章 4.6节。这种设计有几个独特的优势:
- 识别的即时性:效应蛋白修饰整合域时,NLR 可以"第一时间"感知——因为修饰发生在自己身上,不需要等待信号从外部 guardee 传递过来。
- 遗传连锁的便利:sensor NLR 和其整合域编码在同一个基因中(或配对 NLR 基因头对头排列),确保识别组件不会在遗传重组中被分离。
- 工程化的可操作性:整合域的序列可以被人工修改以匹配新的效应蛋白靶标,为"定制 NLR"提供了清晰的策略 → 第14章。
从自然到工程:NLR 设计的前景
整合诱饵模型最激动人心的应用前景是合理设计新型 NLR。基本思路是:(1)鉴定效应蛋白在宿主中的靶标蛋白 X;(2)将 X 的结构域(或其关键片段)整合进已知的 sensor NLR 中替换原有的整合域;(3)验证新的嵌合 NLR 是否能被效应蛋白对 X 的修饰所激活。
这一策略已在概念验证水平取得初步成功:De la Concepcion 等人 (2019) 通过工程化修改水稻 Pikp-1 的 HMA 域,扩展了其对不同 AVR-Pik 等位变异的识别范围。但从概念验证到田间应用还有相当距离——嵌合 NLR 的稳定性、信号传导效率和可能的自身免疫风险都需要逐一解决。
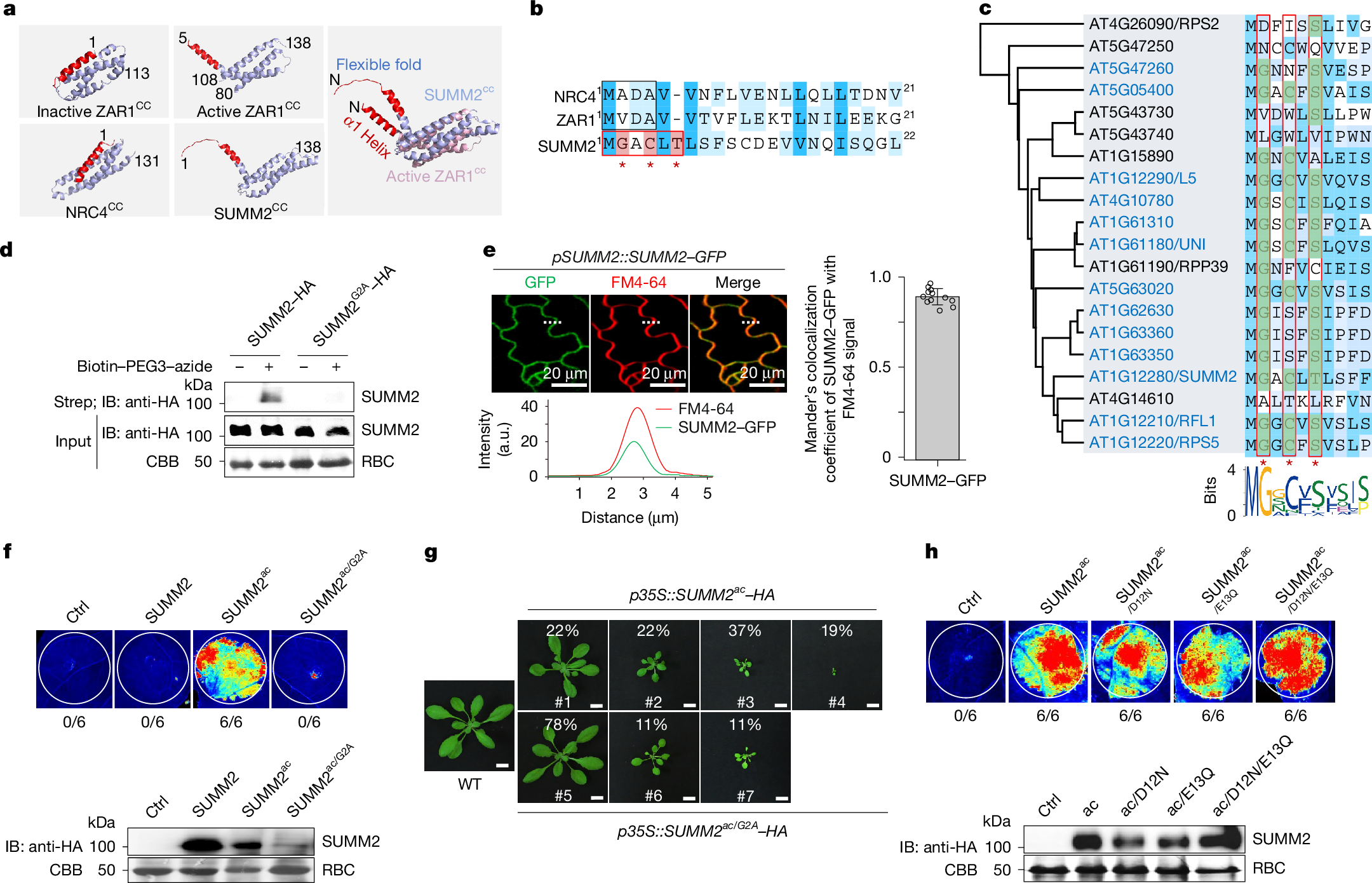
图 8.P1 论文原图:识别之后的 helper NLR 平台决定免疫输出。原图为 Ge et al. (2026) Nature Fig. 1,DOI: 10.1038/s41586-026-10215-1。该图用 CNL 型 SUMM2 激活体系说明,植物识别效应蛋白或效应蛋白活动之后,还需要通过 EDS1-PAD4-ADR1-L1 等 helper NLR 模块组织输出;这把本章的“识别智慧”延伸到“输出如何被放大和约束”。依据 CC BY-NC-ND 4.0 原样复用;图片未作裁剪、改色或内容改动。
8.4从特异性到广谱性:识别策略的谱系
不同的识别策略在"特异性-广谱性"轴上占据不同的位置:
| 识别策略 | 特异性 | 广谱性 | 进化稳定性 | 代表案例 |
|---|---|---|---|---|
| 直接识别 | 极高(单一效应蛋白等位) | 低 | 低(易被点突变逃逸) | Pi-ta/AVR-Pita |
| Guard(监测特定修饰) | 中等(特定修饰类型) | 中等(同一靶标的不同攻击者) | 高 | RPM1/RIN4 磷酸化 |
| Guard(监测靶标消失) | 较广(任何导致靶标降解的攻击) | 较高 | 高 | RPS2/RIN4 切割 |
| Integrated Decoy | 取决于整合域类型 | 可设计 | 高(整合域可独立进化) | RRS1-WRKY/PopP2 |
| PRR 识别(PAMP) | 低(保守模式) | 极高(跨物种/跨属) | 极高(靶标受功能约束) | FLS2/flg22 |
一个重要的洞见是:真正的广谱抗性可能不来自单一的"超级 NLR",而来自多种识别策略的组合部署。PRR 层提供对所有微生物的基础检测;guard NLR 层监测免疫网络枢纽的状态;整合诱饵 NLR 层提供对特定效应蛋白的高灵敏度识别。三个层次叠加,形成了一个既有广度又有深度的识别网络。
8.5植物如何区分敌友:免疫识别的"阈值"问题
植物不仅面对病原体,还与大量有益和中性微生物共存。根际微生物组(rhizosphere microbiome)和叶际微生物组(phyllosphere microbiome)中的微生物密度可达每克根际土壤10⁸-10⁹ CFU——其中绝大多数对植物无害甚至有益 → 第10章。这些微生物同样携带 PAMP(鞭毛蛋白、几丁质等),理论上应该持续触发 PTI。那么,植物如何避免对友好微生物的过度免疫反应?
阈值调控:不是"有/无"而是"多少"
答案的一部分在于信号阈值。PTI 的激活不是一个二元的"开/关"事件,而是对信号强度敏感的渐变过程。少量 PAMP 可能只引起低水平的免疫反应(如基因表达的微调),不足以触发代价高昂的全面防御输出(如 HR)。只有当 PAMP 浓度超过某个阈值——通常意味着微生物已经大量增殖(可能因为它是病原体)——才会触发完全的防御程序。
调控这一阈值的机制包括:
- PRR 的表达水平和周转率:不同组织和发育阶段的 PRR 表达水平不同,设定了不同的检测灵敏度 (Zipfel, 2014)。
- 负调控因子的基础活性:如 BIR 蛋白"占据"BAK1 阻止其与 PRR 非特异性结合,设定了激活阈值 → 第3章 3.1节。
- 有益微生物的主动免疫调节:某些根际有益菌(如P. fluorescens)通过产生特定代谢物(如2,4-DAPG)或调节植物激素水平,主动降低宿主的免疫阈值,在不触发完全 PTI 的情况下诱导 ISR (Pieterse et al., 2014) → 第10章。
效应蛋白作为"恶意信号"
如果 PAMP 识别不足以区分敌友(因为有益微生物也有 PAMP),那么效应蛋白就成为"恶意"的关键标志。只有病原体才需要分泌效应蛋白来抑制免疫和劫持代谢——有益微生物没有这个需求。因此,ETI 的激活可以被视为植物确认"正在被攻击"(而非仅仅"检测到微生物")的高可信度信号。这一逻辑与 Invasion Model 的"入侵模式"概念高度一致 → 第2章 2.4节。
免疫识别的终极挑战不是"能否检测到微生物"(PRR 可以轻易做到),而是"如何判断检测到的微生物是否构成威胁"。植物通过多层策略解决这一问题:PTI 提供"有微生物存在"的基础信号;信号强度的阈值调控区分"少量友好"和"大量入侵";ETI 的激活确认"正在被攻击"。这三个层次共同构成了一个渐进式的威胁评估系统,类似于人体免疫中"固有免疫的模式识别 → 炎症信号的强度判断 → 适应性免疫的精确响应"的分层逻辑。
能否建立一套 NLR 工程化设计的"语法规则"?
整合诱饵模型暗示 NLR 具有模块化的"设计语言":sensor 域决定识别特异性,executor 域决定信号输出,适配器决定两者的连接方式。如果能量化这些模块之间的兼容性规则——哪些整合域与哪些 NLR 骨架兼容?哪些 sensor-executor 配对能产生有效信号?——就有可能实现"按需设计"NLR 的目标。这将是植物免疫学从描述性科学向工程科学转型的标志性进步 → 第14章。
8.6里程碑研究思路拆解
8.6里程碑研究思路拆解
里程碑 1:Mackey et al. (2002) & Axtell & Staskawicz (2003) — RIN4 保卫模型的实验验证
面对的问题:R 蛋白是直接识别效应蛋白,还是间接感知效应蛋白对宿主蛋白的修饰?保卫假说需要实验验证。
关键思路:鉴定效应蛋白 AvrRpm1 和 AvrRpt2 在宿主中的共同靶标 RIN4,然后测试 NLR(RPM1 和 RPS2)是否通过监测 RIN4 的状态变化来激活。
关键证据链:(1)AvrRpm1 诱导 RIN4 磷酸化 → RPM1 激活;(2)AvrRpt2 切割 RIN4 → RPS2 激活;(3)RIN4 过表达可以抑制 RPM1 介导的 HR(RIN4 是 RPM1 的负调控因子,其状态变化解除负调控);(4)RIN4 缺失导致 RPS2 组成性激活(暗示 RPS2 监测的是 RIN4 的"存在"状态)。
影响:首次在同一个 guardee 蛋白上验证了两种不同的 guard 监测机制——磷酸化监测和蛋白水解监测——为保卫模型提供了决定性的实验证据。
里程碑 2:van der Hoorn & Kamoun (2008) — 从 Guard 到 Decoy
面对的问题:保卫模型中,guardee 蛋白同时承受两种进化压力——维持自身功能和被 guard NLR 有效监测。这两种压力是否会冲突?
关键思路:提出"诱饵模型"——当 guardee 蛋白逐渐丧失原始功能,专门演化为效应蛋白的"陷阱"时,上述进化冲突就被解决了。诱饵蛋白的唯一"功能"就是被效应蛋白攻击并触发 NLR 激活。
核心论据:理论模型分析表明,在 guard-guardee 系统中,guardee 的原始功能越弱,NLR 监测的灵敏度和特异性越高——这为 guardee 向 decoy 的进化转变提供了理论基础。
影响:完善了间接识别的概念框架,为后来整合诱饵模型的提出奠定了理论基础。
里程碑 3:De la Concepcion et al. (2019) — NLR 整合域的工程化改造
面对的问题:能否通过修改 NLR 的整合域来扩展其识别范围?
关键思路:利用 AVR-Pik 效应蛋白与 Pikp-1 HMA 域的共晶体结构,鉴定决定识别特异性的关键残基,然后通过定点突变改造 HMA 域,使其能够识别原本逃逸的 AVR-Pik 等位变异。
关键证据链:(1)结构分析鉴定了 HMA 域与 AVR-PikD 界面的关键残基;(2)基于结构的定点突变改造 HMA 域;(3)改造后的 Pikp-1 可以识别更多的 AVR-Pik 等位变异;(4)在水稻原生质体中验证了扩展的识别谱。
影响:首次证明 NLR 的识别特异性可以通过理性设计来扩展,为"按需定制 NLR"的策略提供了概念验证。但距离田间应用还需要验证稳定性、信号效率和安全性。
8.7当前争论与未解问题
- 整合域中多少是真正的"功能诱饵",多少只是中性的域获取?生物信息学鉴定了数百种 NLR 整合域类型,但其中只有少数被实验验证为功能性的效应蛋白结合位点。大规模的功能验证是一个瓶颈。
- sensor-helper 的配对规则能否被形式化?不同 sensor NLR 与哪些 helper NLR 兼容?配对的物种特异性有多强?NRC 网络在茄科中被详细描述 (Wu et al., 2017),但在其他物种中的保守性未知。
- NLR 工程化的安全边界在哪里?改造整合域可能增加自激活风险(即使在没有效应蛋白的条件下也触发 ETI)。如何建立系统性的安全测试框架?
- 免疫阈值是可编程的吗?如果能精确调控 PTI 的激活阈值,就能在特定环境下微调免疫强度——在病原压力高时提高灵敏度,在无病原压力时降低灵敏度以节省资源。实现这一目标需要什么分子工具?
8.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| NLR 整合域的系统发育分析 | 通过比较基因组学和结构域注释,鉴定 NLR 中的非典型整合域(ID),分析其进化起源和分布。 | 需要高质量的 NLR 基因注释管线(如 NLR-Annotator);注意区分真正的整合域和注释伪影;跨物种比较可以揭示保守的 ID 类型。 | Sarris et al., 2016, BMC Biol; Kroj et al., 2016, New Phytol |
| Guard/Decoy 界面的突变分析 | 通过定点突变或截短实验,鉴定 NLR-guardee/decoy 互作的关键残基和效应蛋白修饰位点。结合体外互作和体内免疫表型验证。 | 需要已知的互作对作为起点;突变设计应基于结构信息或保守性分析;注意区分"影响互作"和"影响蛋白折叠"的突变。 | Mackey et al., 2002, Cell; Wang et al., 2019, Science |
| NLR 嵌合体构建与功能测试 | 将不同 NLR 的结构域进行模块化重组(如用 NLR-A 的 sensor 域替换 NLR-B 的 sensor 域),测试嵌合 NLR 的识别特异性和信号输出能力。 | 嵌合位点的选择至关重要(通常在结构域边界处);需要验证嵌合蛋白的正确折叠和亚细胞定位;自激活筛查是必须的安全步骤。 | De la Concepcion et al., 2019, PLoS Biol |
| 效应蛋白-宿主靶标的结构解析 | 通过 X 射线晶体学或冷冻电镜解析效应蛋白与宿主靶标蛋白的共复合体结构,揭示识别/修饰的分子基础。 | 需要大量纯化的稳定复合体;某些效应蛋白需要在宿主细胞内折叠才具有功能;结构信息需要与功能实验(突变分析)相互验证。 | Maqbool et al., 2015, eLife; Wang et al., 2019, Science |
8.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
8.10参考文献
- Adachi H, Derevnina L, Kamoun S. NLR singletons, pairs, and networks: evolution, assembly, and regulation of the intracellular immunoreceptor circuitry of plants. Curr Opin Plant Biol, 2019, 50: 121–131.
- Axtell MJ, Staskawicz BJ. Initiation of RPS2-specified disease resistance in Arabidopsis is coupled to the AvrRpt2-directed elimination of RIN4. Cell, 2003, 112: 369–377.
- Białas A, Zess EK, De la Concepcion JC, et al. Lessons in effector and NLR biology of plant-microbe systems. Mol Plant-Microbe Interact, 2018, 31: 34–45.
- Cesari S, Bernoux M, Moncuquet P, et al. A novel conserved mechanism for plant NLR protein pairs: the "integrated decoy" hypothesis. Front Plant Sci, 2014, 5: 606.
- Dangl JL, Jones JDG. Plant pathogens and integrated defence responses to infection. Nature, 2001, 411: 826–833.
- De la Concepcion JC, Franceschetti M, MacLean D, et al. Protein engineering expands the effector recognition profile of a rice NLR immune receptor. eLife, 2019, 8: e47713.
- Dodds PN, Lawrence GJ, Catanzariti AM, et al. Direct protein interaction underlies gene-for-gene specificity and coevolution of the flax resistance genes and flax rust avirulence genes. Proc Natl Acad Sci USA, 2006, 103: 8888–8893.
- Ge D, Ortiz-Morea FA, Xie Y, et al. Assembly of helper NLR resistosome clusters upon activation of a coiled-coil NLR. Nature, 2026, 652: 251–258. DOI: 10.1038/s41586-026-10215-1.
- Jia Y, McAdams SA, Bryan GT, et al. Direct interaction of resistance gene and avirulence gene products confers rice blast resistance. EMBO J, 2000, 19: 4004–4014.
- Kourelis J, van der Hoorn RAL. Defended to the nines: 25 years of resistance gene cloning identifies nine mechanisms for R protein function. Plant Cell, 2018, 30: 285–299.
- Kroj T, Chanclud E, Michel-Romiti C, et al. Integration of decoy domains derived from protein targets of pathogen effectors into plant immune receptors is widespread. New Phytol, 2016, 210: 618–626.
- Le Roux C, Huet G, Jauneau A, et al. A receptor pair with an integrated decoy converts pathogen disabling of transcription factors to immunity. Cell, 2015, 161: 1074–1088.
- Mackey D, Holt BF, Wiig A, Dangl JL. RIN4 interacts with Pseudomonas syringae type III effector molecules and is required for RPM1-mediated resistance in Arabidopsis. Cell, 2002, 108: 743–754.
- Mackey D, Belkhadir Y, Alonso JM, et al. Arabidopsis RIN4 is a target of the type III virulence effector AvrRpt2 and modulates RPS2-mediated resistance. Cell, 2003, 112: 379–389.
- Maqbool A, Saitoh H, Franceschetti M, et al. Structural basis of pathogen recognition by an integrated HMA domain in a plant NLR immune receptor. eLife, 2015, 4: e08709.
- Pieterse CMJ, Zamioudis C, Berendsen RL, et al. Induced systemic resistance by beneficial microbes. Annu Rev Phytopathol, 2014, 52: 347–375.
- Sarris PF, Cevik V, Dagdas G, et al. Comparative analysis of plant immune receptor architectures uncovers host proteins likely targeted by pathogens. BMC Biol, 2016, 14: 8.
- van der Biezen EA, Jones JDG. Plant disease-resistance proteins and the gene-for-gene concept. Trends Biochem Sci, 1998, 23: 454–456.
- van der Hoorn RAL, Kamoun S. From guard to decoy: a new model for perception of plant pathogen effectors. Plant Cell, 2008, 20: 2009–2017.
- Wang CI, Gunčar G, Forwood JK, et al. Crystal structures of flax rust avirulence proteins AvrL567-A and -D reveal details of the structural basis for flax disease resistance specificity. Plant Cell, 2007, 19: 2898–2912.
- Wang J, Hu M, Wang J, et al. Reconstitution and structure of a plant NLR resistosome conferring immunity. Science, 2019, 364: eaav5870.
- Wu CH, Abd-El-Haliem A, Bozkurt TO, et al. NLR network mediates immunity to diverse plant pathogens. Proc Natl Acad Sci USA, 2017, 114: 8113–8118.
- Zipfel C. Plant pattern-recognition receptors. Trends Immunol, 2014, 35: 345–351.