植物微生物组与免疫
植物不是独居者——它在微生物的海洋中生存,免疫系统必须同时管理敌人和朋友
本章目录
- 根际微生物组的组装逻辑
- 植物基因型塑造微生物组的分子机制
- 免疫系统作为微生物组的筛选压力
- 有益微生物与诱导系统抗性(ISR)
- 病原侵染如何重塑微生物组
- 化学防御的双重角色:抗菌武器还是微生物招募信号?
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
前九章的讨论有一个隐含的假设:植物在一个相对”干净”的环境中对抗单一病原。但现实截然不同——植物的每一个表面和每一个组织都浸没在微生物的海洋中。一克根际土壤包含10⁸-10⁹个细菌细胞,代表数千个物种;一片叶片的表面可以承载10⁶-10⁷个细菌。其中绝大多数对植物无害,许多甚至有益——促进营养吸收、抑制病原、增强胁迫耐受。
这带来了一个前面章节尚未正面回答的核心问题:植物的免疫系统如何在消灭敌人的同时容忍、甚至积极招募有益微生物?答案不是简单的”更精确的识别”,而是一种更深层的系统属性——免疫系统不仅是”武器系统”,也是”微生物组的园丁”,通过持续的信号交换和代谢互作,将微生物群落的组成和功能维持在对宿主有利的状态。
本章将追溯微生物组研究与免疫研究的交汇——从根际微生物组的组装逻辑出发,经由宿主免疫的”门控”机制,到有益微生物诱导的 ISR 和病原如何重塑群落平衡,最后讨论化学防御分子在”抗菌”和”招募”之间的双重角色。
第四部分的四章——微生物组(ch10)、发育权衡(ch11)、环境因子(ch12)和非编码 RNA(ch13)——初看主题分散,实则共享一个核心问题:免疫系统如何在一个多维度约束空间中做出最优决策?这些约束包括:如何在消灭病原的同时容忍有益微生物(ch10)、如何在生长和防御之间分配有限资源(ch11)、如何在多变的环境中维持稳定的免疫输出(ch12)、以及如何在 RNA 层面实现快速、可逆的精细调控(ch13)。四章合在一起,描绘的是一幅”免疫系统在真实世界中运作”的完整图景——不是理想化、单一变量的免疫,而是被微生物组、资源预算、环境波动和调控层级共同塑造的免疫。
10.1根际微生物组的组装逻辑
根际微生物组的组成不是随机的。从散装土壤(bulk soil)到根际(rhizosphere)、根表(rhizoplane)、再到根内(endosphere),微生物的多样性逐步降低而宿主选择的印记逐步增强。这个过程被称为”两步筛选模型”(two-step selection model)(Bulgarelli et al., 2013; Edwards et al., 2015):
- 第一步:根际富集(rhizosphere enrichment):植物根系分泌有机碳(糖、有机酸、氨基酸等),这些根分泌物(root exudates)选择性地富集能利用特定碳源的微生物。不同植物物种的根分泌物组成不同,因此富集的微生物群落也不同——这是植物”主动招募”微生物的第一层机制。
- 第二步:根内筛选(endosphere selection):进入根内的微生物需要通过植物免疫系统的”安检”——包括 PAMP 识别引发的低水平 PTI 反应、抗菌代谢物的局部分泌、以及细胞壁的物理屏障。只有能够有效”谈判”(通过产生免疫调节分子或逃避识别)的微生物才能成功定殖根内。
这一模型的重要推论是:微生物组的组装是宿主主动选择和微生物适应能力共同决定的——既非纯粹的宿主控制,也非纯粹的微生物入侵。
10.2植物基因型塑造微生物组的分子机制
大量证据表明,植物基因型是微生物组组成的重要决定因子——即使在相同的土壤环境中,不同的拟南芥自然群体(accessions)也会组装出显著不同的根际微生物群落 (Lundberg et al., 2012)。哪些宿主基因负责这种”群落塑造”效应?
根分泌物的调控
根分泌物是植物向根际释放的化学信号和营养物质的总和,占植物光合产物的5-20%。其组成受多种因素调控:
- 转运体基因:ABC 转运体和 MATE 家族转运体控制特定代谢物的根际释放。例如,拟南芥 ABCG30 转运体的突变显著改变根分泌物的酚类和氨基酸组成,进而改变根际微生物群落结构 (Badri et al., 2009)。
- 次生代谢途径:不同物种特有的次生代谢产物(如十字花科的硫代葡萄糖苷、禾本科的苯并噁嗪类)在根际发挥选择性的抗菌/促菌作用 (Hu et al., 2018)。
免疫基因的群落效应
最令人惊讶的发现之一是:免疫信号通路的突变可以显著改变微生物组的组成。Lebeis et al. (2015) 在Science上报道,SA 合成或信号缺陷的拟南芥突变体(sid2、npr1 等)的根际微生物组与野生型显著不同——特别是某些细菌科(如 Streptomycetaceae)在 SA 缺陷植物中显著减少,而另一些(如某些 Proteobacteria)则增加。
这一发现的意义深远:SA 不仅是”抗病激素”,也是微生物组的”筛选因子”。SA 信号通路的持续低水平活性可能在没有病原的条件下就在根际创造一种”化学环境”,选择性地有利于某些微生物类群的定殖,不利于另一些。这将免疫-微生物组关系从”病原来了才有关”提升为”时刻都在运作”的持续互作。
类似地,Castrillo et al. (2017) 发现拟南芥磷酸盐响应通路的主调控因子 PHR1 的突变不仅影响磷营养吸收,还系统性地改变根际微生物组——暗示营养信号和免疫信号在塑造微生物组时高度整合。植物可能通过营养状态和免疫状态的联合信息来”决定”招募什么样的微生物群落。
10.3免疫系统作为微生物组的筛选压力
免疫系统如何在分子水平执行"微生物筛选"功能?多条证据线索指向以下机制:
PTI 的"门卫"功能
低水平的 PTI 信号持续存在于根际界面——即使在没有明显病原的条件下,共生微生物携带的 MAMP(如鞭毛蛋白、肽聚糖、几丁质)也会触发一定程度的 PRR 激活。这种持续的低水平 PTI 并不足以杀灭有益微生物,但可能创造一种"选择性通透"的根际环境——只有能够耐受或主动调节这种低水平免疫的微生物才能成功定殖 (Yu et al., 2019)。
支持这一观点的直接证据来自免疫受体突变体的微生物组研究。Teixeira et al. (2021) 发现,拟南芥的 min7 fls2 efr cerk1 多重突变体(同时丧失多种 PRR 和一个囊泡运输蛋白的功能)不仅对病原更敏感,其叶际微生物组也发生了显著改变——原本低丰度的潜在致病菌(如某些Xanthomonas)在突变体中大量扩增,导致菌群失调(dysbiosis)。
抗菌代谢物的选择性
植物产生的抗菌代谢物(如十字花科的异硫氰酸酯、酚类化合物、萜类等)不是等量齐观地杀灭所有微生物,而是对不同微生物类群有差异性抑制效果。例如:
- 拟南芥根系分泌的香豆素类化合物(coumarins,特别是 scopoletin 和 fraxetin)在缺铁条件下大量分泌,不仅螯合铁离子帮助植物获取铁,还选择性地抑制某些致病性真菌同时对有益的Pseudomonas几乎无影响 (Stringlis et al., 2018)。
- 玉米根系产生的苯并噁嗪类化合物(benzoxazinoids,如 DIMBOA)在土壤中降解后的产物选择性地富集特定的根际细菌群落,这些被富集的细菌反过来增强了下一代玉米的抗虫能力 (Hu et al., 2018)。
这些发现暗示:抗菌代谢物的"选择性谱"可能是植物塑造微生物组的一个关键工具——不是"杀灭一切",而是"选择性修剪"。
10.4有益微生物与诱导系统抗性(ISR)
微生物组对植物的最直接"回报"之一是诱导系统抗性(Induced Systemic Resistance, ISR)——有益根际微生物通过在根部与植物互作,增强全株对叶部病原和昆虫的抗性 (Pieterse et al., 2014)。
ISR 的分子机制
与 SA 依赖性的 SAR 不同,ISR 主要依赖 JA/ET 信号通路,且不伴随 PR 基因的组成性表达。ISR 的核心机制是priming——免疫系统被预设到一种"准备态",在遭遇病原时比未经诱导的植物更快、更强地激活防御反应 → 第11章。
ISR 的关键分子事件包括:
- MYB72 转录因子:有益菌P. fluorescens WCS417 在根部诱导 MYB72 的表达。MYB72 是 ISR 建立的必要转录因子,其下游靶标包括参与铁吸收的基因和香豆素合成基因 (Zamioudis et al., 2014)。
- NPR1 的胞质功能:ISR 的系统性传递依赖 NPR1,但有趣的是 NPR1 在 ISR 中主要发挥胞质功能(而非 SAR 中的核功能),具体机制可能涉及其对 JA/ET 信号的调节 (Pieterse et al., 1998) → 第5章 5.1节。
- 挥发性有机化合物(VOCs):某些根际细菌产生的 VOCs(如2,3-丁二醇和 acetoin)可以在不直接接触根系的情况下诱导 ISR——这种"化学通讯"可能在自然土壤中发挥重要作用 (Ryu et al., 2004)。
从单菌株到群落:ISR 的群落基础
一个重要但尚未完全解答的问题是:在自然微生物组中,ISR 是由单一的"关键种"(keystone species)驱动,还是由多种微生物的群落级功能共同贡献?
合成群落(SynCom)实验开始揭示答案。Niu et al. (2017) 构建了由7种玉米根际细菌组成的最小合成群落,发现群落的保护效果优于任何单一菌株——暗示群落成员之间的协同互作(如代谢互补、生态位分配)对于 ISR 是重要的。
10.5病原侵染如何重塑微生物组
免疫-微生物组的互作不是单向的。病原侵染会通过多种机制改变宿主的微生物组组成:
"呼救"效应(Cry for help)
一个引人入胜的假说是"植物呼救"(cry for help)——受病原攻击的植物通过改变根分泌物的组成,选择性地招募具有生防功能的微生物 (Berendsen et al., 2018)。Berendsen 等在拟南芥-Hyaloperonospora arabidopsidis系统中证明:叶部病原侵染导致根分泌物变化 → 根际群落中具有 ISR 诱导能力的细菌(如Xanthomonadaceae和Microbacteriaceae)被选择性富集 → 在"教导性"土壤(经历过病原攻击的土壤)中生长的下一代植物抗性增强。
这种"土壤记忆"(soil legacy / disease-suppressive soil)现象在农业中早有记录——连作数年后,某些土传病害会自然减轻(如小麦全蚀病的"take-all decline")——其分子基础可能正是上述"呼救-招募-保护"的循环。
2025–2026 年的研究把“呼救”从现象推进到可追踪的化学链路。Wu et al. (2025) 发现,荞麦轮作可通过黄酮类根分泌物留下可检测的土壤微生物遗产,增强后茬甘蓝对根肿病的抵抗。Zeng et al. (2026) 则在水稻中解析出一条更直接的通路:稻瘟病侵染激活 OsMAPK3-OsWRKY53-OsKCS2 轴,促进十七烷酸(heptadecanoic acid)分泌,从而选择性招募 Bacillus 形成防御性根际群落。这些结果提示,微生物组记忆并不只是“群落变化”的黑箱,而可以被具体宿主代谢物编码。
图 10.1 根分泌物驱动的微生物组记忆。近期研究显示,植物可用特定根分泌物把病原压力或轮作历史转译成群落选择压力,进而形成跨生长季的抑病性微生物组遗产。
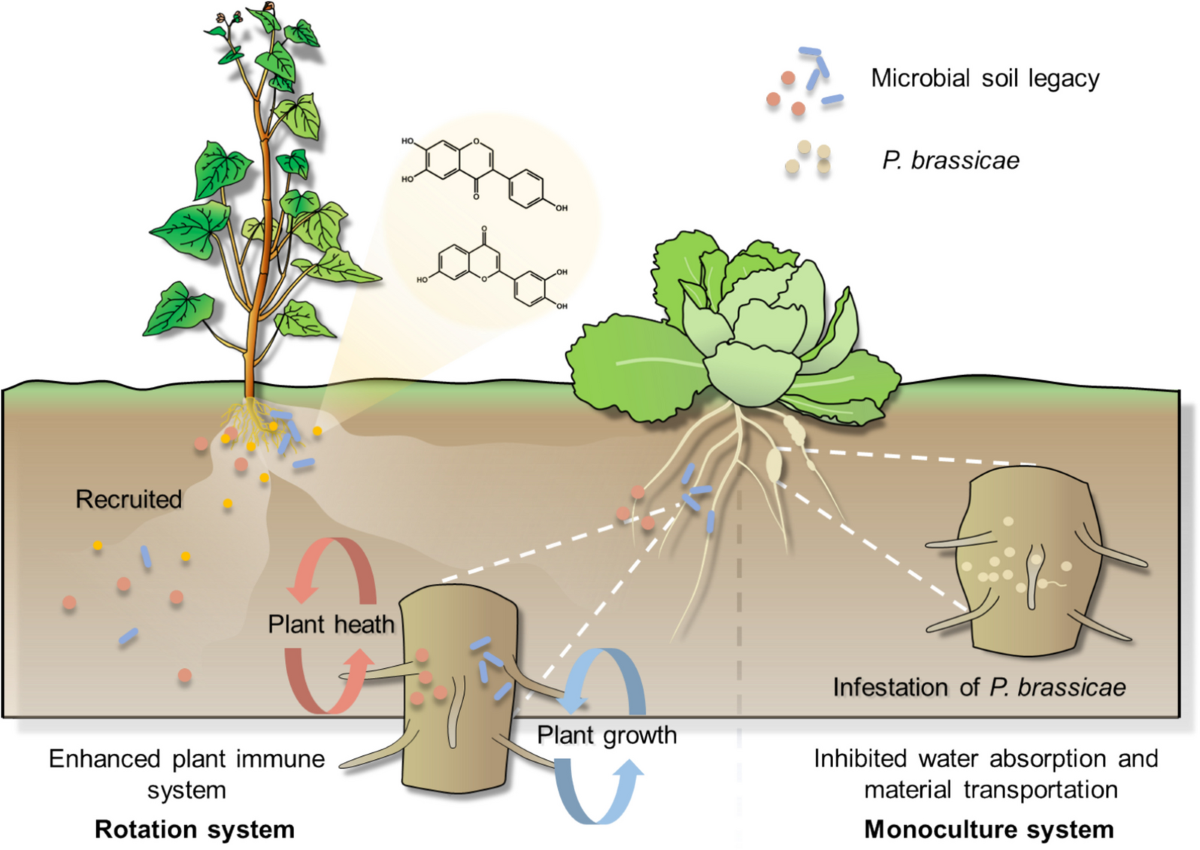
图 10.2 论文原图:荞麦黄酮介导的土壤微生物遗产。原图为 Wu et al. (2025) Microbiome Fig. 7,DOI: 10.1186/s40168-025-02166-y。依据 CC BY-NC-ND 4.0 原样复用;图片未作裁剪、改色或内容改动。
Dysbiosis:当平衡被打破
并非所有病原侵染都会触发有益的群落重组。在某些情况下,病原通过效应蛋白强烈抑制宿主免疫后,原本被免疫系统控制在低丰度的机会致病菌失去约束而大量扩增——导致菌群失调(dysbiosis)。此时的疾病不是单一病原导致的,而是免疫-群落系统的整体失稳 (Duran et al., 2018)。
这一认识对疾病管理有重要启示:某些"疾病"可能不应该用"杀灭特定病原"的策略来处理,而应该用"恢复群落平衡"的策略——类似于人类肠道菌群失调的粪菌移植治疗 → 第15章。
10.6化学防御的双重角色:抗菌武器还是微生物招募信号?
这是本章最具思辨性的问题:我们通常将植物的抗菌代谢物视为"武器"——它们杀灭或抑制微生物。但越来越多的证据表明,同一种化合物在不同浓度和不同环境下可以扮演截然相反的角色。
以香豆素为例:
- 高浓度(μM 级)的 scopoletin 对Fusarium等致病真菌具有直接的抑制活性——这是经典的"武器"功能。
- 低浓度(nM 级)的 scopoletin 可能作为信号分子被特定有益细菌感知,促进其趋化定殖——这是"招募信号"的功能。
- scopoletin 的铁螯合活性改变根际的铁可用性——这创造了一种选择性的营养环境,有利于高铁摄取效率的微生物(通常包括有益的荧光假单胞菌)。
这种"浓度/背景依赖的功能切换"暗示:植物的化学防御体系可能从一开始就不是纯粹的"武器系统",而是一种"环境工程工具"——通过精确调控化学环境来塑造微生物群落的组成。免疫和微生物组管理可能共享同一套分子机器,只是被调控到不同的输出模式。
免疫系统的"设计目标"究竟是"消灭病原"还是"维持有益群落"?
传统视角将免疫系统定义为"防御病原的系统",微生物组管理被视为附带功能。但从进化视角看,有益微生物组的持续存在可能比偶发的病原攻击更能影响植物的长期适应度。如果"维持有益群落"是免疫系统的核心功能之一——而非附带产品——那么我们理解和改造免疫系统的方式都需要根本性的转变:不是追求"最强的防御",而是追求"最佳的群落管理" → 第15章。
10.7里程碑研究思路拆解
里程碑 1:Lebeis et al. (2015) — SA 信号塑造根际微生物组
面对的问题:植物免疫信号是否影响根际微生物组的组成?免疫通路突变对微生物组的效应有多大?
关键思路:在相同土壤中种植拟南芥野生型和一系列免疫/激素信号突变体(sid2、npr1、myc2、ein2 等),通过16S rRNA 基因扩增子测序比较根际微生物组差异。
关键证据链:(1)SA 通路突变体的根际微生物组与野生型显著不同,特别是 Streptomycetaceae 等细菌科的丰度显著变化;(2)SA 信号的效应主要体现在根内(endosphere)而非根际(rhizosphere),暗示 SA 在根内定殖筛选中起作用;(3)外源施加 SA 可以部分模拟基因型效应。
影响:首次在分子遗传学水平证明植物免疫信号直接塑造微生物组组成,将免疫学和微生物组学研究连接起来。
里程碑 2:Berendsen et al. (2018) — 病原攻击触发”呼救”式群落重组
面对的问题:病原侵染是否改变根际微生物组?如果改变,是随机的扰动还是定向的保护性重组?
关键思路:对经历H. arabidopsidis叶部感染的拟南芥进行根际微生物组分析,然后将”经教导”的土壤(disease-conditioned soil)用于种植新一代植物,测试其抗性。
关键证据链:(1)叶部感染导致根际群落中具有生防功能的细菌家族选择性富集;(2)在”教导性土壤”中生长的植物对同一病原的抗性增强;(3)通过 SynCom 实验鉴定了3种关键的保护性细菌。
影响:实验支持”呼救假说”,并揭示了植物-微生物组-病原三方互作中”土壤记忆”的分子基础。为理解”抑病性土壤”现象提供了新框架。
里程碑 3:Stringlis et al. (2018) — 香豆素作为微生物组塑造分子
面对的问题:根分泌物中的哪些化学成分负责选择性地塑造微生物组?
关键思路:通过比较香豆素合成缺陷突变体(f6'h1)与野生型的根际微生物组差异,确定香豆素的群落塑造效应。结合体外抗菌实验验证选择性。
关键证据链:(1)f6'h1 突变体的根际微生物组显著改变;(2)纯化的 scopoletin 对致病性Fusarium和Verticillium具有抑制活性,但对有益的Pseudomonas无明显影响;(3)MYB72(ISR 关键转录因子)调控香豆素合成,将 ISR 和微生物组塑造在分子层面连接。
影响:首次鉴定特定根分泌物分子的微生物组选择性效应,建立了”化学防御 = 微生物组塑造工具”的概念。
10.8当前争论与未解问题
- 哪些免疫节点对微生物组组装的杠杆效应最大?是受体层(PRR)、信号层(SA/JA)还是输出层(抗菌代谢物)?目前证据分散在不同系统中,缺乏系统性的比较。
- ISR 在不同土壤类型和气候条件下的可迁移性边界在哪里?实验室和温室中的 ISR 效果在田间能否稳定复现?土壤理化性质和本底微生物组如何影响 ISR 的效率?
- 如何区分”因病致群落变化”和”群落变化致病”的因果方向?大多数研究是相关性的——在病原存在的条件下观察到群落变化,但因果关系需要通过无菌系统和 SynCom 重构来严格验证。
- 合成群落(SynCom)策略能否从实验室扩展到田间?SynCom 在无菌或灭菌土壤中工作良好,但在复杂的自然土壤中,接种的菌株能否成功定殖并发挥预期功能?竞争排斥和生态位占领是主要障碍。
- 微生物组工程是否会产生”超级杂草”风险?如果工程化微生物组赋予植物显著的竞争优势,是否需要考虑生态安全问题?这是一个尚未充分讨论的伦理和监管议题 → 第15章。
近两年的综述和实证研究把这个领域从“谁在那里”推进到“如何定量解释疾病结局”。Niu & Kolter (2024) 强调,植物病害不应只被看作“宿主 × 病原”的二元结果,而应被建模为宿主基因型、病原压力、微生物组状态与环境参数共同决定的多变量输出。与此同时,水稻叶际微生物组研究显示,宿主免疫相关基因不仅影响自身抗病性,也会塑造叶面微生物群落,并通过群落结构间接改变病害表现 (Su et al., 2024)。这意味着“免疫表型”本身可能包含一个过去被忽略的群落维度:同一个 R 基因或激素通路,在不同本底微生物组中可能产生不同的抗病效果。
10.9关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 无菌/限菌(gnotobiotic)系统 | 在无微生物的条件下培养植物,然后接种已知组成的微生物(单菌株或 SynCom),拆分宿主-微生物互作的因果关系。 | 无菌条件的严格维持;营养配方需模拟自然条件;注意无菌植物的发育表型可能与常规植物不同。 | Vorholt et al., 2017, Nat Rev Microbiol |
| 16S/ITS 扩增子测序 | 通过扩增细菌16S rRNA 基因或真菌 ITS 区域并测序,刻画微生物群落的分类组成和多样性。是微生物组研究的标准方法。 | 引物选择影响覆盖范围(V3-V4 最常用);需要足够的测序深度(>10,000 reads/样品);注意 PCR 偏好和嵌合体过滤。 | Lundberg et al., 2012, Nature |
| 合成群落(SynCom)重建 | 从培养库中选择代表性菌株组合成”最小群落”,在限菌条件下测试群落功能(如 ISR 诱导、病原抑制)。 | 菌株选择的代表性至关重要;需要测试多种组合以鉴定关键成员;菌株间的竞争和互补关系影响群落稳定性。 | Niu et al., 2017, PNAS |
| 根分泌物代谢组学 | 通过 LC-MS/MS 或 GC-MS 分析根分泌物的化学成分,鉴定宿主基因型或处理之间的差异代谢物。 | 采样方法(水培 vs 土壤 vs 琼脂)影响分泌物的组成和浓度;需要同位素内标确保定量准确性;注意区分主动分泌和被动渗漏。 | Stringlis et al., 2018, PNAS |
10.10推荐阅读
🔴 必读
🟡 重要
🟢 拓展
10.11参考文献
- Badri DV, Quintana N, El Kassis EG, et al. An ABC transporter mutation alters root exudation of phytochemicals that provoke an overhaul of natural soil microbiota. Plant Physiol, 2009, 151: 2006–2017.
- Berendsen RL, Pieterse CMJ, Bakker PAHM. The rhizosphere microbiome and plant health. Trends Plant Sci, 2012, 17: 478–486.
- Berendsen RL, Vismans G, Yu K, et al. Disease-induced assemblage of a plant-beneficial bacterial consortium. ISME J, 2018, 12: 1496–1507.
- Bulgarelli D, Schlaeppi K, Spaepen S, et al. Structure and functions of the bacterial microbiota of plants. Annu Rev Plant Biol, 2013, 64: 807–838.
- Castrillo G, Teixeira PJPL, Paredes SH, et al. Root microbiota drive direct integration of phosphate stress and immunity. Nature, 2017, 543: 513–518.
- Durán P, Thiergart T, Garrido-Oter R, et al. Microbial interkingdom interactions in roots promote Arabidopsis survival. Cell, 2018, 175: 973–983.
- Edwards J, Johnson C, Santos-Medellín C, et al. Structure, variation, and assembly of the root-associated microbiomes of rice. Proc Natl Acad Sci USA, 2015, 112: E911–E920.
- Hacquard S, Spaepen S, Garrido-Oter R, Schulze-Lefert P. Interplay between innate immunity and the plant microbiota. Annu Rev Phytopathol, 2017, 55: 565–589.
- Hu L, Robert CAM, Cadot S, et al. Root exudate metabolites drive plant-soil feedbacks on growth and defense by shaping the rhizosphere microbiota. Nat Commun, 2018, 9: 2738.
- Lebeis SL, Paredes SH, Lundberg DS, et al. Salicylic acid modulates colonization of the root microbiome by specific bacterial taxa. Science, 2015, 349: 860–864.
- Lundberg DS, Lebeis SL, Paredes SH, et al. Defining the core Arabidopsis thaliana root microbiome. Nature, 2012, 488: 86–90.
- Niu B, Paulson JN, Zheng X, Kolter R. Simplified and representative bacterial community of maize roots. Proc Natl Acad Sci USA, 2017, 114: E2450–E2459.
- Niu B, Kolter R. Quantifying host-microbiota interactions in plant disease outcomes. Annu Rev Phytopathol, 2024, 62: 273–294. DOI: 10.1146/annurev-phyto-021622-103318.
- Pieterse CMJ, Van Wees SCM, Van Pelt JA, et al. A novel signaling pathway controlling induced systemic resistance in Arabidopsis. Plant Cell, 1998, 10: 1571–1580.
- Pieterse CMJ, Zamioudis C, Berendsen RL, et al. Induced systemic resistance by beneficial microbes. Annu Rev Phytopathol, 2014, 52: 347–375.
- Ryu CM, Farag MA, Hu CH, et al. Bacterial volatiles promote growth in Arabidopsis. Proc Natl Acad Sci USA, 2003, 100: 4927–4932.
- Stringlis IA, Yu K, Feussner K, et al. MYB72-dependent coumarin exudation shapes root microbiome assembly to promote plant health. Proc Natl Acad Sci USA, 2018, 115: E5213–E5222.
- Su P, et al. Host genetic control of the rice phyllosphere microbiome contributes to disease resistance. Nat Commun, 2024, 15: 23.
- Teixeira PJPL, Colaianni NR, Fitzpatrick CR, Dangl JL. Beyond pathogens: microbiota interactions with the plant immune system. Curr Opin Microbiol, 2019, 49: 7–17.
- Trivedi P, Leach JE, Tringe SG, et al. Plant–microbiome interactions: from community assembly to plant health. Nat Rev Microbiol, 2020, 18: 607–621.
- Vorholt JA. Microbial life in the phyllosphere. Nat Rev Microbiol, 2012, 10: 828–840.
- Wu J, Hu S, Chen J, et al. Soil microbial legacy mediated by buckwheat flavonoids enhances cabbage resistance to clubroot disease. Microbiome, 2025, 13: 176. DOI: 10.1186/s40168-025-02166-y.
- Yu K, Liu Y, Tichelaar R, et al. Rhizosphere-associated Pseudomonas suppress local root immune responses by gluconic acid-mediated lowering of environmental pH. Curr Biol, 2019, 29: 3913–3920.
- Zamioudis C, Hanson J, Pieterse CMJ. β-glucosidase BGLU42 is a MYB72-dependent key regulator of rhizobacteria-induced systemic resistance and modulates iron deficiency responses in Arabidopsis roots. New Phytol, 2014, 204: 368–379.
- Zeng J, Wen T, Zhao J, et al. Rice roots recruit Bacillus via the secretion of heptadecanoic acid. Nat Plants, 2026. DOI: 10.1038/s41477-026-01965-x.