微生物组工程与生物防治
超越单一菌株,以微生物组的视角重新设计植保策略
本章目录
- 从单一菌株到合成群落(SynCom)
- 微生物组工程的策略与挑战
- 合成生物学与工程菌株
- 田间尺度的挑战:实验室结果为何往往"缩水"
- 伦理、监管与产业化
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
传统生物防治的历史可以追溯到一个多世纪前——19世纪末,研究者就注意到某些土壤中种植特定作物后病害会自然减轻。20世纪中叶以来,以Bacillus、Trichoderma和Pseudomonas为代表的单一生防菌株被广泛开发为商业制剂。然而,单一菌株策略在田间的表现长期令人失望——实验室中80-90%的抑制率到了大田常常"缩水"到20-30%,甚至完全失效 (Finkel et al., 2017)。
问题出在哪里?第10章已经揭示了一个关键认识:植物的免疫和微生物管理不是针对单一对手的一对一博弈,而是在复杂群落背景下的系统级互作。一个孤立的生防菌株被投放到田间复杂土壤中,面对的不仅是靶标病原,还有成千上万的竞争者、掠食者和合作者。它需要成功定殖、获取营养、抵抗本土微生物的拮抗、与宿主免疫系统"谈判"——所有这些都发生在温度、湿度、pH、养分高度可变的环境中。
这一认识正在催生一场范式转变:从"单兵作战"的生防菌策略,转向"群落设计"的微生物组工程。本章将追溯这一转变的科学基础和实践进展——从合成群落(SynCom)的设计原则,到合成生物学驱动的工程菌株,再到田间尺度面临的现实障碍,最后讨论这条路线的伦理与监管前景。
15.1从单一菌株到合成群落(SynCom)
单一菌株生防的成功与局限
单一菌株生物防治并非完全失败——某些商业化产品在特定条件下表现出色。例如,Bacillus subtilis QST 713(商品名 Serenade)对多种叶部和土传病害的防效已在温室和部分田间条件下得到验证;Trichoderma harzianum T-22 在番茄根腐病的管理中积累了数十年的应用经验 (Harman et al., 2004)。这些成功案例的共同特征是:环境条件相对可控(温室、育苗基质)、靶标病原明确、施用方式可以保证高密度的局部接种。
但在大田开放环境中,单一菌株策略面临三重困境:
- 定殖衰减:接种的菌株在竞争激烈的根际环境中难以维持有效的种群密度。接种后数周内,菌量可下降2-3个数量级 (Lugtenberg & Kamilova, 2009)。
- 生态位限制:单一菌株的代谢和生态位能力有限,难以适应土壤类型、pH、温度、水分的广泛变异。一个在壤土中表现优异的菌株可能在砂土或黏土中完全失效。
- 功能单一:一个菌株通常只擅长一种保护机制——要么产生抗生素直接拮抗病原,要么诱导宿主 ISR,要么竞争营养位——而田间的有效保护往往需要多重机制同时运作 → 第10章 10.4节。
SynCom 的设计逻辑
合成群落(Synthetic Community, SynCom)策略试图克服上述局限:不是用一个"超级菌株"替代整个群落,而是用一组精心挑选的菌株模拟自然保护性微生物组的关键功能。
SynCom 的设计遵循三个核心原则:
- 功能互补:选择的菌株应覆盖多种保护机制——直接拮抗、ISR 诱导、营养竞争、生态位占领——而非重复同一种功能。Niu et al. (2017) 的玉米 SynCom 实验表明,功能多样性(而非物种多样性本身)是群落保护效果的最佳预测因子。
- 生态相容:菌株之间不应存在强烈的拮抗关系。理想情况下,它们应该能在根际形成稳定的共存格局——通过代谢互补(一个菌株的代谢产物是另一个的营养来源)或空间分隔(定殖于根表的不同微环境)实现。
- 宿主兼容:SynCom 成员应能通过宿主免疫系统的"安检"——即能够在根际/根内成功定殖而不触发过强的防御反应。这需要菌株具备适当的免疫调节能力 → 第10章 10.3节。
- 环境适应:群落的功能冗余设计确保即使某些成员在特定环境条件下表现不佳,其他成员可以"补位"——这是SynCom 相对于单一菌株的核心优势。
SynCom 成功案例
近年来,多个 SynCom 研究展示了群落策略的潜力:
- 玉米7株最小群落:Niu et al. (2017) 从玉米根际分离的数百个菌株中筛选出7株核心细菌,构成一个最小功能群落。去除其中任何一个成员都会显著削弱群落对Fusarium verticillioides 的抑制效果,表明群落成员间存在不可替代的协同功能。
- 拟南芥根内细菌群落:Durán et al. (2018) 构建了包含细菌、真菌和卵菌的三界 SynCom,发现细菌群落能有效限制潜在致病性真菌和卵菌的过度增殖——保护功能不是来自直接抗菌活性,而是来自群落结构的生态约束 → 第10章 10.5节。
- 抑病性土壤的 SynCom 模拟:Berendsen et al. (2018) 从"教导性土壤"中鉴定出3株关键保护性细菌,将它们组合接种后能部分重现土壤记忆效应——这为将自然抑病现象"工程化"提供了概念验证。
图 15.1 从单一生防菌到可定制微生物组工程。SynCom 提供了群落级功能互补,宿主分泌物和益生元策略则尝试调动本土群落;田间应用需要把土壤诊断、标准菌株库和算法配方结合起来。
15.2微生物组工程的策略与挑战
除了直接接种 SynCom,微生物组工程还包括一系列通过间接手段调控根际群落的策略。这些策略可以大致分为两大类:"播种"策略(直接引入目标微生物)和"调控"策略(通过改变环境或宿主来定向重塑本土群落)。
宿主遗传学驱动的群落调控
第10章的讨论已经表明,宿主基因型——特别是根分泌物组成和免疫信号通路——是微生物组组成的重要决定因子。这一认识开辟了一条全新的育种思路:通过选育特定的宿主等位基因来"从内部"优化微生物组。
- 根分泌物工程:通过遗传改造或等位基因选择,改变根系分泌的有机酸、香豆素或次生代谢物的组成,从而选择性地富集有益微生物。例如,Stringlis et al. (2018) 的工作暗示,增强 MYB72-香豆素通路可能同时增强铁吸收和有益微生物的招募 → 第10章 10.6节。
- 免疫信号微调:Lebeis et al. (2015) 的发现——SA 信号影响根际群落组成——提示通过调节免疫信号的基线水平可以间接优化微生物组。但这需要极其精细的调控:SA 过高会排斥有益微生物,SA 过低则会失去对机会致病菌的控制。
土壤管理与群落调控
农业管理措施本身就是微生物组的强力调控手段:
- 轮作:不同作物的根分泌物交替施加不同的选择压力,防止单一病原群落的过度富集。轮作是最古老也可能是最有效的"微生物组管理"手段。
- 有机质添加:堆肥和生物炭的施用改变土壤碳质量和物理结构,间接影响微生物群落的组成和功能。Bonanomi et al. (2010) 的荟萃分析表明,有机质添加对土传病害的抑制效果高度依赖于有机质的分解阶段——新鲜有机质有时反而促进病害。
- 覆盖作物和间作:不同植物物种共存时,其根际群落会发生复杂的互作和重组,可能产生对病害有益的"邻居效应"。
益生元策略
借鉴人类肠道微生物组领域的概念,"植物益生元"(plant prebiotics)策略旨在通过施加特定化学物质来选择性促进有益微生物的增殖,而非直接接种微生物。这种方法的优势在于:化学物质比活体微生物更容易标准化生产、储存和施用。潜在的"益生元"包括特定的有机酸、氨基酸、以及合成的信号分子类似物 (Vorholt et al., 2017)。
近两年的实证研究让益生元策略更具体。Wu et al. (2025) 表明,荞麦黄酮可在土壤中留下有益的微生物组遗产,增强后茬作物抗根肿病能力;Zeng et al. (2026) 则把水稻对稻瘟病的感知、十七烷酸分泌和 Bacillus 招募串成一条可干预的防御通路。对于工程应用来说,这类工作提示我们可以不只“添加菌株”,还可以“设计宿主分泌物或轮作化学环境”,让本土群落自己向抑病方向重排。
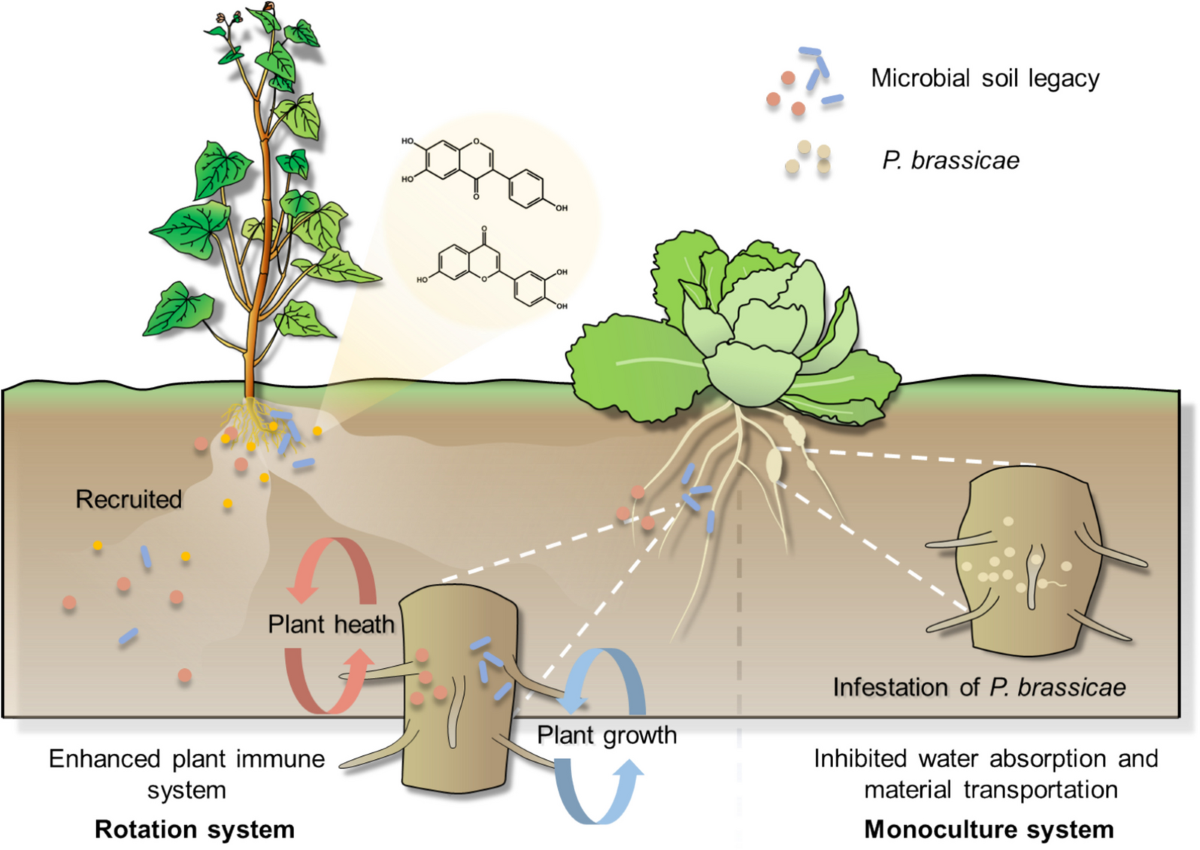
图 15.2 论文原图:轮作化学环境作为微生物组工程入口。原图为 Wu et al. (2025) Microbiome Fig. 7,DOI: 10.1186/s40168-025-02166-y。这里强调其转化含义:宿主代谢物和轮作制度可被视为调动本土有益群落的工程化手段。依据 CC BY-NC-ND 4.0 原样复用;图片未作裁剪、改色或内容改动。
15.3合成生物学与工程菌株
合成生物学为生物防治提供了一套全新的工具箱:不是在自然界中寻找功能合适的菌株,而是在分子水平重新设计微生物的功能。
基因回路设计
合成生物学的核心理念是将复杂的生物功能分解为可预测、可组合的"基因模块"。应用于生物防治的设计方向包括:
- 条件性抗菌物产生:在工程菌株中构建基因回路,使其仅在检测到病原信号分子(如病原的群体感应信号 AHL 或特定毒素)时才启动抗菌物合成——这种"智能"设计避免了抗菌物的持续生产所带来的代谢负担和对非靶标微生物的影响 (Geddes et al., 2019)。
- 增强定殖能力:通过导入高效的碳源利用基因、根表黏附因子或胁迫耐受基因,增强工程菌株在根际的竞争力。
- 多功能集成:将直接拮抗、ISR 诱导和营养促进等功能模块整合到同一底盘微生物中,创造"多功能生防菌"。
底盘微生物的选择
工程菌株的"底盘"选择至关重要。理想的底盘应具备:(1)天然的根际定殖能力;(2)遗传操作工具成熟;(3)已有安全性评估数据;(4)能够通过宿主免疫系统的"安检"。目前,Pseudomonas fluorescens、Bacillus subtilis和某些Rhizobium物种是最常用的底盘。但一个矛盾是:最容易操作的模式菌株(如E. coli)往往不是好的根际定殖者,而最好的根际定殖者(如某些 Burkholderiaceae)的遗传工具还不完善。
CRISPR 和 RNAi 介导的病原抑制
一个日益受到关注的方向是将 RNA 干扰技术与微生物载体结合。工程细菌可以被设计为在根际持续产生靶向病原关键基因的 dsRNA——这些 dsRNA 被病原吸收后触发 RNAi 沉默,抑制其生长或毒力 → 第13章 13.4节。Huang et al. (2022) 已经在实验室条件下验证了这一概念的可行性。然而,dsRNA 在土壤中的稳定性、跨界传递效率和靶标特异性仍是待解决的关键问题。
15.4田间尺度的挑战:实验室结果为何往往"缩水"
从实验室到田间的"可翻译性鸿沟"(translational gap)是微生物组工程面临的最大现实障碍。理解这一鸿沟的来源是弥合它的前提。
规模效应
实验室中的 SynCom 实验通常在灭菌或限菌基质中进行——这消除了本土微生物的竞争,为接种菌提供了一个"空白生态位"。但在田间自然土壤中,每克土壤已经包含10⁸-10⁹个微生物细胞和数千个物种——接种菌必须在这个已经饱和的群落中争得一席之地。这就是所谓的"竞争排斥"问题:一个功能上完美的 SynCom 可能因为无法在本土群落中建立种群而完全失效 (Kaminsky et al., 2019)。
环境异质性
田间环境在空间和时间上的异质性远超实验室条件。同一块田地的不同位置可能存在土壤质地、水分含量、有机质含量和 pH 的显著差异——而这些参数中的每一个都会影响微生物的存活和活性。一个在 pH 6.5-7.0 的壤土中表现优异的 SynCom 可能在 pH 5.0 的酸性砂土中完全失去功能。
时间动态
微生物组的组成和功能不是静态的,而是随季节、作物生长阶段和天气事件不断变化。接种的微生物能否在整个生长季中维持有效种群?还是需要在关键时间点多次施用?目前大多数研究只追踪了接种后数周内的动态,对于生长季尺度甚至跨年尺度的持久性知之甚少。
作物-病原-微生物组的三方互作
实验室研究通常简化为"植物 + SynCom + 单一病原"的三方系统。但田间的植物同时面对多种病原、昆虫和非生物胁迫——一个 SynCom 可能在抑制Fusarium根腐的同时意外增加叶部细菌病害的易感性。这种"跷跷板效应"反映了免疫-激素网络的内在权衡 → 第5章 5.3节、→ 第11章。
微生物组工程是否需要"因地制宜"——不同土壤、不同气候需要不同的方案?
如果答案是"是",那么微生物组工程的产业化模式可能不是生产一种通用产品,而是建立一套"诊断-设计-定制"的服务体系——先分析目标田块的土壤微生物组基线和环境参数,然后从标准化的菌株库中选择最适合的组合。这类似于精准医学中"基于个体基因组的个性化用药"理念——但面对的复杂性可能更高,因为每一块田地的"微生物组基因组"都是独特的 → 第12章 12.4节。
15.5伦理、监管与产业化
微生物组工程的快速发展也带来了监管和伦理方面的新问题:
- 基因工程微生物(GEM)的环境释放:工程菌株在田间释放后的扩散、基因水平转移和生态后果是监管的核心关切。与转基因作物不同,微生物的扩散和进化速度更快,"召回"几乎不可能。目前各国的监管框架对 GEM 环境释放有严格限制,这在很大程度上限制了合成生物学策略的田间验证。
- 非 GEM 策略的监管灰区:天然菌株的 SynCom 组合不涉及基因工程,但其监管框架尚不明确——是作为"微生物肥料"还是"生物农药"注册?不同国家的分类标准差异很大。
- 知识产权与公共利益:微生物组工程涉及菌株专利、群落配方知识产权和田间数据所有权等问题。如何在保护创新激励的同时确保小农群体的可及性,是一个尚需深入讨论的公平问题。
- 生态安全评估:大规模改变农田微生物组组成是否会产生不可预见的生态后果?例如,一个经过优化的根际微生物组是否会向周围非农生态系统扩散,影响本土植物-微生物互作?目前的风险评估框架主要针对单一生物体,尚缺乏评估"群落级干预"的生态后果的成熟方法论 → 第10章 10.8节。
15.6里程碑研究思路拆解
里程碑 1:Niu et al. (2017) — 最小合成群落的设计与验证
面对的问题:自然微生物组中哪些成员是保护功能的"必要且充分"组分?能否用最少的菌株重建群落保护功能?
关键思路:从玉米根际分离大量培养菌株,通过系统的组合实验(加一株/减一株设计)筛选出最小功能群落。
关键证据链:(1)7株细菌组成的 SynCom 能在无菌基质中有效抑制Fusarium verticillioides;(2)去除任一成员显著削弱保护效果,表明功能不可冗余;(3)群落的保护效果优于任何单一菌株。
影响:为"最小群落"设计提供了方法论范式,证明群落的协同功能不可还原为个体功能的简单加和。
里程碑 2:Carlström et al. (2019) — SynCom 组装规则的系统解析
面对的问题:合成群落的组装是否遵循可预测的规则?菌株间的相互作用如何影响群落最终结构?
关键思路:构建包含拟南芥根际细菌的大规模 SynCom 实验矩阵,系统比较成对互作和群落组装结果。
关键证据链:(1)体外成对互作实验的结果无法可靠预测群落中的菌株丰度——群落行为是涌现性质;(2)宿主存在时的群落组装比无宿主时更具确定性,暗示宿主是群落的"稳定器";(3)竞争排斥在群落水平被缓冲——单独培养时互相拮抗的菌株在群落中可以共存。
影响:揭示了 SynCom 设计不能仅基于成对兼容性测试,需要群落水平的实验验证。同时提示宿主在群落工程中不是被动的"花盆",而是主动的组装调控者。
15.7当前争论与未解问题
- SynCom 的最优复杂度是多少?太简单的群落可能缺乏足够的功能冗余和生态稳定性;太复杂的群落又难以标准化生产和质量控制。"甜蜜点"可能因作物、病害和环境而异,但目前缺乏系统的比较研究。
- 实验室-田间可翻译性的瓶颈能否被预测和克服?是否存在一组可量化的环境参数(如土壤 pH、有机碳含量、本底群落多样性)可以预测特定 SynCom 在给定田块中的成功概率?建立这样的预测模型需要大量的多地点田间试验数据。
- 工程菌株与天然 SynCom 的战略选择?工程菌株在功能上更可控但面临严格的监管限制;天然 SynCom 更易被接受但功能优化空间有限。未来的主流路线是哪一个,还是两者的混合策略?
- 微生物组工程的长期稳定性如何保障?接种的微生物能否在多个生长季中维持有效种群?微生物的快速进化是否会导致保护功能随时间漂移或丧失?
- 跨作物迁移性的边界在哪里?一个在拟南芥中验证的 SynCom 设计原则,在水稻、小麦或番茄中是否适用?不同作物的根分泌物和免疫信号差异如何影响 SynCom 的宿主兼容性?
近年的定量化框架提示,微生物组工程不应只追求“接种后是否提高抗性”的单点答案,而应建立可预测的病害结局模型:宿主基因型、土壤本底群落、病原压力、气候因子和接种群落之间存在高阶互作 (Niu & Kolter, 2024)。这对产业化很关键:如果某个 SynCom 在 A 地块有效、在 B 地块失效,失败原因可能不是菌株本身“无效”,而是缺少与本底群落和环境状态匹配的生态位。未来更可行的路线可能是“标准菌株库 + 田块诊断 + 算法配方”,而不是单一产品打天下。
15.8关键实验方法
| 实验方法 | 用途 | 经典文献 |
|---|---|---|
| 无菌/限菌 SynCom 重建 | 在受控条件下验证合成群落的功能 | Niu et al., 2017, PNAS |
| 加一/减一组合设计 | 鉴定群落中不可替代的关键成员 | Niu et al., 2017, PNAS |
| 宏基因组/宏转录组 | 解析自然群落的功能潜力与实际活性 | Trivedi et al., 2020, Nat Rev Microbiol |
| 稳定同位素探针(SIP) | 追踪根分泌物碳在微生物群落中的流动 | Zhalnina et al., 2018, Nat Microbiol |
| 多地点田间验证试验 | 评估 SynCom 在真实环境下的表现 | Finkel et al., 2017, Annu Rev Phytopathol |
15.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
15.10参考文献
- Berendsen RL, Vismans G, Yu K, et al. Disease-induced assemblage of a plant-beneficial bacterial consortium. ISME J, 2018, 12: 1496–1507.
- Bonanomi G, Antignani V, Pane C, Scala F. Suppression of soilborne fungal diseases with organic amendments. J Plant Pathol, 2007, 89: 311–324.
- Carlström CI, Field CM, Bortfeld-Miller M, et al. Synthetic microbiota reveal priority effects and keystone strains in the Arabidopsis phyllosphere. Nat Ecol Evol, 2019, 3: 1445–1454.
- Durán P, Thiergart T, Garrido-Oter R, et al. Microbial interkingdom interactions in roots promote Arabidopsis survival. Cell, 2018, 175: 973–983.
- Finkel OM, Castrillo G, Herrera Paredes S, et al. Understanding and exploiting plant beneficial microbes. Curr Opin Plant Biol, 2017, 38: 155–163.
- Geddes BA, Paramasivan P, Jez JM, et al. Engineering transkingdom signalling in plants to control gene expression in rhizosphere bacteria. Nat Commun, 2019, 10: 3430.
- Harman GE, Howell CR, Viterbo A, et al. Trichoderma species—opportunistic, avirulent plant symbionts. Nat Rev Microbiol, 2004, 2: 43–56.
- Kaminsky LM, Trexler RV, Malik RJ, et al. The inherent conflicts in developing soil microbial inoculants. Trends Biotechnol, 2019, 37: 140–151.
- Lebeis SL, Paredes SH, Lundberg DS, et al. Salicylic acid modulates colonization of the root microbiome by specific bacterial taxa. Science, 2015, 349: 860–864.
- Lugtenberg B, Kamilova F. Plant-growth-promoting rhizobacteria. Annu Rev Microbiol, 2009, 63: 541–556.
- Niu B, Paulson JN, Zheng X, Kolter R. Simplified and representative bacterial community of maize roots. Proc Natl Acad Sci USA, 2017, 114: E2450–E2459.
- Niu B, Kolter R. Quantifying host-microbiota interactions in plant disease outcomes. Annu Rev Phytopathol, 2024, 62: 273–294. DOI: 10.1146/annurev-phyto-021622-103318.
- Stringlis IA, Yu K, Feussner K, et al. MYB72-dependent coumarin exudation shapes root microbiome assembly to promote plant health. Proc Natl Acad Sci USA, 2018, 115: E5213–E5222.
- Trivedi P, Leach JE, Tringe SG, et al. Plant–microbiome interactions: from community assembly to plant health. Nat Rev Microbiol, 2020, 18: 607–621.
- Vorholt JA, Vogel C, Carlström CI, Müller DB. Establishing causality: opportunities of synthetic communities for plant microbiome research. Cell Host Microbe, 2017, 22: 142–155.
- Wu J, Hu S, Chen J, et al. Soil microbial legacy mediated by buckwheat flavonoids enhances cabbage resistance to clubroot disease. Microbiome, 2025, 13: 176. DOI: 10.1186/s40168-025-02166-y.
- Zeng J, Wen T, Zhao J, et al. Rice roots recruit Bacillus via the secretion of heptadecanoic acid. Nat Plants, 2026. DOI: 10.1038/s41477-026-01965-x.
- Zhalnina K, Louie KB, Hao Z, et al. Dynamic root exudate chemistry and microbial substrate preferences drive patterns in rhizosphere microbial community assembly. Nat Microbiol, 2018, 3: 470–480.