免疫的进化
免疫系统是进化的产物。理解它的进化逻辑,才能真正理解它的设计原理
本章目录
- NLR 的起源与多样化
- PRR 的保守性与变异性
- "军备竞赛"的分子证据
- 免疫的进化代价:自身免疫、适应度惩罚与 trade-off
- 跨物种比较:植物免疫与动物免疫的进化趋同
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
植物免疫系统不是被"设计"出来的,而是在亿万年的共进化压力下被"雕刻"出来的。理解这个雕刻过程——即免疫的进化——不仅是学术兴趣,更是将基础研究转化为育种策略的关键。因为一个不理解进化逻辑的改良方案,注定会被进化本身所颠覆。
本章将从三个维度审视免疫的进化:变异的来源(免疫基因如何产生新的多样性)、选择的机制(什么样的进化压力塑造了我们今天看到的免疫系统)、以及进化的代价(为什么免疫系统不能无限增强)。我们还将把植物免疫放入更广阔的比较生物学视野中,探讨植物与动物免疫之间令人惊讶的进化趋同。
6.1NLR 的起源与多样化
NLR 的古老起源
NLR 蛋白并非植物的"发明"。具有 NB-ARC 结构域的蛋白广泛存在于真核生物中——从动物的 APAF-1 和 NLR 家族(如 NLRP3 炎性小体),到植物的抗病 NLR,再到真菌和细菌中的同源蛋白。这些蛋白共同的特征是:通过核苷酸结合和水解驱动分子开关,控制蛋白-蛋白互作和下游信号。NB-ARC 结构域的起源可以追溯到真核生物的最后共同祖先(Last Eukaryotic Common Ancestor, LECA),甚至可能更早 (Urbach & Ausubel, 2017)。
然而,植物 NLR 的特殊之处在于其爆炸性多样化。拟南芥 Col-0 基因组编码约150个 NLR 基因,水稻约480个,某些野生植物物种超过1000个。相比之下,人类基因组仅编码约23个 NLR。这种数量上的巨大差异反映了一个根本的进化约束:植物没有适应性免疫系统(没有体细胞重组或克隆选择机制),因此必须依赖种系编码(germline-encoded)的受体库来应对效应蛋白的多样性 (Jacob et al., 2013)。
NLR 多样化的分子机制
NLR 基因的快速多样化依赖于几种关键的基因组机制:
- 串联重复与不等交换:大多数 NLR 基因以基因簇(cluster)形式存在于基因组中——拟南芥约65%的 NLR 位于复杂基因簇内。基因簇内的不等交换(unequal crossing-over)可以快速产生新的 NLR 嵌合体(chimera),具有新的识别特异性 (Michelmore & Meyers, 1998)。
- LRR 域的高变异率:NLR 的 LRR 域(决定识别特异性的关键区域)表现出显著高于基因组平均水平的非同义突变率(dN/dS > 1),表明该区域处于正选择(positive selection)——即有利于产生新变异的选择压力 (Mondragón-Palomino et al., 2002)。
- 整合域的获取:如第4章讨论的,NLR 可以通过基因重排将效应蛋白靶标的结构域整合到自身中,创造全新的识别能力 → 第4章 4.6节。整合域的多样性(超过50种类型)说明这种获取机制在进化中反复独立发生 (Kroj et al., 2016)。
- "出生-死亡"模型:Michelmore & Meyers (1998) 提出 NLR 基因家族遵循"出生-死亡"(birth-and-death)进化模型——新基因通过复制"出生",失去功能的拷贝通过假基因化"死亡"。在这个模型下,NLR 基因家族的大小在进化中高度动态,不同谱系的扩张和收缩模式各不相同。
Pan-NLRome:物种 NLR 多样性的全景
单一参考基因组无法代表一个物种的完整 NLR 多样性。Van de Weyer et al. (2019) 对拟南芥64个自然群体(accessions)进行了系统的 NLR 基因清点(pan-NLRome),发现惊人的多样性:
- 参考基因组 Col-0 的约150个 NLR 只是物种总 NLR 库的一小部分;考虑所有等位变异和存在/缺失变异(PAV),物种水平的 NLR 库远大于任何单一基因组。
- NLR 基因的存在/缺失变异(PAV)非常普遍——许多 NLR 在一些群体中存在而在另一些中完全缺失。
- 即使在共享的 NLR 基因中,等位多样性也极高,LRR 域的变异尤为突出。
这些发现具有重要的育种学启示:传统育种中使用的参考基因组可能遗漏了大量有价值的抗性变异。充分利用野生群体和近缘种的 NLR 多样性,是扩展作物抗性的一个重要但尚未充分开发的资源 → 第14章。
6.2PRR 的保守性与变异性
与 NLR 的极端多样化形成鲜明对比的是,PRR 在进化上相对保守。FLS2 在大多数被子植物中都存在同源物;EFR 虽然局限于十字花科,但其信号通路组分(BAK1、BIK1、RBOHD 等)在植物界广泛保守 (Zipfel, 2014)。
为什么 PRR 比 NLR 保守?
这种差异的进化解释与两类受体识别靶标的性质有关:
- PRR 靶标(PAMP)受功能约束:flg22 是细菌鞭毛蛋白的保守片段,鞭毛的运动功能限制了该区域的变异自由度。同理,几丁质是真菌细胞壁的必需组分,EF-Tu 是翻译的核心因子。这些靶标的高度保守性意味着病原很难通过简单突变来逃避 PRR 识别。
- NLR 靶标(效应蛋白)缺乏功能约束:效应蛋白虽然对毒力很重要,但大多数可以被丢弃或替代——病原可以通过获取新的效应蛋白来补偿丢失旧的。这种"可丢弃性"使得效应蛋白可以快速进化以逃避 NLR 识别。
然而,PRR 也并非完全不变。最近的群体遗传学研究发现,FLS2 在自然群体中存在影响 flg22 敏感性的功能变异——一些拟南芥群体的 FLS2 对 flg22 反应减弱,可能是因为这些群体所处的环境中细菌压力较低,维持高灵敏度 FLS2 的选择优势减弱 (Vetter et al., 2012)。这提示我们:即使是保守的 PRR,其维持也是有代价的,在没有病原压力的环境中可能被弱化。
PRR 跨物种转移的进化启示
PRR 的相对保守性使其成为跨物种免疫工程的理想候选。Lacombe et al. (2010) 将拟南芥的 EFR 转入番茄和烟草,成功赋予了这些物种对 EF-Tu 的识别能力和增强的抗菌性。这一成功背后的进化逻辑是:EFR 的下游信号通路组分(BAK1、BIK1 等)在番茄中高度保守,因此跨物种转移的"信号接驳"问题可以被自然解决 → 第14章。
图 6.1 NLR 与 PRR 进化速率的对比及其进化解释。PRR 识别的 PAMP 通常承担微生物基本功能,因此变异空间小;NLR 识别或监测的效应蛋白更容易丢失、替换或突变,推动 NLR 基因簇通过复制、重组和正选择快速多样化。
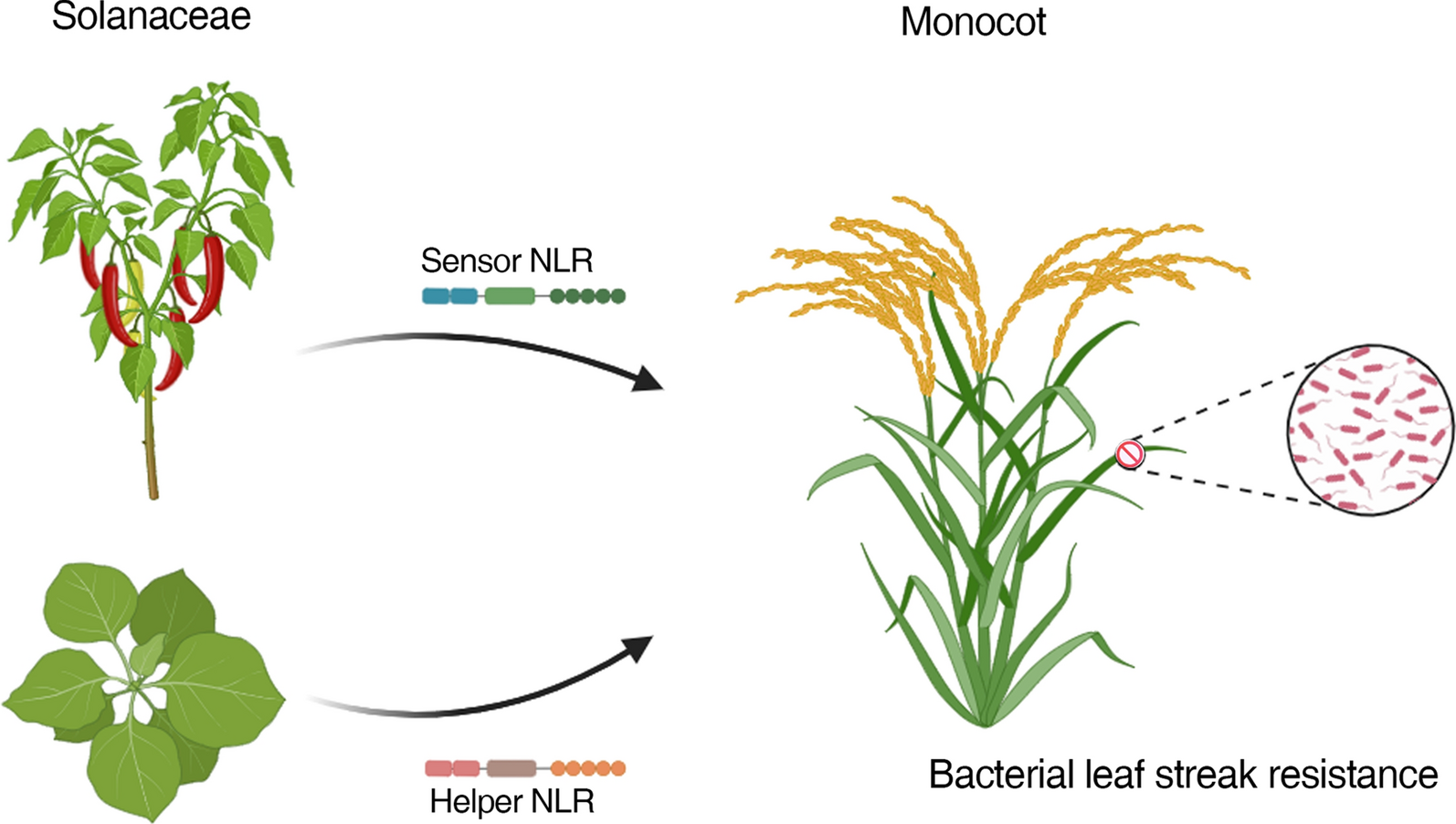
图 6.P1 论文原图:从 NLR 功能机制到抗性工程应用。原图为 Peng (2025) Phytopathology Research Fig. 1,DOI: 10.1186/s42483-025-00387-5。该图把 NLR 功能机制、抗性资源挖掘和工程化部署联系起来,适合作为 NLR 进化与转化应用之间的桥梁。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
6.3"军备竞赛"的分子证据
植物与病原之间的共进化常被比喻为"军备竞赛"(arms race)。但这不仅是一个修辞,而是有扎实的分子证据支持的进化过程。
效应蛋白的进化逃逸
病原逃避 NLR 识别的策略包括:
- 效应蛋白丢失或假基因化:当一个效应蛋白被宿主 NLR 识别后,携带该效应蛋白的病原个体被选择淘汰。如果该效应蛋白不是毒力所必需的,种群中丢失该基因的个体就具有选择优势。例如,P. syringae 的 AvrRpt2 在面对携带 RPS2 的拟南芥群体时,频率显著降低 (Guttman et al., 2014)。
- 效应蛋白的点突变:在保持毒力功能的前提下,效应蛋白表面残基的突变可以逃避 NLR 识别。稻瘟菌的 AVR-Pik 效应蛋白存在多个等位变异(PikA-PikE),不同变异对不同 Pik NLR 等位具有差异性逃逸能力 (Kanzaki et al., 2012)。
- 新效应蛋白的水平获取:通过质粒、噬菌体或转座子介导的水平基因转移,病原可以快速获取全新的效应蛋白库。P. syringae 的 T3SS 效应蛋白组中有相当比例被认为来自水平转移 (McCann & Guttman, 2008)。
平衡选择与频率依赖动力学
军备竞赛并不总是单向的"升级"。在自然群体中,NLR 等位多样性的维持常常遵循负频率依赖选择(negative frequency-dependent selection)的逻辑:当某个 R 等位在群体中频率很高时,能逃避该 R 等位识别的病原菌株获得选择优势并扩张;随着逃逸型病原频率升高,携带该 R 等位的宿主失去选择优势,其他 R 等位开始被偏好。这种动态维持了群体中多个 R 等位的长期共存 (Stahl et al., 1999; Bergelson et al., 2001)。
拟南芥 RPM1 位点是平衡选择的经典案例。群体遗传学分析发现,RPM1 基因在拟南芥自然群体中呈现典型的存在/缺失多态性(PAV)——约半数群体携带功能性 RPM1,另一半携带缺失等位。这种多态性已维持数百万年,远超中性预期的等位存留时间,暗示存在强烈的平衡选择 (Stahl et al., 1999; Tian et al., 2003)。
"Trench warfare"模型
Stahl et al. (1999) 提出了"堑壕战"(trench warfare)模型来区别于经典军备竞赛模型:在军备竞赛中,新的 R 和 Avr 等位不断被创造和淘汰(前进的战线);而在堑壕战中,同一组 R 等位在群体中长期波动但不被彻底淘汰——战线几乎不移动,但局部战斗从未停止。RPM1 的 PAV 多态性更符合堑壕战模型。
两种模型可能同时作用于不同的基因位点:快速进化的 NLR 基因簇可能遵循军备竞赛逻辑,而功能上不可替代的 NLR 则可能表现为堑壕战动态。
6.4免疫的进化代价:自身免疫、适应度惩罚与 trade-off
如果更多的 NLR 意味着更好的保护,为什么植物没有无限扩展其 NLR 库?答案在于免疫是有代价的——这些代价在多个层面限制了免疫系统的进化扩张。
自身免疫(Autoimmunity):NLR 误激活的风险
NLR 蛋白处于精密的自抑制状态,但自抑制机制并非万无一失。当不同的 NLR 等位在杂交后代中组合时,可能产生杂种坏死(hybrid necrosis)——两个在各自遗传背景中功能正常的 NLR 等位,在新组合中相互激活,导致无病原条件下的组成性免疫激活和生长严重抑制 (Bomblies et al., 2007)。
拟南芥中最经典的案例是 DM1/DM2 不兼容位点(由 Bomblies 等人发现):某些群体间杂交产生的 F1 后代在温度升高时出现严重的矮化和坏死表型。遗传分析发现这是由两个独立的 NLR 基因座的特定等位组合引起的——每个等位单独存在时功能正常,但两者组合时一个 NLR 的产物恰好被另一个 NLR "识别"为危险信号,触发自身免疫反应。
杂种坏死不是实验室产物——它在自然群体和育种程序中都有报道。在小麦中,Ne1 和 Ne2 基因互作引起的杂种坏死是阻碍某些杂交组合的已知育种障碍 (Bomblies & Weigel, 2007)。这种现象的进化意义是深刻的:NLR 库的扩展受到遗传兼容性的限制——不是所有 NLR 组合都能和平共处。
适应度惩罚:抗性的代价
即使没有自身免疫,携带功能性 R 基因本身也可能有代价。在没有病原压力的条件下,携带 RPM1 的拟南芥群体比缺失 RPM1 的群体产生更少的种子——这是在竞争性种植实验中直接测量到的适应度代价 (Tian et al., 2003)。
这种代价可能来源于:
- NLR 蛋白本身的代谢成本:维持大量 NLR 蛋白的表达和折叠质控需要能量和氨基酸投入。
- 低水平的组成性免疫激活:即使处于自抑制状态,NLR 可能存在微弱的基础活性,消耗防御资源。
- 与其他遗传因子的拮抗效应:NLR 基因簇的扩展可能影响邻近基因的表达或功能。
生长-防御权衡的进化根源
更广泛地说,免疫系统的进化代价是"生长-防御权衡"(growth-defense trade-off)在进化时间尺度上的体现。在资源有限的条件下,投入免疫的资源就不能投入生长和繁殖——自然选择在两者之间寻找最优平衡点,而这个平衡点取决于环境中病原压力的强度和变异 → 第9章。
6.5跨物种比较:植物免疫与动物免疫的进化趋同
植物和动物在超过15亿年前分离,各自独立进化出了免疫系统。然而,两者之间存在令人惊讶的功能趋同——不是因为共同祖先,而是因为面对相似的进化压力(微生物入侵)时,自然选择趋向于相似的解决方案。
结构层面的趋同
| 功能模块 | 植物 | 动物 | 趋同本质 |
|---|---|---|---|
| 表面模式识别 | PRR(RLK/RLP) | TLR, Dectin-1 | LRR 域识别保守模式 |
| 胞内受体 | NLR(NB-ARC-LRR) | NLR(NACHT-LRR) | 核苷酸结合开关 + LRR 识别 |
| 寡聚化信号复合体 | Resistosome | Inflammasome / Apoptosome | 激活态寡聚体驱动效应 |
| 成孔细胞死亡 | ZAR1 CC 域 | Gasdermin | 膜孔道触发炎性/免疫性死亡 |
| NADase 信号 | TIR 域 | SARM1 TIR 域 | NAD⁺ 切割产生小分子信号 |
特别值得注意的是 TIR 域的 NADase 活性——植物 TNL 的 TIR 域和动物 SARM1 的 TIR 域独立进化出了相同的酶学功能。这种酶学趋同暗示 NAD⁺ 代谢可能是一个特别适合作为"危险信号"的生化通路——NAD⁺ 的耗竭本身就足以触发细胞代谢崩溃和死亡 (Essuman et al., 2018; Horsefield et al., 2019) → 第4章 4.5节。
系统层面的差异
尽管存在惊人的趋同,植物和动物免疫系统之间的差异同样深刻:
- 无适应性免疫:植物没有发展出类似 T/B 细胞的体细胞重组和克隆选择系统。植物用大量种系编码的受体来补偿这一"缺失"。
- 无专职免疫细胞:植物的每个细胞都是"免疫战士",没有循环的免疫细胞系统 → 第1章 1.4节。
- 免疫记忆的不同实现:动物通过记忆 T/B 细胞实现高度特异性的免疫记忆;植物通过表观遗传修饰和代谢物积累实现非特异性的 priming/SAR——"记住"的不是具体的病原,而是"曾经遭受过攻击"这个状态 → 第11章。
植物-动物免疫的比较不仅是学术上的智力享受,还有实际价值。gasdermin 成孔机制在动物中的发现启发了对植物 NLR 成孔功能的搜索,最终导致了 ZAR1 抗病小体的突破。反过来,植物 TIR 域 NADase 的发现也为理解动物 SARM1 的功能提供了关键线索。跨界比较免疫学正在成为一个越来越有生产力的研究策略。
NLR 多样性是否存在进化上限?如果存在,是什么决定了这个上限?
理论上,NLR 库越大,识别的效应蛋白越多,抗性越广谱。但实际观察到的 NLR 数量存在一个"天花板"——即使在 NLR 库最大的物种中也很少超过2000个。限制因素可能包括:(1)自身免疫风险随 NLR 数量增加而加速上升(组合爆炸问题);(2)NLR 蛋白质控的代谢成本;(3)基因组物理空间的限制。理解这个上限对于设计"最优 NLR 组合"的育种策略至关重要——增加 NLR 数量不是无限可行的,关键是选择正确的 NLR 组合 → 第14章。
6.6里程碑研究思路拆解
里程碑 1:Van de Weyer et al. (2019) — 拟南芥 pan-NLRome
面对的问题:单一参考基因组能代表物种的真实免疫多样性吗?已知 NLR 基因在群体间差异很大,但缺乏系统性的物种水平清点。
关键思路:利用长读长测序(PacBio)和定制的 NLR 注释管线(NLR-Annotator),对64个拟南芥自然群体进行全面的 NLR 基因清点和比较分析。
关键证据链:(1)发现大量参考基因组中不可见的 NLR 等位和基因(PAV 变异普遍);(2)LRR 域变异最高,NB-ARC 域相对保守;(3)部分 NLR 的 PAV 与已知抗性表型关联;(4)NLR 基因簇区域的重组率显著高于基因组平均。
影响:推动 NLR 研究从"单基因/单等位"进入"群体系统"层面,为挖掘野生群体中的新抗性资源提供了路线图。
里程碑 2:Stahl et al. (1999) — RPM1 位点的平衡选择
面对的问题:R 基因在自然群体中的进化动态是什么?是快速替换(arms race)还是长期波动(trench warfare)?
关键思路:分析 RPM1 基因座在拟南芥自然群体中的多态性模式。如果军备竞赛主导,应该看到新等位不断替换旧等位(低多态性、频繁选择性清除);如果平衡选择主导,应该看到多个等位长期共存(高多态性、中间频率等位)。
关键证据链:(1)RPM1 在自然群体中表现为二态分布——功能性等位和缺失等位各占约50%;(2)两种等位周围的序列分化时间远超物种分化时间,暗示多态性已维持数百万年;(3)该模式最符合负频率依赖选择(堑壕战模型)。
影响:首次在 R 基因位点提供了平衡选择的明确证据,建立了"堑壕战"模型作为军备竞赛的替代性进化框架。
里程碑 3:Bomblies et al. (2007) — NLR 介导的杂种坏死
面对的问题:为什么某些拟南芥群体间杂交的后代表现出严重的矮化和坏死?这种"杂种不兼容性"的分子基础是什么?
关键思路:通过遗传定位发现不兼容性由两个基因座的特定等位组合引起,其中至少一个编码 NLR 蛋白。由此提出:NLR 蛋白的多样化不仅受病原驱动,还受到遗传兼容性的约束——不同 NLR 等位在新遗传背景中可能被误激活。
关键证据链:(1)遗传定位到 DM1(编码 NLR)和 DM2 两个基因座;(2)不兼容表型为温度依赖的组成性免疫激活;(3)免疫信号通路突变(如 eds1)可抑制坏死表型。
影响:揭示了 NLR 进化的内在代价——自身免疫风险——为理解 NLR 库大小的进化限制提供了分子基础。对育种实践也有直接启示:堆叠 R 基因时必须考虑等位间的兼容性。
6.7当前争论与未解问题
- 哪些 NLR 变异最具转化价值?pan-NLRome 揭示了海量的 NLR 多样性,但如何从中筛选出对育种最有价值的等位?需要建立"NLR 变异→效应蛋白识别谱→田间抗性"的预测管线。
- 如何预测 R 基因部署后的突破风险?历史上,单基因 R 基因的大面积部署往往在3-5年内被病原突破。能否通过病原群体的效应蛋白组监测和进化模拟,预测特定 R 基因的"预期寿命"? (McDonald & Linde, 2002)
- Helper NLR 的保守性是否限制了识别端的扩展?sensor NLR 可以快速多样化,但如果所有 sensor 都依赖少数保守的 helper NLR(如 NRG1/ADR1/NRC),helper 的"带宽"可能成为瓶颈。
- 能否建立跨物种的免疫模块迁移规则?PRR 的跨物种转移已有成功案例,但 NLR 的跨物种转移成功率低得多——主要因为 sensor-helper 配对的物种特异性。如何克服这一障碍?
- 驯化对免疫多样性的影响有多大?作物驯化过程中的遗传瓶颈是否显著减少了 NLR 多样性?如果是,野生近缘种中"遗失的多样性"有多少可以被重新利用?
6.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| Pan-NLRome 构建(RenSeq / NLR-Annotator) | 利用靶向捕获测序(RenSeq)或全基因组 NLR 注释管线,在群体水平系统清点 NLR 基因及其等位变异。 | 长读长测序(PacBio/Nanopore)对 NLR 基因簇的组装至关重要;短读长可能错误折叠重复区域。需要专用的 NLR 结构域注释工具。 | Van de Weyer et al., 2019, Cell; Steuernagel et al., 2020, Plant Physiol |
| 群体遗传统计(Tajima's D / π / dN/dS) | 检测自然选择的信号。Tajima's D 偏离中性预期暗示选择;dN/dS > 1 暗示正选择。用于鉴定受选择作用的 NLR 位点。 | 需要足够的群体样本量(通常 >20 个群体);注意群体结构和连锁不平衡的影响;基因转换可能模拟正选择的信号。 | Stahl et al., 1999, Nature; Bergelson et al., 2001, Plant Physiol |
| 杂种坏死/自身免疫筛选 | 通过构建特定 NLR 等位组合的杂交后代,检测是否出现温度依赖的组成性免疫激活(矮化、坏死斑、PR 基因组成性表达)。 | 温度条件关键(许多不兼容性为温度依赖型);需要在多个温度条件下筛选;遗传背景效应可能掩盖或增强不兼容性。 | Bomblies et al., 2007, PLoS Biol |
| 效应蛋白组(effectome)分析 | 通过基因组测序和分泌组预测,系统鉴定病原群体中的效应蛋白库及其变异。结合 NLR 识别谱可以预测 R 基因突破风险。 | 效应蛋白的预测依赖分泌信号和已知基序(如 RXLR、T3SS 信号),假阳性率需要实验验证控制;群体水平采样对变异检测至关重要。 | Guttman et al., 2014, PLoS Pathog |
6.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
6.10参考文献
- Barragan AC, Weigel D. Plant NLR diversity: the known unknowns of pan-NLRomes. Curr Opin Plant Biol, 2021, 56: 393–401.
- Bergelson J, Kreitman M, Stahl EA, Tian D. Evolutionary dynamics of plant R-genes. Science, 2001, 292: 2281–2285.
- Bomblies K, Lempe J, Epple P, et al. Autoimmune response as a mechanism for a Dobzhansky-Muller-type incompatibility syndrome in plants. PLoS Biol, 2007, 5: e236.
- Bomblies K, Weigel D. Hybrid necrosis: autoimmunity as a potential gene-flow barrier in plant species. Nat Rev Genet, 2007, 8: 382–393.
- Essuman K, Summers DW, Sasaki Y, et al. The SARM1 Toll/Interleukin-1 receptor domain possesses intrinsic NAD⁺ cleavage activity that promotes pathological axonal degeneration. Neuron, 2017, 93: 1334–1343.
- Guttman DS, McHardy AC, Schulze-Lefert P. Microbial genome-enabled insights into plant-microorganism interactions. Nat Rev Genet, 2014, 15: 797–813.
- Horsefield S, Burdett H, Zhang X, et al. NAD⁺ cleavage activity by animal and plant TIR domains in cell death pathways. Science, 2019, 365: 793–799.
- Jacob F, Vernaldi S, Maekawa T. Evolution and conservation of plant NLR functions. Front Immunol, 2013, 4: 297.
- Kanzaki H, Yoshida K, Saitoh H, et al. Arms race co-evolution of Magnaporthe oryzae AVR-Pik and rice Pik genes driven by their physical interactions. Plant J, 2012, 72: 894–907.
- Karasov TL, Horton MW, Bergelson J. Genomic variability as a driver of plant-pathogen coevolution? Curr Opin Plant Biol, 2014, 18: 24–30.
- Kourelis J, van der Hoorn RAL. Defended to the nines: 25 years of resistance gene cloning identifies nine mechanisms for R protein function. Plant Cell, 2018, 30: 285–299.
- Kroj T, Chanclud E, Michel-Romiti C, et al. Integration of decoy domains derived from protein targets of pathogen effectors into plant immune receptors is widespread. New Phytol, 2016, 210: 618–626.
- Lacombe S, Rougon-Cardoso A, Sherber E, et al. Interfamily transfer of a plant pattern-recognition receptor confers broad-spectrum bacterial resistance. Nat Biotechnol, 2010, 28: 365–369.
- McCann HC, Guttman DS. Evolution of the type III secretion system and its effectors in plant-microbe interactions. New Phytol, 2008, 177: 33–47.
- McDonald BA, Linde C. Pathogen population genetics, evolutionary potential, and durable resistance. Annu Rev Phytopathol, 2002, 40: 349–379.
- Michelmore RW, Meyers BC. Clusters of resistance genes in plants evolve by divergent selection and a birth-and-death process. Genome Res, 1998, 8: 1113–1130.
- Mondragón-Palomino M, Meyers BC, Michelmore RW, Gaut BS. Patterns of positive selection in the complete NBS-LRR gene family of Arabidopsis thaliana. Genome Res, 2002, 12: 1305–1315.
- Peng YL. Engineering plant immunity: from nucleotide-binding leucine-rich repeat receptor functional mechanisms to practical applications. Phytopathol Res, 2025. DOI: 10.1186/s42483-025-00387-5.
- Stahl EA, Dwyer G, Mauricio R, et al. Dynamics of disease resistance polymorphism at the Rpm1 locus of Arabidopsis. Nature, 1999, 400: 667–671.
- Steuernagel B, Jupe F, Witek K, et al. NLR-parser: rapid annotation of plant NLR complements. Bioinformatics, 2015, 31: 1665–1667.
- Tamborski J, Krasileva KV. Evolution of plant NLRs: from natural history to precise modifications. Annu Rev Plant Biol, 2020, 71: 355–378.
- Tian D, Traw MB, Chen JQ, et al. Fitness costs of R-gene-mediated resistance in Arabidopsis thaliana. Nature, 2003, 423: 74–77.
- Urbach JM, Ausubel FM. The NBS-LRR architectures of plant R-proteins and metazoan NLRs evolved in independent events. Proc Natl Acad Sci USA, 2017, 114: 1063–1068.
- Van de Weyer AL, Monteiro F, Furzer OJ, et al. A species-wide inventory of NLR genes and alleles in Arabidopsis thaliana. Cell, 2019, 178: 1260–1272.
- Vetter MM, Repsher D, Singh T, et al. Flagellin perception varies quantitatively in Arabidopsis thaliana and its relatives. Mol Biol Evol, 2012, 29: 1655–1667.
- Zipfel C. Plant pattern-recognition receptors. Trends Immunol, 2014, 35: 345–351.