激素信号网络
免疫不是孤立发生的。激素网络是植物协调免疫、发育与环境响应的中枢
本章目录
- SA 通路:经典抗病激素的分子解析
- JA 通路:与 SA 的拮抗及其生态意义
- SA–JA 拮抗的分子基础与适应意义
- ET、ABA 及新兴激素信号的免疫角色
- 激素交叉的组学视角:网络而非线性通路
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
1961年,White 首次报道烟草花叶病毒感染后水杨酸(SA)水平升高。此后半个多世纪,植物激素与免疫的关系从"有趣的现象学关联"逐步发展为"具有完整分子逻辑的信号网络"。但一个核心问题始终困扰着研究者:植物如何用有限的几种激素编码无限多样的威胁信息?
答案不在于激素本身,而在于激素之间的关系。SA、JA、ET、ABA 等激素并非简单的"抗病开关",而是通过精密的拮抗、协同和时序调控,形成一个能够根据威胁类型动态配置防御策略的决策网络。本章将解析这个网络的核心组分和运作逻辑,从经典的 SA 和 JA 通路出发,经由 SA-JA 拮抗的分子基础,到 ET、ABA 等激素的免疫角色,最后用系统生物学的视角审视这个网络的整体属性。
一个重要的警告:激素免疫研究中充斥着"SA 抗活体营养型、JA 抗坏死营养型"的简化叙事。这种叙事作为入门框架有其价值,但正如我们将看到的,现实远比这复杂——同一种激素在不同浓度、不同时间、不同组织中可以发挥完全相反的功能。
5.1SA 通路:经典抗病激素的分子解析
SA 的生物合成
植物中 SA 主要通过异分支酸途径(isochorismate pathway)合成,该途径贡献了病原诱导 SA 积累的约90% (Wildermuth et al., 2001)。关键酶 ICS1(Isochorismate Synthase 1,拟南芥中也称 SID2)将分支酸转化为异分支酸;随后 PBS3(一种 GH3 家族酰基腺苷酸合成酶)和 EPS1 共同将异分支酸转化为 SA (Rekhter et al., 2019; Torrens-Spence et al., 2019)。这一合成途径直到2019年才被完整阐明——此前长达二十年间,从异分支酸到 SA 的最后一步一直是未解之谜。
SA 合成的转录调控是一个正反馈环路的核心:PAMP 识别或 ETI 激活 → MAPK 级联激活 → CBP60g/SARD1 转录因子活化 → ICS1 基因表达上调 → SA 积累 → 通过 NPR1 进一步增强防御基因表达(包括 CBP60g/SARD1 自身),形成正反馈 (Wang et al., 2011; Sun et al., 2015)。这个正反馈设计确保了一旦 SA 信号被触发,就能迅速放大到足以驱动系统性防御的水平。
NPR1:SA 信号的主开关
NPR1(Nonexpresser of PR genes 1)是 SA 信号转导的核心枢纽,也是整个植物免疫信号研究中功能最清晰的单一蛋白之一 (Cao et al., 1997; Wu et al., 2012)。
NPR1 的工作机制是一个教科书级的氧化还原调控范例:
- 静息状态:NPR1 以寡聚体形式存在于胞质中,通过分子间二硫键维持非活性构象。
- SA 感知:SA 直接结合 NPR1(Kd ≈ 140 nM),诱导构象变化 (Wu et al., 2012)。同时,SA 积累触发的氧化还原变化(通过硫氧还蛋白 TRX-h)还原 NPR1 的二硫键。
- 单体化与入核:二硫键还原导致 NPR1 寡聚体解离为单体,单体形式暴露核定位信号(NLS),进入细胞核 (Mou et al., 2003)。
- 转录共激活:入核的 NPR1 与 TGA 转录因子互作,激活 PR(Pathogenesis-Related)基因和其他防御基因的表达 (Zhang et al., 2003)。
- 信号终止:核内的 NPR1 被 CUL3 泛素连接酶泛素化并经蛋白酶体降解,确保信号不过度持续 (Spoel et al., 2009)。
图 5.1 SA-NPR1 信号通路的分子逻辑。病原信号诱导 CBP60g/SARD1 和 SA 合成基因表达,SA 积累推动 NPR1 从胞质寡聚体转为可入核单体;入核 NPR1 与 TGA 等转录因子协同激活 PR 基因,同时通过 NPR3/NPR4 和蛋白酶体周转限制信号持续时间。
NPR1 还有两个旁系同源蛋白 NPR3 和 NPR4,它们也能结合 SA,但扮演 NPR1 的负调控因子角色——在低 SA 浓度下促进 NPR1 降解,在高 SA 浓度下释放 NPR1。这一"浓度依赖性调控"使 SA-NPR 系统对 SA 浓度梯度敏感,可以区分"基础水平"和"感染诱导水平"的 SA 信号 (Fu et al., 2012; Ding et al., 2018)。
SA 与系统性获得抗性(SAR)
SA 通路的一个最重要的功能产出是 SAR——局部感染诱导的全株增强抗性 → 第1章 1.2节。SAR 的建立不仅依赖 SA 本身,还需要多种移动信号的协同作用:甲基水杨酸(MeSA)、壬二酸(azelaic acid)、甘油醛-3-磷酸(G3P)以及 N-hydroxypipecolic acid(NHP)等 (Fu & Dong, 2013; Hartmann et al., 2018)。其中,NHP 是近年来鉴定的最强效的 SAR 诱导物之一——其合成依赖 ALD1 和 FMO1,缺失任一基因即完全丧失 SAR 能力 (Chen et al., 2018) → 第11章。
SA 通路常被简化为"SA 升高 → NPR1 入核 → PR 基因表达"的线性模型。但实际上,SA 信号系统的精密之处在于其浓度编码和时间编码:不同浓度的 SA 通过 NPR1/NPR3/NPR4 的差异性亲和力激活不同的输出程序;SA 的积累时序(急性爆发 vs 持续低水平)编码了不同的防御策略(HR vs SAR)。
5.2JA 通路:与 SA 的拮抗及其生态意义
JA 的生物合成与信号转导
茉莉酸(Jasmonic Acid, JA)及其生物活性形式 JA-Ile(茉莉酰-异亮氨酸)是调控坏死营养型病原防御和昆虫抗性的核心激素。JA 的合成始于叶绿体膜脂中的 α-亚麻酸(18:3),经过脂氧合酶(LOX)、丙二烯氧化物合酶(AOS)和丙二烯氧化物环化酶(AOC)催化,在叶绿体中生成12-氧-植物二烯酸(OPDA);OPDA 转运至过氧化物酶体,经 β-氧化生成 JA;JA 随后被 JAR1 酶与异亮氨酸结合,形成活性形式 JA-Ile (Wasternack & Song, 2017)。
JA-Ile 的信号转导通过 COI1-JAZ 受体模块实现:
- 静息状态:JAZ(Jasmonate ZIM-domain)蛋白与 MYC2 等转录因子结合,抑制其转录活性。JAZ 同时招募 TOPLESS/TPR 共抑制子和组蛋白去乙酰化酶(HDAC),维持靶基因的沉默状态 (Pauwels et al., 2010)。
- JA-Ile 感知:JA-Ile 作为"分子胶水",促进 COI1(F-box 蛋白,SCF^COI1^ 泛素连接酶的底物受体)与 JAZ 蛋白的互作。COI1-JA-Ile-JAZ 三元复合体的晶体结构已被解析 (Sheard et al., 2010)。
- JAZ 降解:COI1 将 JAZ 蛋白泛素化,经26S 蛋白酶体降解。
- 转录去抑制:JAZ 降解后,MYC2(及 MYC3/MYC4)被释放,激活下游防御基因——包括植保素合成基因、蛋白酶抑制剂基因(抗虫)和次生代谢基因 (Fernández-Calvo et al., 2011)。
JA 信号的分支:MYC 分支 vs ERF 分支
JA 信号下游存在两个主要的转录分支,且两者的功能有所分化:
- MYC 分支:由 MYC2/3/4 转录因子驱动,主要调控伤害响应和昆虫防御(如蛋白酶抑制剂、挥发物合成),同时介导 JA 对 SA 通路的负调控。
- ERF 分支:由 ERF1 和 ORA59 等乙烯响应因子驱动,需要 JA 和 ET 的协同激活,主要调控对坏死营养型病原(如B. cinerea)的防御(如 PDF1.2 等防御素的表达)(Lorenzo et al., 2003)。
两个分支之间存在拮抗关系:MYC2 抑制 ERF 分支基因的表达,反之亦然。这种分支间的拮抗使植物能够根据具体威胁类型(昆虫 vs 坏死病原)微调 JA 信号的输出方向 (Verhage et al., 2011)。
5.3SA-JA 拮抗的分子基础与适应意义
SA 与 JA 通路之间的拮抗关系是植物激素免疫研究中最经典、也最被过度简化的现象之一。
拮抗的分子机制
SA 对 JA 通路的抑制至少通过以下几条分子途径实现:
- NPR1 依赖性抑制:核内 NPR1 与 TGA 转录因子的互作可以抑制 JA 响应基因的表达。但有趣的是,NPR1 对 JA 通路的抑制主要依赖其胞质功能(而非核功能),具体机制尚未完全阐明 (Spoel et al., 2003)。
- GRX480/ROXY 介导:SA 诱导谷氧还蛋白 GRX480 的表达,GRX480 与 TGA 转录因子互作,抑制 ORA59 和 PDF1.2 的表达 (Ndamukong et al., 2007)。
- WRKY 转录因子网络:SA 诱导的 WRKY70 同时激活 SA 响应基因和抑制 JA 响应基因,是 SA-JA 拮抗的一个关键交叉节点 (Li et al., 2004)。
- MYC2 的双重角色:MYC2 在激活 JA 分支基因的同时,也通过抑制 SA 合成基因 ICS1 的表达负调控 SA 通路 (Laurie-Berry et al., 2006)。这种双向拮抗确保了 SA 和 JA 通路不会同时全力激活。
拮抗的适应意义:资源分配优化
SA-JA 拮抗的进化意义何在?主流解释是资源分配优化:活体营养型病原和坏死营养型病原/昆虫需要截然不同的防御策略(对前者有效的 HR 反而助长后者),同时全面激活两条通路在代谢上成本过高。因此,SA-JA 拮抗作为一种"决策开关",帮助植物根据当前威胁类型优先配置防御资源 (Pieterse et al., 2012)。
然而,"二选一"的简化叙事忽视了大量的复杂性:
- 时间依赖性:在感染早期,SA 和 JA 可以短暂地协同激活;拮抗效应主要在持续感染阶段显现 (Mur et al., 2006)。
- 浓度依赖性:低浓度 SA 对 JA 通路的抑制弱于高浓度。生理条件下的 SA 浓度梯度产生的效应可能与药理学剂量实验不同。
- 组织依赖性:根部的 SA-JA 关系与叶片不同——根部两条通路更倾向于协同而非拮抗 (Millet et al., 2010) → 第10章。
- 病原操纵:P. syringae 产生的冠菌素(coronatine)是 JA-Ile 的结构类似物,通过激活 JA 通路来拮抗对其不利的 SA 防御——这是病原利用 SA-JA 拮抗来"劫持"植物防御决策的经典案例 (Zheng et al., 2012) → 第8章。
图 5.2 SA-JA 拮抗的分子节点与生态逻辑。SA 模块通过 NPR1、WRKY70、GRX480 等节点抑制 JA 输出,JA 模块也可反向限制 SA 合成和响应;这种关系不是固定跷跷板,而是受威胁类型、组织、时间和微生物组背景调节的动态决策系统。
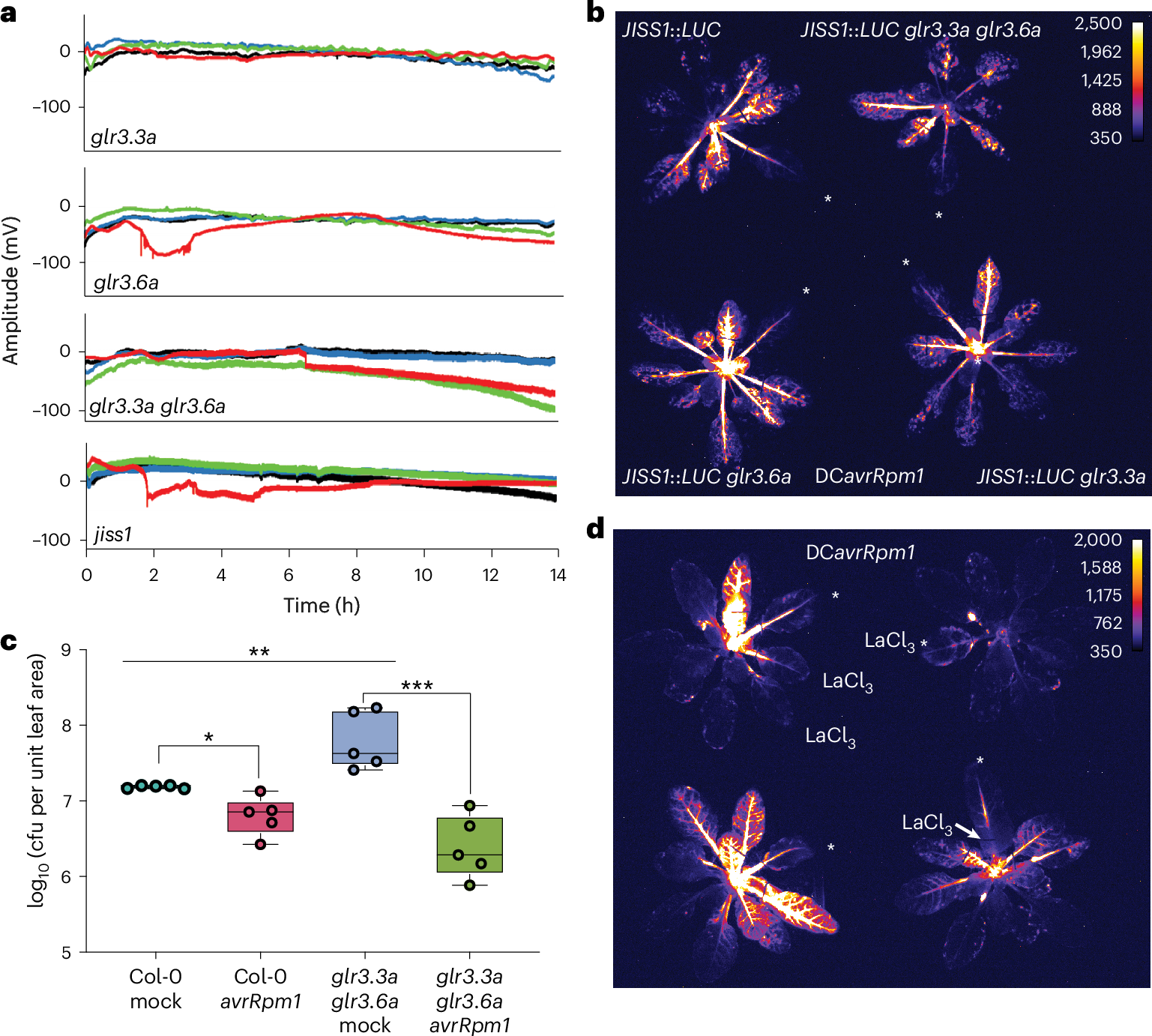
图 5.P1 论文原图:JA 依赖的系统性电信号改写“SA-JA 二选一”的旧叙事。原图为 Gaikwad et al. (2026) Nature Plants Fig. 6,DOI: 10.1038/s41477-025-02178-4。该图显示 ETI 可诱导 JA 依赖的远端电信号,为理解激素串扰提供了比静态拮抗模型更接近时空动态的证据。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
SA-JA 拮抗不是一个固定的"跷跷板",而是一个受上下文调制的动态决策系统。其输出取决于激素浓度、时间窗口、组织类型和微生物组背景等多个变量。在讨论激素拮抗时,始终要问:"在什么浓度?什么时间?什么组织?什么生态背景下?"
5.4ET、ABA 及新兴激素信号的免疫角色
乙烯(ET):JA 的协同伙伴
乙烯在植物免疫中的作用与 JA 密切交织。ET 信号通过 EIN2-EIN3/EIL1 通路传导:在无 ET 时,EIN3 被 EBF1/2 泛素化降解;ET 存在时,EIN2 稳定 EIN3,后者激活下游靶基因 (Alonso et al., 1999; An et al., 2010)。
在免疫中,ET 的主要功能包括:
- 与 JA 协同激活 ERF 分支:ET 和 JA 共同激活 ERF1/ORA59 转录因子,驱动 PDF1.2 等抗真菌防御素的表达。单独的 JA 或 ET 信号不足以完全激活这些基因 (Lorenzo et al., 2003)。
- 调控 PAMP 诱导的防御:ET 信号增强 flg22 诱导的 FRK1 等早期防御基因的表达,可能通过稳定相关 mRNA 实现 (Mersmann et al., 2010)。
- 在 ISR 中的关键角色:有益根际细菌(如Pseudomonas fluorescens)诱导的系统性抗性(Induced Systemic Resistance, ISR)主要依赖 JA/ET 通路而非 SA 通路 (Pieterse et al., 1998) → 第10章。
脱落酸(ABA):免疫的双面调控因子
ABA 在免疫中的角色极为复杂且常常矛盾——同一种激素既可以促进防御,又可以抑制防御,取决于感染阶段和病原类型。
ABA 的正调控角色:
- ABA 促进气孔关闭,是植物抵抗细菌从气孔入侵的第一道激素防线 (Melotto et al., 2006)。
- ABA 诱导胼胝质沉积,增强细胞壁屏障。
- ABA 在早期 PAMP 响应中可以增强某些防御基因的表达。
ABA 的负调控角色:
- ABA 抑制 SA 合成和信号,削弱对活体营养型病原的防御。P. syringae 通过效应蛋白促进 ABA 合成/信号来"劫持"这一拮抗关系 (de Torres-Zabala et al., 2007)。
- 干旱胁迫(高 ABA)显著增加植物对病原的易感性,部分原因是 ABA 介导的免疫抑制 (Mohr & Cahill, 2007)。
ABA 的这种"双面性"可能反映了其在免疫中不同时间阶段的角色切换:在感染早期(数小时内),ABA 促进气孔关闭等快速物理防御;在持续感染阶段(数天),ABA 积累抑制 SA 通路,可能作为一种"成本控制"机制避免过度防御造成的生长代价。
新兴激素信号
除经典激素外,近年来多种新的信号分子被发现参与免疫调控:
- 油菜素内酯(BR):BR 信号通过 BES1/BZR1 转录因子与免疫信号交叉。BRI1(BR 受体)和 FLS2(flg22 受体)共享共受体 BAK1,形成了 BR 生长信号和免疫信号之间的分子竞争界面 (Albrecht et al., 2012) → 第9章。
- 生长素(Auxin):多种病原(包括Agrobacterium和根结线虫)通过操纵生长素信号重编程宿主细胞以利于自身生存。SA 通路可以抑制生长素信号,这被认为是免疫-生长协调的另一个维度 (Wang et al., 2007)。
- 肽类信号(DAMP 肽):植物产生的小肽如 PEP1/2(由 PROPEP 前体加工)和 PIP1/2,通过 PEPR1/2 和 RLK7 等受体放大免疫信号。这些 DAMP 肽可被视为"内源性免疫增强剂",连接了损伤感知与激素防御网络 (Huffaker et al., 2006) → 第6章。
5.5激素交叉的组学视角:网络而非线性通路
当我们从单一激素通路的视角退后一步,用系统生物学的眼光审视整个激素-免疫网络时,一个根本性的认知转变浮现出来:植物激素免疫不是"SA 通路 + JA 通路 + ET 通路 + ..."的简单叠加,而是一个高度互联的网络系统,其行为具有涌现性质。
转录组学揭示的网络属性
Tsuda et al. (2009) 对拟南芥 SA、JA、ET 和 PAD4 四个信号扇区的网络分析揭示了一个关键特征:在 ETI 条件下,四个扇区之间呈现高度补偿性冗余——单个扇区的丧失对整体抗性影响不大,但多个扇区同时丧失则导致急剧崩溃。这种网络拓扑使 ETI 对效应蛋白的攻击具有鲁棒性——即使一条通路被效应蛋白抑制,其他通路可以补偿 → 第2章 2.6节。
相比之下,PTI 条件下各扇区的贡献更接近简单加性——这可能是 PTI 比 ETI 更容易被效应蛋白抑制的一个分子解释。
时空动态:激素浪潮的精确编排
高时间分辨率的激素定量分析(LC-MS/MS)揭示了一个令人印象深刻的时序特征:不同激素在感染后以精确的时间顺序被激活。以P. syringae感染拟南芥为例:
- 0-2小时:ET 快速爆发(数分钟内检测到乙烯释放增加)
- 2-8小时:JA/JA-Ile 水平开始上升
- 8-24小时:SA 大量积累,达到驱动 SAR 的水平
- 24-72小时:ABA 水平变化取决于病原类型和感染严重程度
这种时序编排不是偶然的——它反映了防御策略的时间逻辑:早期的 ET 爆发提供快速的转录微调信号;JA 的中期积累启动抗菌代谢物合成;SA 的后期积累驱动持续的转录重编程和 SAR。激素的时间序列本身就是一种信息编码 (Pieterse et al., 2012)。
2026 年的茉莉酸研究进一步修正了这种线性分工。Gaikwad et al. (2026) 发现,局部感染可快速触发 JA 信号,并通过系统性 JA 波推动植物全株免疫的启动与建立。这意味着 JA 不应只被放在“抗虫/抗坏死营养型病原”的支路中理解;在某些感染背景下,它也可能是系统免疫早期建立的驱动信号,与 SA-NHP 轴共同塑造远端组织的 priming 状态。
图 5.3 感染后主要免疫激素的时间动态与功能分工。不同激素不是独立开关,而是在不同时间窗内形成互相调制的信号波。2026 年的 JA 系统信号研究提示,JA 波可参与系统免疫的启动,而不仅是局部抗虫或抗坏死营养型防御的输出。
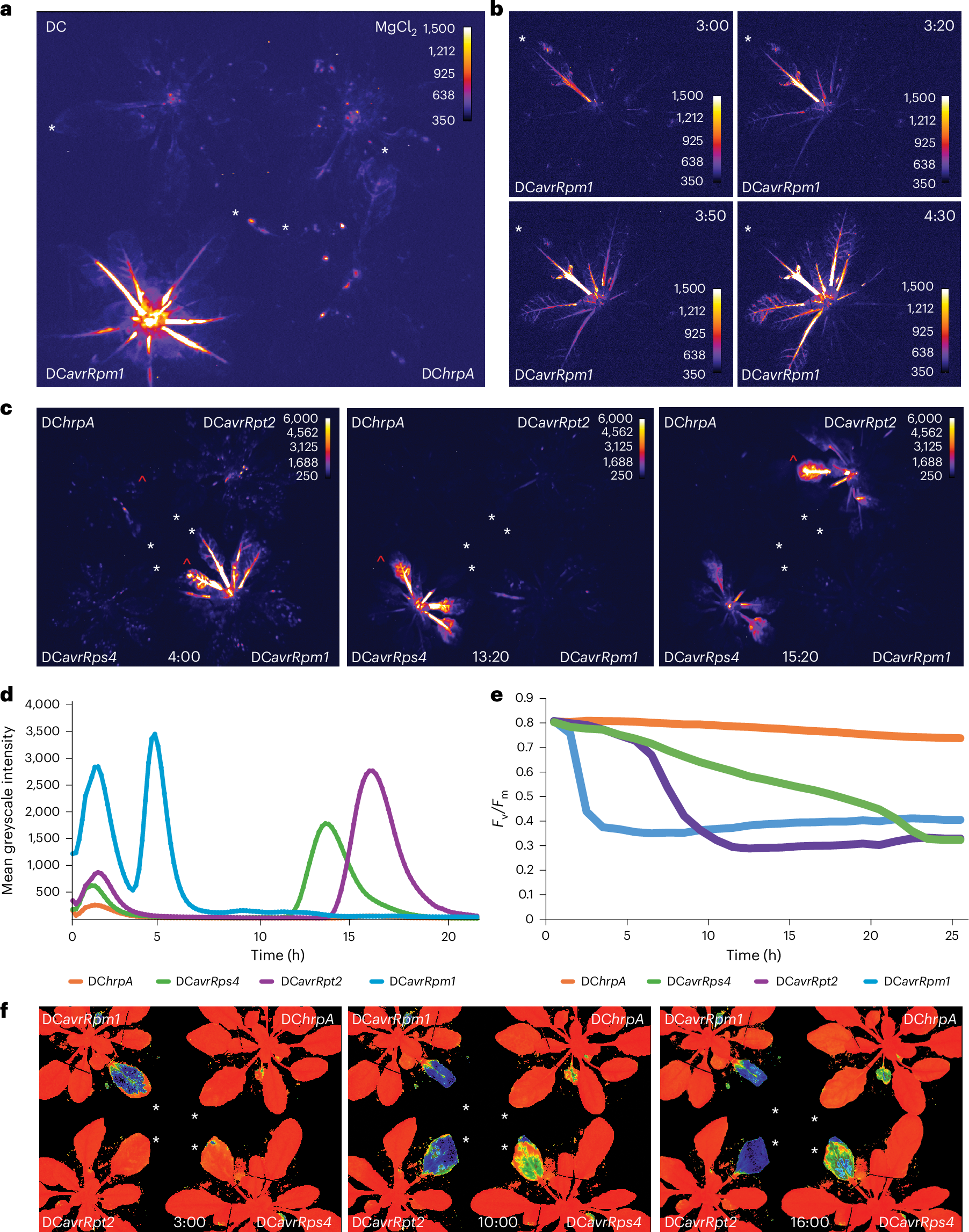
图 5.P2 论文原图:JA 局部与远端信号参与系统免疫建立。原图为 Gaikwad et al. (2026) Nature Plants Fig. 1,DOI: 10.1038/s41477-025-02178-4。该图提供了 JA 信号从局部诱导扩展到系统性免疫的最新实验证据,补充本节的时间动态模型。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
能否在不触发生长代价的情况下增强激素介导的免疫?
激素免疫的一个核心困境是:增强 SA 通路提升抗病性,但同时抑制生长素和 BR 信号导致矮化和减产;增强 JA 通路提升抗虫性,但引发资源的大量转向次生代谢。解耦这种权衡的策略包括:(1)仅在感染发生时条件性激活激素通路(如使用病原诱导型启动子驱动 ICS1);(2)操控 SA-JA 拮抗的特定节点(如修改 NPR3/NPR4 的 SA 亲和力)使"低浓度 SA 也能有效激活防御";(3)利用 priming 概念——以极低的基础激素代价预设信号系统,仅在感染时快速放大 → 第9章, 第14章。哪种策略最有前景,很可能取决于具体的作物-病原体系和田间环境。
5.6里程碑研究思路拆解
里程碑 1:Pieterse et al. (2012) — 激素免疫网络化框架
面对的问题:大量关于 SA、JA、ET 在免疫中角色的实验结果互相矛盾——同一种激素在不同实验系统中表现出促进或抑制防御的相反效果。
关键思路:提出将激素免疫从"单一通路"思维升级为"网络串话"思维。激素的功能不取决于其本身,而取决于其与其他激素信号的交互关系和时空背景。
关键证据链:系统性比较不同病原类型(活体营养型/坏死营养型/半活体营养型/昆虫/有益微生物)诱导的激素谱,发现每种威胁诱导独特的激素组合("激素指纹"),且植物的防御输出与这一组合相关而非与单一激素相关。
影响:该综述建立了激素免疫研究的标准框架,至今仍是该领域被引用最多的入口文献。其核心洞见——"网络交互决定输出"——已被后续的组学数据广泛支持。
里程碑 2:Wu et al. (2012) — NPR1 作为 SA 受体
面对的问题:SA 是植物免疫的核心激素,NPR1 是其信号通路的关键枢纽——但 SA 的"受体"究竟是什么?NPR1 是 SA 的直接靶标还是间接效应器?
关键思路:利用平衡透析(equilibrium dialysis)和差异扫描荧光法(DSF),在纯蛋白体系中证明 SA 直接结合 NPR1 的 BTB 结构域区域。同时,通过过渡金属介导的亲和纯化和结构域截短实验,鉴定了 SA 结合的关键残基。
关键证据链:(1)纯化 NPR1 直接结合 ³H-SA,Kd ≈ 140 nM;(2)SA 结合促进 NPR1 构象变化(增强与 TGA 转录因子的互作);(3)破坏 SA 结合位点的突变消除 NPR1 在体内的免疫功能。
影响:解决了长达十余年的"SA 受体之争"(此前 NPR3/NPR4 也被提议为 SA 受体),确立 NPR1 为 SA 信号的核心感知器。
里程碑 3:Sheard et al. (2010) — COI1-JAZ-JA-Ile 三元受体复合体结构
面对的问题:JA 信号的感知机制是什么?COI1 和 JAZ 如何被 JA-Ile 连接起来?
关键思路:通过 X 射线晶体学解析了 COI1-JA-Ile-JAZ1 三元复合体的三维结构,揭示 JA-Ile 充当"分子胶水"的精确机制。
关键证据链:(1)晶体结构显示 JA-Ile 结合于 COI1 和 JAZ1 之间的口袋中;(2)肌醇五磷酸(IP5)作为辅因子参与复合体稳定;(3)基于结构预测的关键残基突变验证了功能重要性。
影响:提供了植物激素-受体互作的第一个完整原子级结构模型之一,也解释了为什么冠菌素(JA-Ile 的结构类似物)能"劫持" JA 通路——它以更高亲和力结合同一个口袋。
5.7当前争论与未解问题
- SA-JA 拮抗在不同组织中是否保守?大多数研究在叶片中进行,但根部 SA-JA 关系可能更倾向协同。根部免疫激素网络的特殊性需要更多系统性研究。
- 如何实现"精准激素增强"以降低生长代价?全局性增强 SA 信号导致严重的生长抑制。能否通过时空精准控制(病原诱导型启动子、组织特异性表达)或信号节点微调(修改 NPR 家族的 SA 亲和力)实现代价可控的免疫增强?
- 病原操纵激素网络的最脆弱节点在哪里?多种效应蛋白靶向激素合成或信号转导的不同步骤。识别"最常被攻击的节点"可以揭示网络的结构弱点,也为"加固"这些节点提供工程靶标 → 第8章。
- 能否用数学模型预测激素交叉的输出?给定一个具体的激素浓度组合(SA, JA-Ile, ET, ABA),能否定量预测防御基因表达的变化?微分方程模型和机器学习方法都在尝试,但目前预测能力有限。
- 微生物组如何影响宿主激素网络?根际和叶际微生物持续通过代谢物和 MAMP 影响植物的激素稳态。在"全微生物组"背景下理解激素网络的行为,是整合免疫学和微生物组学的前沿挑战 → 第10章。
5.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 激素定量(LC-MS/MS) | 同时定量测定组织中多种激素(SA、JA、JA-Ile、ABA、ET 前体 ACC 等)的绝对含量。是构建感染时序激素谱的核心方法。 | 需要同位素内标(如 d4-SA)确保定量准确性;注意取样速度(激素水平可在数分钟内变化);区分游离态和结合态激素。 | Forcat et al., 2008, Plant Methods |
| 激素信号突变体/报告基因分析 | 利用信号通路关键基因的突变体(sid2、npr1、coi1、ein2 等)分析各通路的功能贡献。结合报告基因(如 PR1::GUS、PDF1.2::GFP)实时监测通路激活。 | 注意多重突变体的构建策略和遗传背景一致性;报告基因的时空分辨率受启动子选择限制;部分激素突变体(如 coi1)有严重的发育表型。 | Fu & Dong, 2013, Annu Rev Plant Biol |
| 双病原/序贯挑战实验 | 先接种一种病原(或施加激素),再接种第二种病原,测量串话对防御效果的影响。是验证 SA-JA 拮抗生态意义的核心策略。 | 两次接种的时间间隔、接种剂量和接种部位都会影响结果;需要同时设置所有单一处理和组合处理的对照。 | Spoel et al., 2007, PNAS |
| 转录组 + 网络分析 | 在不同激素处理/突变体背景下进行 RNA-seq,通过差异表达分析和网络推断(如 WGCNA)鉴定激素交叉调控的关键节点。 | 实验设计需要覆盖多个时间点和处理组合;网络推断方法的选择影响结果(共表达网络 vs 因果推断网络);需要独立验证关键预测。 | Tsuda et al., 2009, PLoS Genet |
5.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
5.10参考文献
- Albrecht C, Boutrot F, Segonzac C, et al. Brassinosteroids inhibit pathogen-associated molecular pattern-triggered immune signaling independent of the receptor kinase BAK1. Proc Natl Acad Sci USA, 2012, 109: 303–308.
- Alonso JM, Hirayama T, Roman G, et al. EIN2, a bifunctional transducer of ethylene and stress responses in Arabidopsis. Science, 1999, 284: 2148–2152.
- An F, Zhao Q, Ji Y, et al. Ethylene-induced stabilization of ETHYLENE INSENSITIVE3 and EIN3-LIKE1 is mediated by proteasomal degradation of EIN3 binding F-box 1 and 2. Plant Cell, 2010, 22: 2384–2401.
- Cao H, Glazebrook J, Clarke JD, et al. The Arabidopsis NPR1 gene that controls systemic acquired resistance encodes a novel protein containing ankyrin repeats. Cell, 1997, 88: 57–63.
- Chen YC, Holmes EC, Rajniak J, et al. N-hydroxy-pipecolic acid is a mobile metabolite that induces systemic disease resistance in Arabidopsis. Proc Natl Acad Sci USA, 2018, 115: E4920–E4929.
- de Torres-Zabala M, Truman W, Bennett MH, et al. Pseudomonas syringae pv. tomato hijacks the Arabidopsis abscisic acid signalling pathway to cause disease. EMBO J, 2007, 26: 1434–1443.
- Ding Y, Sun T, Ao K, et al. Opposite roles of salicylic acid receptors NPR1 and NPR3/NPR4 in transcriptional regulation of plant immunity. Cell, 2018, 173: 1454–1467.
- Fernández-Calvo P, Chini A, Fernández-Barbero G, et al. The Arabidopsis bHLH transcription factors MYC3 and MYC4 are targets of JAZ repressors and act additively with MYC2 in the activation of jasmonate responses. Plant Cell, 2011, 23: 701–715.
- Fu ZQ, Dong X. Systemic acquired resistance: turning local infection into global defense. Annu Rev Plant Biol, 2013, 64: 839–863.
- Fu ZQ, Yan S, Saleh A, et al. NPR3 and NPR4 are receptors for the immune signal salicylic acid in plants. Nature, 2012, 486: 228–232.
- Gaikwad T, Breen S, Breeze E, et al. Rapid local and systemic jasmonate signalling drives the initiation and establishment of plant systemic immunity. Nat Plants, 2026, 12: 152–163. DOI: 10.1038/s41477-025-02178-4.
- Hartmann M, Zeier T, Bernsdorff F, et al. Flavin monooxygenase-generated N-hydroxypipecolic acid is a critical element of plant systemic immunity. Cell, 2018, 173: 456–469.
- Huffaker A, Pearce G, Ryan CA. An endogenous peptide signal in Arabidopsis activates components of the innate immune response. Proc Natl Acad Sci USA, 2006, 103: 10098–10103.
- Laurie-Berry N, Joardar V, Street IH, Kunkel BN. The Arabidopsis thaliana JASMONATE INSENSITIVE 1 gene is required for suppression of salicylic acid-dependent defenses during infection by Pseudomonas syringae. Mol Plant-Microbe Interact, 2006, 19: 789–800.
- Li J, Brader G, Palva ET. The WRKY70 transcription factor: a node of convergence for jasmonate-mediated and salicylate-mediated signals in plant defense. Plant Cell, 2004, 16: 319–331.
- Lorenzo O, Piqueras R, Sánchez-Serrano JJ, Solano R. ETHYLENE RESPONSE FACTOR1 integrates signals from ethylene and jasmonate pathways in plant defense. Plant Cell, 2003, 15: 165–178.
- Melotto M, Underwood W, Koczan J, et al. Plant stomata function in innate immunity against bacterial invasion. Cell, 2006, 126: 969–980.
- Mersmann S, Bourdais G, Rietz S, Robatzek S. Ethylene signaling regulates accumulation of the FLS2 receptor and is required for the oxidative burst contributing to plant immunity. Plant Physiol, 2010, 154: 391–400.
- Millet YA, Danna CH, Clay NK, et al. Innate immune responses activated in Arabidopsis roots by microbe-associated molecular patterns. Plant Cell, 2010, 22: 973–990.
- Mohr PG, Cahill DM. Suppression by ABA of salicylic acid and lignin accumulation and the expression of multiple genes, in Arabidopsis infected with Pseudomonas syringae pv. tomato. Funct Integr Genomics, 2007, 7: 181–191.
- Mou Z, Fan W, Dong X. Inducers of plant systemic acquired resistance regulate NPR1 function through redox changes. Cell, 2003, 113: 935–944.
- Mur LAJ, Kenton P, Atzorn R, et al. The outcomes of concentration-specific interactions between salicylate and jasmonate signaling include synergy, antagonism, and oxidative stress leading to cell death. Plant Physiol, 2006, 140: 249–262.
- Ndamukong I, Abdallat AA, Thurow C, et al. SA-inducible Arabidopsis glutaredoxin interacts with TGA factors and suppresses JA-responsive PDF1.2 transcription. Plant J, 2007, 50: 128–139.
- Pauwels L, Barbero GF, Geerinck J, et al. NINJA connects the co-repressor TOPLESS to jasmonate signalling. Nature, 2010, 464: 788–791.
- Pieterse CMJ, Van Wees SCM, Van Pelt JA, et al. A novel signaling pathway controlling induced systemic resistance in Arabidopsis. Plant Cell, 1998, 10: 1571–1580.
- Pieterse CMJ, Van der Does D, Zamioudis C, et al. Hormonal modulation of plant immunity. Annu Rev Cell Dev Biol, 2012, 28: 489–521.
- Rekhter D, Lüdke D, Ding Y, et al. Isochorismate-derived biosynthesis of the plant stress hormone salicylic acid. Science, 2019, 365: 498–502.
- Sheard LB, Tan X, Mao H, et al. Jasmonate perception by inositol-phosphate-potentiated COI1-JAZ co-receptor. Nature, 2010, 468: 400–405.
- Spoel SH, Koornneef A, Claessens SMC, et al. NPR1 modulates cross-talk between salicylate- and jasmonate-dependent defense pathways through a novel function in the cytosol. Plant Cell, 2003, 15: 760–770.
- Spoel SH, Johnson JS, Dong X. Regulation of tradeoffs between plant defenses against pathogens with different lifestyles. Proc Natl Acad Sci USA, 2007, 104: 18842–18847.
- Spoel SH, Mou Z, Tada Y, et al. Proteasome-mediated turnover of the transcription coactivator NPR1 plays dual roles in regulating plant immunity. Cell, 2009, 137: 860–872.
- Sun T, Zhang Y, Li Y, et al. ChIP-seq reveals broad roles of SARD1 and CBP60g in regulating plant immunity. Nat Commun, 2015, 6: 10159.
- Torrens-Spence MP, Bobokalonova A, Carballo V, et al. PBS3 and EPS1 complete salicylic acid biosynthesis from isochorismate in Arabidopsis. Mol Plant, 2019, 12: 884–897.
- Tsuda K, Sato M, Stoddard T, et al. Network properties of robust immunity in plants. PLoS Genet, 2009, 5: e1000772.
- Verhage A, van Wees SCM, Pieterse CMJ. Plant immunity: it's the hormones talking, but what do they say? Plant Physiol, 2011, 154: 536–540.
- Vlot AC, Dempsey DMA, Klessig DF. Salicylic acid, a multifaceted hormone to combat disease. Annu Rev Phytopathol, 2009, 47: 177–206.
- Wang D, Pajerowska-Mukhtar K, Culler AH, Dong X. Salicylic acid inhibits pathogen growth in plants through repression of the auxin signaling pathway. Curr Biol, 2007, 17: 1784–1790.
- Wang L, Tsuda K, Truman W, et al. CBP60g and SARD1 play partially redundant critical roles in salicylic acid signaling. Plant J, 2011, 67: 1029–1041.
- Wasternack C, Song S. Jasmonates: biosynthesis, metabolism, and signaling by proteins activating and repressing transcription. J Exp Bot, 2017, 68: 1303–1321.
- Wildermuth MC, Dewdney J, Wu G, Ausubel FM. Isochorismate synthase is required to synthesize salicylic acid for plant defence. Nature, 2001, 414: 562–565.
- Wu Y, Zhang D, Chu JY, et al. The Arabidopsis NPR1 protein is a receptor for the plant defense hormone salicylic acid. Cell Rep, 2012, 1: 639–647.
- Zhang Y, Tessaro MJ, Lassner M, Li X. Knockout analysis of Arabidopsis transcription factors TGA2, TGA5, and TGA6 reveals their redundant and essential roles in systemic acquired resistance. Plant Cell, 2003, 15: 2647–2653.
- Zheng XY, Spivey NW, Zeng W, et al. Coronatine promotes Pseudomonas syringae virulence in plants by activating a signaling cascade that inhibits salicylic acid accumulation. Cell Host Microbe, 2012, 11: 587–596.