从基础到抗病育种
基础免疫研究如何转化为田间的抗病能力?
本章目录
- 经典抗病育种的成功与局限
- NLR 工程与合理设计
- PTI 强化与非 NLR 抗病策略
- 组合部署:堆叠、轮换与区域管理
- 基因编辑时代的新工具
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
植物免疫学过去三十年的进展令人瞩目——我们解析了 PRR 和 NLR 的结构、阐明了信号转导的分子级联、揭示了激素网络的精密调控。但一个令人不安的现实是:基础研究的爆发式增长并未同步转化为田间抗病能力的等比例提升。全球主要作物因病害造成的产量损失仍然维持在10-16%(Savary et al., 2019),新兴病害持续出现,而已部署的抗性基因不断被病原克服。
这一"转化鸿沟"的核心不在于基础知识不够,而在于从机制发现到田间部署的完整链路中存在多个瓶颈:抗性资源的鉴定、功能验证、遗传导入、多基因组合设计、耐久性评估、以及与产量和品质的协调——每一个环节都有其独特的技术和概念障碍。
Dangl, Horvath & Staskawicz (2013) 在 Science 上提出了一个关键论断:"Pivoting the plant immune system from dissection to deployment"——植物免疫学需要从"拆解"模式转向"部署"模式。本章正是沿着这一思路,系统梳理从基础免疫机制到田间抗病能力的转化链路,分析每个环节的现状、瓶颈和前沿突破。
14.1经典抗病育种的成功与局限
认知演变
过去:传统抗病育种依赖"发现主效 R 基因→回交导入→品种释放"的线性流程。这一策略在20世纪下半叶取得了巨大成功——小麦锈病、水稻稻瘟病、番茄叶霉病等重要病害都通过 R 基因的部署得到了有效控制。
转折:但"繁荣-崩溃"循环(boom-and-bust cycle)反复上演——一个新 R 基因品种推广后3-5年,病原群体中相应 Avr 基因的突变或缺失突变体被选择出来,抗性随即失效 (McDonald & Linde, 2002)。最典型的案例是小麦品种 Lr24 的抗叶锈基因在大面积推广后仅数年即被克服。
现在:共识转向多基因堆叠、定量抗性利用和动态部署管理——从追求"最强的单一抗性"转向追求"最耐久的系统抗性"。
抗性资源的挖掘
有效转化的第一步是找到可用的抗性来源。主要策略包括:
- 野生近缘种:作物驯化过程中大量遗传多样性被丢失——栽培小麦仅保留了其野生祖先 ~30% 的 NLR 多样性 (Steuernagel et al., 2020)。野生近缘种是尚未被开发的巨大抗性基因库。例如,来自野生稻的 Pigm 位点包含一对 NLR 基因(PigmR/PigmS),其精妙的表观遗传调控实现了广谱抗性与产量的兼顾 (Deng et al., 2017) → 第4章。
- 自然变异的 GWAS 挖掘:基因组关联分析(GWAS)在大规模自然群体中鉴定与抗性关联的遗传位点。这一方法的优势在于能发现微效多基因位点——传统遗传学方法难以检测的"定量抗性"组分。
- 抗性基因富集测序(RenSeq):利用序列捕获技术专门富集 NLR 基因组区域进行测序,可以在短时间内获得一个物种的完整 NLR 库存清单 (Steuernagel et al., 2016)。这一技术极大地加速了 R 基因克隆的速度——从传统的图位克隆需要数年缩短到数月。
14.2NLR 工程与合理设计
抗病小体(resistosome)的结构解析 → 第4章 和对 NLR 激活机制的深入理解,为 NLR 的理性设计(rational design)提供了前所未有的分子信息基础。
整合结构域的工程化
含有整合结构域(Integrated Domain, ID)的 NLR 是工程化的最有前景的靶标。ID 本质上是一个被整合到 NLR 蛋白中的效应蛋白靶标"诱饵"——如水稻 Pik-1 中的 HMA 结构域是 AVR-PikD 效应蛋白的结合靶标 → 第8章。理论上,通过修改 ID 的结合特异性,可以改变 NLR 的识别谱——使其识别原本不能识别的效应蛋白。
De la Concepcion et al. (2019) 在水稻 Pikp-1 的 HMA 结构域中引入两个氨基酸突变,成功扩展了其对不同 AVR-Pik 等位基因的识别范围。这是 NLR 工程化的一个重要概念验证,但距离实际应用还有距离——修改后的 NLR 需要在田间条件下验证其广谱性、信号完整性和对产量的影响。
NLR 结构域交换与嵌合体
另一种策略是在不同 NLR 之间交换功能结构域,创造新的识别-信号组合。例如,将一个高效信号结构域(如 ZAR1 的 CC 结构域)与一个具有所需识别特异性的 LRR 结构域组合。但 NLR 的自抑制构象对结构域间的精密配合高度敏感——随意交换往往导致蛋白质错折叠、自激活或信号丧失。结构引导的设计和高通量筛选是克服这一障碍的关键 (Tamborski & Krasileva, 2020)。
扩展识别范围的替代路线
"保卫/诱饵"模式的 NLR 也提供了工程化入口。理论上,可以修改被 NLR 监测的"保卫"蛋白,使其成为新效应蛋白的靶标——从而将已有的 NLR-信号模块重新用于识别新的病原威胁。Kim et al. (2016) 将大豆的 PBS1 激酶中的 AvrPphB 切割位点替换为不同病原蛋白酶的识别序列,成功地将 RPS5 介导的抗性重定向到新的病原——这一"PBS1 decoy"策略为 NLR 工程化提供了模块化的设计框架。
图 14.1 NLR 工程化的三种策略。ID 修改通过改变整合域结合界面扩展识别谱;结构域交换试图把不同 NLR 的识别端和信号端重组;诱饵重定向则修改被监测靶标,使既有 NLR 模块能够感知新的病原酶活性。
14.3PTI 强化与非 NLR 抗病策略
NLR 介导的 ETI 是最强力的免疫层,但也是最容易被病原通过 Avr 基因进化克服的一层。因此,越来越多的研究者开始关注非 NLR 的抗病策略——这些策略可能提供更持久(虽然可能更温和)的保护。
PRR 跨物种转移
一个优雅的策略是将一个物种的 PRR 转移到另一个不具有该受体的物种中,扩展其 PAMP 识别谱。经典案例包括:
- 拟南芥的 EFR 受体(识别细菌 EF-Tu)转移到番茄和水稻中,增强了对多种细菌病原的广谱抗性 (Lacombe et al., 2010)。
- 水稻的 XA21 受体转移到柑橘中,增强了对柑橘溃疡病菌的抗性。
PRR 转移策略的一个显著优势是耐久性预期较高——因为 PRR 识别的是病原无法轻易改变的保守分子模式(如 EF-Tu 的结构对细菌存活是必需的),病原通过突变逃避的进化空间有限 → 第3章。
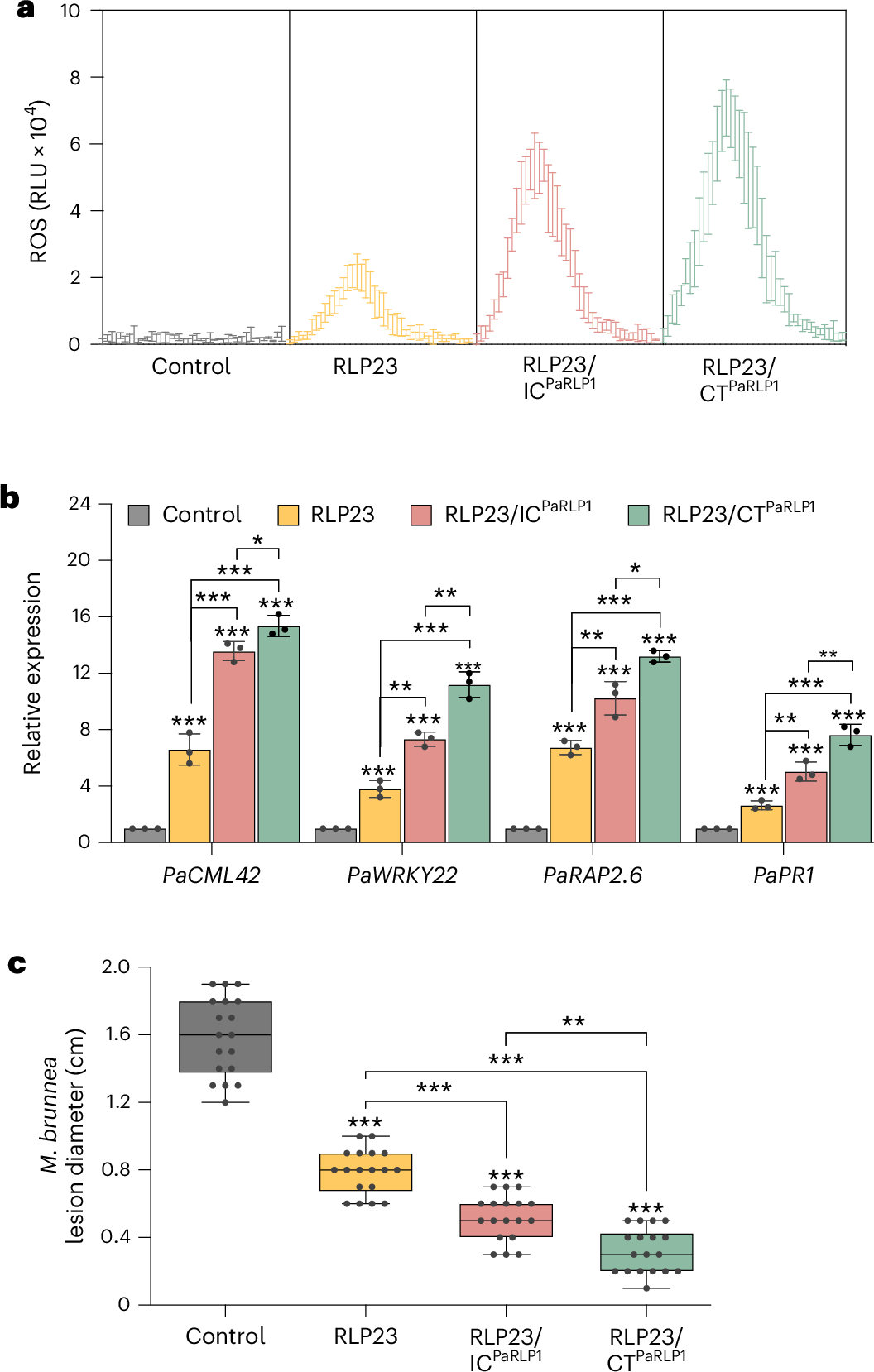
图 14.P1 论文原图:工程化 PRR 把广谱抗性推向跨作物部署。原图为 Yang et al. (2025) Nature Biotechnology Fig. 5,DOI: 10.1038/s41587-025-02858-8。该图展示 RLP23 工程策略在不同植物体系中的可迁移性,直接对应本节“PTI 强化与非 NLR 抗病策略”的育种含义。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
感病基因(S 基因)的敲除
另一种颠覆性的思路是:不是给植物"加武器",而是"去掉弱点"。许多病原的成功侵染依赖于宿主的特定基因——这些基因在正常发育中有功能,但被病原"劫持"用于促进感染。敲除或功能修饰这些"感病基因"(Susceptibility gene, S gene)可以赋予植物广谱而持久的抗性 (van Schie & Takken, 2014)。
最成功的案例是 MLO 基因:大麦 mlo 突变体对白粉菌的抗性已在田间验证了超过40年而未被克服——这可能是已知最持久的抗性案例 (Kusch & Panstruga, 2017)。CRISPR 技术使得在作物中精确敲除 S 基因成为现实——小麦、番茄和水稻的 MLO 同源基因已被成功编辑。
然而,S 基因策略面临一个内在矛盾:S 基因之所以存在于植物基因组中,通常是因为它们有正常的生理功能——敲除它们可能带来发育缺陷或其他胁迫下的不利影响。例如,mlo 突变体虽然抗白粉菌,但在某些条件下表现出自发坏死和对坏死营养型病原的易感性增加 → 第11章。精确编辑 S 基因的特定结构域(使其丧失被病原利用的功能但保留正常生理功能)是解决这一矛盾的关键方向。
HIGS 与 RNAi 抗病
宿主诱导基因沉默(HIGS)策略——在转基因植物中持续表达靶向病原关键基因的 dsRNA——已在多种病理系统中展示了保护效果 → 第13章 13.4节。HIGS 的优势在于靶标可以精确设计,且病原通过突变逃避沉默的进化空间较小(需要靶标序列的广泛变异而不影响基因功能)。但其大规模应用仍面临转基因作物的监管限制和公众接受度问题。
14.4组合部署:堆叠、轮换与区域管理
即使拥有完美的单一抗性基因,如果部署策略不当,抗性也注定被克服。部署策略决定了抗性的寿命——这一认识正在将抗病育种从"基因猎人"模式转向"系统工程师"模式。
基因堆叠(Gene stacking / Gene pyramiding)
将多个针对同一病原的 R 基因堆叠到同一品种中,大幅提高病原同时克服所有抗性的概率门槛。理论预测表明:如果单基因抗性被克服的概率为 p,那么n个独立基因的堆叠将克服概率降至 p^n——这一指数效应使得3-5个基因的堆叠在理论上极难被突破 (McDonald & Linde, 2002)。
但堆叠策略的实践面临两个关键挑战:
- 上位性和适应度代价:多个 NLR 基因共存于一个基因组中可能产生自身免疫(hybrid necrosis 样效应)→ 第6章 6.4节,或累积生长代价。需要仔细测试堆叠组合的兼容性。
- 遗传连锁和育种难度:许多 NLR 基因聚集在基因组的特定区域(NLR 基因簇),导致不同抗性等位基因在遗传重组中难以分离和重新组合。
时间和空间部署策略
除了在同一品种中堆叠基因,还可以通过时空策略分散选择压力:
- 品种轮换:在不同年份种植携带不同 R 基因的品种,防止病原群体对单一 R 基因产生定向选择。
- 品种混合(Multiline/mixture):在同一田块中混种携带不同 R 基因的品种,通过群体水平的多样性降低病原传播效率和选择强度 (Mundt, 2002)。
- 区域管理:在更大的地理尺度上协调 R 基因的部署,避免大面积种植携带相同 R 基因的品种——这需要育种者、种子公司和政策制定者的协调合作。
14.5基因编辑时代的新工具
CRISPR-Cas 系统的出现从根本上改变了抗病育种的工具箱——从被动利用自然变异转向主动创造定制化的遗传改良。
精确编辑的应用场景
- S 基因精确编辑:如前述 MLO 的敲除。CRISPR 还可以实现更精细的操作——仅修改 S 基因中被病原利用的特定氨基酸,保留其正常功能。
- 启动子编辑调控表达水平:通过编辑 R 基因或 PRR 的启动子区域,微调其表达水平和时空模式——例如增强 R 基因在高感染风险时期或器官的表达,同时降低其在其他时间的基线表达以减少代价。
- 调控区域编辑优化激素平衡:编辑 SA-JA 信号网络中关键调控因子的顺式调控元件,优化免疫-生长平衡 → 第11章。
碱基编辑和 Prime editing
碱基编辑器(ABE、CBE)和 Prime editing 可以在不产生双链断裂的情况下引入单核苷酸变异——这对于修改 NLR 的识别特异性(改变 LRR 结构域中的关键残基)或修复 S 基因中被病原利用的位点特别有价值。
监管前景
基因编辑作物(特别是不含外源DNA的编辑类型)在部分国家(如美国、日本、阿根廷)已被纳入与传统育种品种相同的监管框架,大幅加速了产品的开发和推广。但在欧盟等地区,编辑作物仍被归类为 GMO,面临严格限制。这种监管不一致性是影响编辑抗病品种全球推广的重要非技术因素。
能否构建"抗病-产量-品质"三目标同步优化的育种管线?
传统育种中,抗病性、产量和品质常常表现为部分拮抗的性状——增强抗性可能降低产量或改变品质。但 Deng et al. (2017) 的 Pigm 工作表明,通过精妙的表观遗传调控可以实现抗性与产量的兼顾。基因编辑技术使得对调控区域的精确操控成为可能——理论上,可以构建一条"多目标同步优化"的育种管线:在编辑 S 基因增强抗性的同时,优化产量相关基因的表达;在堆叠 NLR 的同时,编辑自身免疫抑制因子防止代价叠加。但这需要对免疫-生长-品质的调控网络有比目前更深入的系统理解 → 第11章、→ 第16章。
14.6里程碑研究思路拆解
里程碑 1:Dangl, Horvath & Staskawicz (2013) — 从机制拆解到部署工程
面对的问题:为何免疫机制研究的丰硕成果未能同步转化为田间的持久抗性?基础研究和应用之间的"死亡谷"在哪里?
关键思路:系统回顾30年来 R 基因克隆和部署的历史,提出"设计-验证-部署"一体化的转化框架。核心论断是:转化瓶颈不在于发现(我们已经克隆了数百个 R 基因),而在于部署策略的系统化——需要从"一个基因一个品种"的线性思维转向多基因组合、动态管理的系统思维。
关键证据链:通过历史案例分析(如小麦锈病、水稻稻瘟病的 R 基因部署史)总结了失败的共同模式——大面积单一 R 基因部署 → 强定向选择 → 快速克服。同时指出了成功案例的共同特征——多基因堆叠、定量抗性利用、品种多样性部署。
影响:这篇综述在植物免疫学界引发了从"发现导向"到"工程导向"的范式讨论,推动了 NLR 工程化和编辑抗病策略的兴起。
里程碑 2:Deng et al. (2017) — Pigm:抗性与产量兼顾的表观遗传解决方案
面对的问题:广谱抗性基因往往伴随严重的产量损失——能否找到一种机制,使抗性在需要时充分表达,不需要时降低到最低?
关键思路:Pigm 位点包含一对串联的 NLR 基因:PigmR 赋予广谱抗稻瘟病性但降低产量,PigmS 竞争性抑制 PigmR 但恢复产量。两者的表达比例通过启动子区域的 DNA 甲基化进行表观遗传调控。
关键证据链:(1)PigmR 过表达增强抗性但降低种子大小;(2)PigmS 与 PigmR 竞争形成异源二聚体,抑制后者的免疫信号;(3)PigmS 的表达水平受 DNA 甲基化调控——在花粉发育关键期 PigmS 表达上升以保证产量,在营养生长期 PigmR 优势表达以维持抗性。
影响:提供了一个"抗性不等于代价"的精妙范例,证明通过调控两个基因的表达平衡可以同时优化抗性和产量——这一思路可以被推广到其他 NLR 对的工程化。
14.7当前争论与未解问题
- 如何在育种早期预测 R 基因被克服的风险?病原的进化潜力(有效群体大小、突变率、重组频率、Avr 基因的必要性)决定了 R 基因的预期寿命。能否建立一套"抗性耐久性风险评估"工具,在基因部署前预测其被克服的时间尺度?
- NLR 工程化规则是否可跨作物迁移?在水稻 Pik 系统中验证的 HMA 结构域修改,在小麦或番茄的 NLR 中是否可以类比操作?不同作物的 NLR 信号通路配置差异如何影响工程化 NLR 的功能?
- 如何标准化抗病-产量-品质三目标评估?目前抗性评价主要在温室条件下使用单一病原进行,产量和品质评价在田间进行——两者往往由不同团队在不同条件下完成。需要建立整合的多目标评价体系。
- 基因编辑作物的监管框架如何走向全球协调?当前各国对编辑作物的分类和监管差异巨大,严重影响了技术的全球推广和国际贸易。科学界能否推动基于产品(而非过程)的监管框架?
- PTI 强化策略的耐久性是否如预期的那样高?理论上 PRR 转移的耐久性高于 NLR,但长期田间数据仍然缺乏。病原是否能通过修改 MAMP 或产生 PTI 抑制性效应子来克服 PRR 介导的抗性?
2025 年的两类工作使这一争论更具体:一类是细胞表面合成免疫受体工程,尝试把可识别模块与植物免疫输出模块重新组合 (Yang et al., 2025);另一类是可激活 NLR 工程,把病原蛋白酶活性转化为触发免疫的开关 (Wang et al., 2025)。它们共同指向一个新的育种问题:未来抗病育种不只是“导入哪个天然 R 基因”,而是“设计怎样的识别逻辑、激活阈值和部署组合”。这也意味着田间评价必须从单一抗病表型扩展到稳定性、代价、病原逃逸路径和监管可接受性。
14.8关键实验方法
| 实验方法 | 用途 | 经典文献 |
|---|---|---|
| QTL/GWAS + 精细定位 | 在自然群体中鉴定抗性关联位点,精细定位到候选基因 | Poland et al., 2009, PNAS |
| RenSeq(R 基因富集测序) | 快速获取物种的完整 NLR 库存清单,加速 R 基因克隆 | Steuernagel et al., 2016, Plant Biotechnol J |
| CRISPR 与转基因验证 | 构建并验证抗性模块,精确编辑 S 基因或调控区域 | Borrelli et al., 2018, Plant Biotechnol J |
| 多病原谱挑战 | 评估改造后的抗性模块对不同病原小种/种群的广谱性 | Kourelis & van der Hoorn, 2018, Plant Cell |
| 多点田间试验 | 在不同环境和病原压力下验证抗性的耐久性和产量效应 | Mundt, 2018, Phytopathology |
14.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
14.10参考文献
- Dangl JL, Horvath DM, Staskawicz BJ. Pivoting the plant immune system from dissection to deployment. Science, 2013, 341: 746–751.
- De la Concepcion JC, Franceschetti M, MacLean D, et al. Protein engineering expands the effector recognition profile of a rice NLR immune receptor. eLife, 2019, 8: e47713.
- Deng Y, Zhai K, Xie Z, et al. Epigenetic regulation of antagonistic receptors confers rice blast resistance with yield balance. Science, 2017, 355: 962–965.
- Dong OX, Ronald PC. Genetic engineering for disease resistance in plants: recent progress and future perspectives. Plant Physiol, 2019, 180: 26–38.
- Kim SH, Qi D, Ashfield T, et al. Using decoys to expand the recognition specificity of a plant disease resistance protein. Science, 2016, 351: 684–687.
- Kourelis J, van der Hoorn RAL. Defended to the nines: 25 years of resistance gene cloning identifies nine mechanisms for R protein function. Plant Cell, 2018, 30: 285–299.
- Kusch S, Panstruga R. mlo-based resistance: an apparently universal "weapon" to defeat powdery mildew disease. Mol Plant-Microbe Interact, 2017, 30: 179–189.
- Lacombe S, Rougon-Cardoso A, Sherwood E, et al. Interfamily transfer of a plant pattern-recognition receptor confers broad-spectrum bacterial resistance. Nat Biotechnol, 2010, 28: 365–369.
- McDonald BA, Linde C. Pathogen population genetics, evolutionary potential, and durable resistance. Annu Rev Phytopathol, 2002, 40: 349–379.
- Mundt CC. Use of multiline cultivars and cultivar mixtures for disease management. Annu Rev Phytopathol, 2002, 40: 381–410.
- Nelson R, Wiesner-Hanks T, Wisser R, Balint-Kurti P. Navigating complexity to breed disease-resistant crops. Nat Rev Genet, 2018, 19: 21–33.
- Savary S, Willocquet L, Pethybridge SJ, et al. The global burden of pathogens and pests on major food crops. Nat Ecol Evol, 2019, 3: 430–439.
- Steuernagel B, Periyannan SK, Hernández-Pinzón I, et al. Rapid cloning of disease-resistance genes in plants using mutagenesis and sequence capture. Nat Biotechnol, 2016, 34: 652–655.
- Steuernagel B, Jupe F, Witek K, et al. NLR-parser: rapid annotation of plant NLR complements. Bioinformatics, 2015, 31: 1665–1667.
- Tamborski J, Krasileva KV. Evolution of plant NLRs: from natural history to precise modifications. Annu Rev Plant Biol, 2020, 71: 355–378.
- van Schie CCN, Takken FLW. Susceptibility genes 101: how to be a good host. Annu Rev Phytopathol, 2014, 52: 551–581.
- Wang X, Ji C, Wang L, et al. Remodelling autoactive NLRs for broad-spectrum immunity in plants. Nature, 2025, 645: 737–745. DOI: 10.1038/s41586-025-09252-z.
- Yang Y, Steidele CE, Huang X, et al. Engineered pattern recognition receptors enhance broad-spectrum plant resistance. Nat Biotechnol, 2025. DOI: 10.1038/s41587-025-02858-8.