PTI 与 ETI 的关系演变
从泰然二分到深度交织,这对概念的演变史折射了整个领域的思想变迁
本章目录
- Flor 的基因对基因假说:一切的起点
- Zigzag 模型:将免疫分成两个层级
- PTI-ETI 协同放大:二元边界的崩塌
- Invasion Model 与免疫识别的统一视角
- 当下的开放讨论:我们还需要 PTI/ETI 这对术语吗?
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
科学概念的命运往往比发明它们的人更跌宕。PTI(Pattern-Triggered Immunity)和 ETI(Effector-Triggered Immunity)这对术语自2006年被正式提出以来,经历了从被奉为金科玉律到被质疑是否仍有存在必要的完整生命周期——而这一切仅仅发生在不到二十年间。
理解这对概念的演变史,不仅是理解植物免疫研究的必经之路,更是观察科学范式如何诞生、成熟、遭遇挑战并被修正的一个绝佳窗口。我们将看到,最具影响力的模型往往不是因为”正确”才成功,而是因为它在正确的时间提供了一个足够好的思考框架——直到新的证据迫使我们重新审视那些曾经被默认接受的假设。
本章将追溯这段概念史:从 Flor 的基因对基因假说出发,经过 Zigzag 模型的建立,到2021年 PTI-ETI 协同放大证据的爆发,再到 Invasion Model 对免疫识别的统一性重新阐释。最后,我们将面对一个正在被激烈讨论的问题:我们还需要 PTI/ETI 这对术语吗?
2.1Flor 的基因对基因假说:一切的起点
PTI 与 ETI 的故事,必须从一个更古老的概念讲起。
1940年代至1970年代,美国农业部的 Harold H. Flor 在北达科他州的亚麻锈病系统(Linum usitatissimum–Melampsora lini)中进行了长达三十年的遗传分析。他的核心发现可以用一句话概括:宿主中每一个决定抗性的基因(R 基因),在病原中都有一个对应的决定无毒性的基因(Avr 基因) (Flor, 1971)。只有当 R 基因与对应的 Avr 基因同时存在时,才会触发抗性反应;任何一方缺失,互作结果就是感病。
这一”基因对基因假说”(gene-for-gene hypothesis)具有惊人的预测力和简洁性。在分子生物学工具尚未成熟的年代,它仅凭遗传学数据就准确地预言了植物抗病性的基本逻辑——一种高度特异性的分子识别关系。但这个假说也埋下了一个深远的概念陷阱:它天然地暗示 R-Avr 互作是一种”直接的、受体-配体式的识别”。正如我们在第1章讨论的,后来的保卫假说和诱饵模型表明,间接识别可能才是更普遍的机制 → 第1章 1.3节。
从”特异性抗性”到”基础抗性”:被忽视的另一半
Flor 的体系完美地解释了品种间的特异性抗性差异,但它没有回答另一个同样重要的问题:当 R-Avr 识别不发生时,植物就完全没有防御了吗?
答案显然是否定的。即使在”兼容互作”(compatible interaction,即缺乏有效 R-Avr 配对)中,植物仍然会激活一定程度的防御反应——只是不足以完全阻止病原。这种非特异性的、广泛存在的基础防御,在很长一段时间内被称为”基础抗性”(basal resistance)或”水平抗性”(horizontal resistance),但其分子机制一直不如 R 基因抗性那样清楚。
直到1990年代末至2000年代初,随着第一批 PRR(Pattern Recognition Receptor)的鉴定——特别是拟南芥中识别细菌鞭毛蛋白的 FLS2 (Gómez-Gómez & Boller, 2000) 和识别延伸因子的 EFR (Zipfel et al., 2006)——“基础抗性”才获得了清晰的分子解释:它在很大程度上就是 PRR 介导的模式触发免疫(PTI)。
至此,两条研究线索——Flor 体系的特异性 R 基因抗性和 PRR 介导的非特异性基础抗性——像两条独立的河流,各自流淌了数十年后即将汇合。2006年的 Zigzag 模型,正是这次汇合的产物。
2.2Zigzag 模型:将免疫分成两个层级
2006年,Jonathan Jones 和 Jeffery Dangl 在Nature上发表了题为”The plant immune system”的综述,提出了日后被称为”Zigzag 模型”的概念框架 (Jones & Dangl, 2006)。这篇论文迄今已被引用超过一万次,是植物免疫领域——或许也是整个植物科学领域——被引用最多的单篇文献之一。
模型的核心逻辑
Zigzag 模型将植物与病原的互作描述为一场持续升级的分子军备竞赛,分为四个阶段:
- PTI 建立:植物表面 PRR 识别病原保守的分子模式(PAMP/MAMP),激活基础免疫反应(PTI)。此时免疫”幅度”(amplitude)升高,大多数非适应性病原被阻止。
- 效应子抑制(ETS):成功的病原通过分泌效应蛋白抑制 PTI 信号通路的关键节点,将免疫幅度压低到病原可以增殖的水平——即效应子触发的易感性(Effector-Triggered Susceptibility, ETS)。
- ETI 反击:植物的 NLR 受体通过直接或间接方式识别效应蛋白,重新激活强烈的免疫反应(ETI),通常伴随超敏细胞死亡(HR)。免疫幅度跃升至更高水平。
- 新一轮军备竞赛:病原通过丢弃被识别的效应蛋白、进化新效应蛋白或获得新的 PTI 抑制手段逃避 ETI。植物则进化新的 NLR 来识别新效应蛋白。如此交替循环,形成”之字形”的免疫幅度波动。
图 2.1 Zigzag 模型示意图。植物通过 PRR 识别建立 PTI,病原效应蛋白压低免疫幅度形成 ETS,NLR 识别效应蛋白后触发更强 ETI;随后病原逃逸、植物再进化新识别能力,形成之字形的共进化波动。
模型的革命性贡献
Zigzag 模型的成功并非因为它发现了新的实验事实——它是一篇综述,不包含原始数据。它的真正贡献在于概念整合:
- 统一了两个领域:将此前相对独立的 PAMP 识别研究和 R 基因抗性研究放入同一个框架,建立了清晰的层级关系。
- 引入了动态视角:用”幅度”的涨落取代了静态的”抗/感”二分法,暗示免疫是一个连续的、可量化的过程。
- 赋予效应蛋白双重身份:效应蛋白既是病原的武器(抑制 PTI),又是植物的靶标(触发 ETI)。这一洞见直接推动了此后十五年间大量效应蛋白功能研究。
- 提供了可操作的实验范式:”PTI → ETS → ETI”的叙事为实验设计提供了明确的逻辑:识别 PAMP/PRR → 鉴定效应蛋白及其靶标 → 发现对应的 NLR。
隐含的假设与局限
然而,Zigzag 模型在巨大成功的同时也固化了几个关键假设,这些假设在后续研究中逐一受到挑战:
假设一:PTI 和 ETI 是独立运作的两个层次。在 Zigzag 模型的叙事中,PTI 被效应蛋白”关闭”后,ETI 才被”打开”——两者似乎是一种替代关系而非协同关系。模型图中的免疫幅度在 ETS 阶段降至基线以下,暗示 PTI 在效应蛋白存在时基本失效。
假设二:PTI 是”弱”的,ETI 是”强”的。模型图中 ETI 的幅度远高于 PTI,给人的印象是 PTI 只能提供基本防御,真正有效的抗性来自 ETI。但实际上,PRR 介导的免疫在自然界中可能承担了大部分防御工作——毕竟大多数微生物从未成功突破 PTI (Zipfel, 2014)。
假设三:所有 PAMP 识别都是”模式触发”的,所有效应蛋白识别都是”效应子触发”的。但某些效应蛋白在质外体活动并被表面受体识别(如Cladosporium fulvum的 Avr 蛋白被 Cf 受体蛋白识别),而某些 PAMP 的识别方式与效应蛋白的间接识别高度相似。PTI/ETI 的划分标准——是按识别的位置(细胞表面 vs 细胞内)、识别的对象(保守模式 vs 效应蛋白)、还是反应的强度?——从未被明确统一 (Thomma et al., 2011)。
Zigzag 模型是一个优秀的教学工具,但不完美的科学模型。它的价值在于为整个领域提供了共同语言和思考框架,使得不同实验室的发现可以被放入统一的叙事中讨论。但正是这种统一性,也可能限制了我们看到不符合框架之证据的能力。理解一个模型的假设与局限,与理解它的贡献同样重要。
2.3PTI-ETI 协同放大:二元边界的崩塌
如果说 Zigzag 模型是植物免疫领域的”标准模型”,那么2021年初同时发表在Nature和Science上的两篇论文,就是对这个标准模型最有力的修正——甚至可以说是一次概念地震。
裂缝的出现:2006-2020年间的不和谐音符
在 Ngou 和 Yuan 的工作发表之前,Zigzag 模型的”两层独立”假设已经面临越来越多的质疑,只是这些质疑还没有凝聚成一个替代性框架:
- Tsuda & Katagiri (2010) 的网络分析表明,PTI 和 ETI 共享大量下游信号组分——SA、JA、ET 和 PAD4 通路在两种免疫反应中均被激活,只是程度和动态不同。
- 多项研究观察到,ETI 的标志性输出(如持续的 ROS 爆发、胼胝质大量沉积、PR 基因高表达)在 PTI 信号组分缺失的背景下会显著减弱 (Lu et al., 2010; Zhang et al., 2010)。
- 转录组学比较显示,PTI 和 ETI 诱导的基因表达变化在种类上高度重叠(约70%的 ETI 差异表达基因也被 PTI 诱导),差异主要体现在幅度和持续时间而非基因种类 (Tao et al., 2003; Navarro et al., 2004)。
这些证据像是一面墙上的裂缝——每一条单独看都不致命,但汇总起来清楚地暗示:PTI 和 ETI 并非两个独立的信号通路,而是共用同一套信号基础设施的两种激活模式。
关键突破:2021年的两篇论文
Ngou et al. (2021, Nature)在拟南芥中构建了一个精巧的实验系统:利用雌二醇诱导型启动子控制细菌效应蛋白 AvrRps4 的表达,从而在没有细菌感染(因此没有 PAMP 刺激)的条件下,单独激活 ETI 通路。他们发现:
- 单独激活 ETI(不伴随 PTI)仅产生微弱的 ROS 爆发和极低水平的胼胝质沉积——远低于正常细菌感染时的水平。
- 当 ETI 激活与 PAMP(flg22)处理同时进行时,ROS 爆发和胼胝质沉积出现了超加性效应(superadditive effect)——即协同输出远大于两者单独之和。
- ETI 激活后,PTI 通路关键组分(包括 PRR 共受体 BAK1/SERK4 和 RBOHD)的蛋白水平显著上调,表明 ETI 主动增强 PTI 的信号基础设施。
Yuan et al. (2021, Science)则从反方向验证了相同结论:他们构建了 PRR 信号几乎完全缺失的拟南芥多重突变体(fls2 efr cerk1 lyk5 bak1-5 bkk1-1等组合),发现在这些背景下,NLR 介导的 ETI 反应(包括对Pst DC3000 携带 AvrRps4 的抗性)大幅减弱。关键发现包括:
- 在 PTI 信号缺失的多重突变体中,ETI 激活的转录重编程规模显著缩小。
- SA 积累——ETI 的核心输出之一——在 PRR 缺陷背景下显著降低。
- ETI 激活后,FLS2、EFR 等 PRR 的转录水平在2-6小时内显著上升,形成一个正反馈环路:ETI 增强 PTI 的感知能力,而增强的 PTI 又为 ETI 提供更强的效应输出平台。
图 2.2 PTI-ETI 协同放大的分子机制模型。PTI 提供可快速启动的信号底盘,ETI 通过转录和蛋白水平增强 PRR、共受体、RBOHD 与激素模块,两者形成正反馈,从而产生强于单独激活的防御输出。
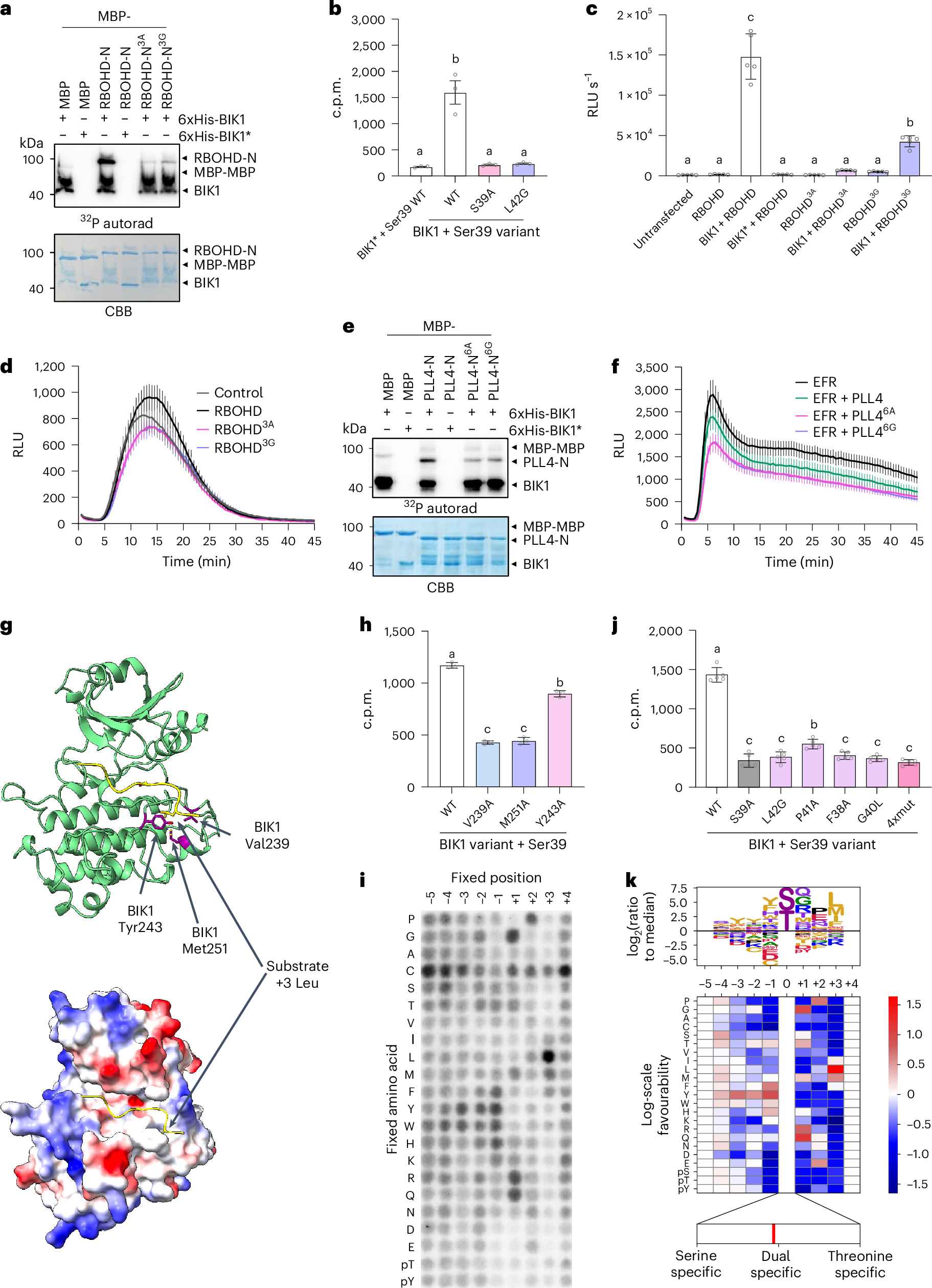
图 2.P1 论文原图:BIK1 底物图谱把 PTI 与 ETI 的共享底盘具体化。原图为 Toth et al. (2026) Nature Plants Fig. 1,DOI: 10.1038/s41477-025-02218-z。该图显示 PRR 相关 RLCK 枢纽 BIK1 的底物范围可延伸到多类免疫调控节点和 NLR 受体,有助于理解 PTI 与 ETI 并非两条孤立通路,而是在早期激酶层发生交汇。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
协同模型的核心逻辑
综合两项研究,PTI-ETI 协同放大模型可以概括为:
- PTI 提供信号基础设施:PRR 信号通路的组分(RBOHD、MAPK 级联、转录因子等)是 ETI 输出执行的必要平台。没有这个平台,ETI 的信号”有指令但缺工具”。
- ETI 提供信号放大引擎:NLR 激活后,通过转录上调 PRR 和共受体的表达,增强 PTI 通路的感知灵敏度和效应输出能力。ETI 像一个”增益放大器”,把 PTI 的音量旋钮从”低”拧到”高”。
- 正反馈环路形成协同效应:两个层次形成相互增强的正反馈环,产生远超单独之和的防御输出。这解释了为什么完整的抗性反应需要两个系统的协同运作。
- 时间维度的分工:PTI 提供快速(秒至分钟级)的初始响应,ETI 在数小时内通过转录重编程增强和维持这一响应。两者的时间尺度互补,确保防御既快速又持久。
协同模型的边界与未解问题
协同模型虽然令人信服,但也有其局限性需要清醒认识:
物种普遍性:两篇论文的核心实验均在拟南芥中完成。在作物系统中,PTI-ETI 协同的定量程度可能不同。例如,水稻的 NLR 蛋白 Pigm 直接在细胞核中调控免疫基因转录,其 ETI 对 PTI 基础设施的依赖程度可能低于拟南芥系统 (Deng et al., 2017)。
NLR 类型依赖性:不同类型的 NLR(TNL vs CNL vs RNL)激活后的下游机制不同。TIR 域 NLR(TNL)通过产生小分子信号激活 EDS1-PAD4-ADR1 辅助 NLR 通路 (Lapin et al., 2022),而 CC 域 NLR(CNL)如 ZAR1 直接形成质膜孔道 (Wang et al., 2019)。这两类 NLR 对 PTI 底盘的依赖是否一致?初步证据提示可能存在差异 → 第4章。
生态学真实性:实验室中通常使用单一 PAMP 和单一效应蛋白研究协同效应。但在自然感染中,植物同时面对多种 PAMP 和多种效应蛋白的复杂组合,协同效应的实际表现可能更为复杂。
协同模型的根本意义不仅在于”PTI 和 ETI 会互相帮忙”,更在于它打破了层级思维:PTI 不再是”被动的第一层”,ETI 也不再是”独立的终极武器”。两者更像是同一个防御网络的两种激活入口,共享同一套执行机器。这一认识对育种策略有深远影响——仅仅堆叠 R 基因而忽视 PRR 系统的健全性,可能无法获得预期的抗性增益 → 第14章。
2.4Invasion Model 与免疫识别的统一视角
如果 PTI 和 ETI 并非泾渭分明的两层,那么植物免疫识别的本质究竟是什么?早在协同模型被实验验证之前,就有研究者试图从更根本的层面重新审视这个问题。
Thomma 等人的质疑
2011年,Thomma、Nürnberger 和 Scheel 在Trends in Plant Sciences上发表了一篇尖锐的评论,直接质疑 PTI/ETI 二分法的合理性 (Thomma et al., 2011)。他们指出了几个难以调和的矛盾:
- 分类标准不一致:PTI/ETI 的划分到底是基于配体的性质(保守模式 vs 效应蛋白)、受体的位置(表面 vs 细胞内)、还是反应的强度?不同的标准会给出不同的分类结果。
- ”灰色地带”案例太多:番茄 Cf 蛋白在细胞表面识别C. fulvum的 Avr 效应蛋白——按受体位置应归为 PTI,按配体性质应归为 ETI。乙烯诱导的 xylanase(EIX)是微生物分泌的蛋白,被番茄 LeEIX2 受体识别——它是 PAMP 还是效应蛋白?
- 进化连续性被忽视:许多”效应蛋白”实际上是微生物正常生理活动的副产物,只是恰好被植物免疫系统识别。将它们与有明确毒力功能的 T3SS 效应蛋白归为同一类别,可能掩盖了识别机制的多样性。
Invasion Model 的提出
基于这些质疑,Cook、de Wit 和 Thomma (2015) 正式提出了”入侵模型”(Invasion Model)。该模型的核心主张是:放弃按配体类型划分免疫层次,转而按照”入侵模式”(invasion pattern, IP)的概念统一所有免疫识别。
在 Invasion Model 中:
- 所有被植物免疫系统识别的分子信号统称为”入侵模式”(IP),不再区分 PAMP 和效应蛋白。IP 可以是微生物保守分子(如 flg22)、效应蛋白、损伤相关分子(DAMP)、或任何暗示”入侵正在发生”的分子线索。
- 所有免疫受体统称为”入侵模式受体”(IP receptor, IPR),不再区分 PRR 和 NLR。IPR 的功能本质是一样的:感知入侵信号,启动防御。
- 免疫反应的强度和性质不取决于识别层次的”级别”,而取决于信号的强度、持续时间和下游网络的配置。
图 2.3 Zigzag 模型与 Invasion Model 的概念对比。Zigzag 模型按 PAMP 与效应蛋白区分 PTI/ETI;Invasion Model 则把所有能提示入侵的分子统一称为入侵模式,把受体统一看作入侵模式受体,强调免疫输出由信号情境而非名称决定。
Invasion Model 的优势与争议
Invasion Model 的最大优势在于概念简洁性:它消除了 PTI/ETI 边界处的分类困难,将所有免疫识别纳入同一框架。它也更好地容纳了一些”不合群”的识别系统——例如 Cf 蛋白对质外体效应蛋白的识别、NLR 对 PAMP 的胞内识别等。
但 Invasion Model 也面临批评:
- 可能过于抽象:通过消除所有分类,它可能让初学者失去了组织知识的”抓手”。PTI/ETI 虽然不完美,但作为教学工具确实有效。
- 回避了机制差异:表面受体(RLK/RLP)和细胞内受体(NLR)在结构、信号转导机制和进化动态上确实存在根本差异。将它们统称为 IPR 可能掩盖这些重要的机制区别。
- 缺乏新的实验预测:一个好的模型应该能做出可检验的预测。Invasion Model 主要是一种重新分类方案,它提出了什么 Zigzag 模型无法做出的新预测?这一点尚不明确。
Pruitt、Gust 和 Nürnberger (2021) 在Nature Plants上发表的评论文章”Plant immunity unified”试图进一步发展 Invasion Model,整合2021年的协同证据。他们提出,免疫识别应该按受体位置(细胞表面 vs 细胞内)来分类,而非按配体类型。这一分类标准至少是明确的、可操作的,并且与信号转导机制的差异有更好的对应关系 (Pruitt et al., 2021)。
2.5当下的开放讨论:我们还需要 PTI/ETI 这对术语吗?
经过上述概念演变,一个实际问题浮出水面:在2020年代的语境下,PTI 和 ETI 这对术语还应该继续使用吗?
学界目前大致存在三种立场:
立场一:继续使用,但重新定义
持这一立场的研究者(包括 Ngou 和 Yuan 论文的部分作者)认为,PTI/ETI 术语已深深嵌入领域的语言习惯和文献体系中,废除它们的实际成本远高于收益。更务实的做法是保留术语,但明确修正其含义:PTI 指由细胞表面受体(RLK/RLP)介导的免疫,ETI 指由细胞内受体(NLR)介导的免疫,两者不再是独立的层级,而是协同运作的平行系统 (Ngou et al., 2022)。
立场二:逐步淘汰,过渡到新框架
Thomma 等人和 Invasion Model 的支持者认为,PTI/ETI 术语携带着太多历史包袱——“pattern”暗示保守性,”effector”暗示毒力功能——这些隐含的假设会持续误导思考。长远来看,应该过渡到更中性的术语体系,如”表面受体介导的免疫”(surface receptor-mediated immunity)和”细胞内受体介导的免疫”(intracellular receptor-mediated immunity)(Thomma et al., 2011; Cook et al., 2015)。
立场三:这根本不是最重要的问题
也有研究者认为,术语之争在很大程度上是一种”语义学陷阱”。真正重要的不是如何命名,而是如何建模——理解每一种具体的受体-配体对在特定病理系统中的定量贡献和互作关系。在实际研究中,研究者关心的是”FLS2 和 ZAR1 如何协同工作”,而不是”这算 PTI 还是 ETI”(DeFalco & Zipfel, 2021)。
术语之争的实质不是”谁起的名字好听”,而是不同的命名方案隐含了不同的思维框架。使用 PTI/ETI 术语时,我们不自觉地倾向于将免疫视为层级式的;使用 IP/IPR 术语时,则倾向于将免疫视为网络式的。两种框架各有盲区。本书出于教学便利,将继续使用 PTI/ETI 术语,但读者应始终记住:这对术语描述的是一个连续谱上的两端,而非两个离散的实体。
如果放弃 PTI/ETI 二分法,什么框架能更好地描述植物免疫识别的全貌?
这个问题目前没有共识答案。Invasion Model 提供了一个更统一但也更抽象的框架。”表面受体 vs 细胞内受体”的分类在机制上更清晰,但仍然是二分的。也许未来的最优框架不是二元的,而是一个多维的”免疫空间”——受体类型、配体性质、信号动态、输出模式各为一个维度,每种具体的免疫反应占据这个空间中的一个点。这种”参数化”的思维方式已经在系统免疫学(systems immunology)领域崭露头角 → 第12章。
对于实际研究,最重要的可能不是选择哪个框架,而是在使用任何框架时都保持对其假设的清醒意识。一旦模型从”有用的工具”变成”不言自明的真理”,科学进步就会减速。
2.6里程碑研究思路拆解
里程碑 1:Ngou et al. (2021) — ETI 需要 PTI 底盘
面对的问题:Zigzag 模型将 PTI 和 ETI 描述为独立的两层防御。但如果真的独立,为什么在某些 PTI 缺陷突变体中,ETI 反应也会减弱?
关键思路:要测试 ETI 是否依赖 PTI,需要在没有 PAMP 刺激的条件下单独激活 ETI——但正常细菌感染总是同时提供 PAMP 和效应蛋白。解决方案是使用化学诱导系统:将效应蛋白 AvrRps4 置于雌二醇诱导型启动子控制下,在无菌条件下用雌二醇单独激活 ETI。
关键证据链:(1)单独 ETI 产生的 ROS 和胼胝质极少;(2)ETI + flg22 产生超加性效应;(3)ETI 激活上调 BAK1/SERK4/RBOHD 蛋白水平;(4)在 bak1/serk4 双突变体中,ETI 介导的抗性大幅减弱。
实验设计的精巧之处:诱导型系统解决了"分离 PTI 和 ETI"这一长期技术难题。同时,作者使用了蛋白水平(而非仅转录水平)的检测来证明 ETI 上调 PRR 组分,增加了结论的可靠性。
局限性:诱导系统的时间动态可能与自然感染不完全一致;雌二醇本身可能有微弱的生理效应需要排除。
里程碑 2:Tsuda & Katagiri (2010) — PTI 与 ETI 的信号网络比较
面对的问题:PTI 和 ETI 的下游信号通路究竟是独立的还是共享的?此前的研究多聚焦于单个通路,缺乏系统性比较。
关键思路:利用拟南芥的信号突变体组合(sid2、dde2、ein2、pad4等单突变和多重突变),在 PTI 和 ETI 条件下分别测量细菌增殖终点,通过定量网络分析评估各信号扇区的贡献。
关键证据链:(1)SA、JA、ET 和 PAD4 四个信号扇区在 PTI 和 ETI 中均有贡献,但权重不同;(2)PTI 中各扇区呈加性贡献,ETI 中则呈现显著的冗余性补偿——单个扇区缺失对 ETI 影响不大,但多个同时缺失则导致急剧崩溃;(3)这种网络拓扑差异可以用数学模型形式化描述。
影响:这是第一项用网络思维系统分析 PTI/ETI 关系的工作,为后来的协同模型奠定了概念基础。"信号网络共享但拓扑不同"的结论至今仍是该领域的核心认知。
里程碑 3:Cook, de Wit & Thomma (2015) — Invasion Model 的正式提出
面对的问题:PTI/ETI 二分法存在无法自洽的分类困难——同一种分子信号在不同标准下会被归入不同类别。
关键思路:提出用"入侵模式"(Invasion Pattern, IP)统一取代 PAMP 和效应蛋白的分类,用"入侵模式受体"(IPR)统一取代 PRR 和 NLR 的分类。不是发现新事实,而是提出新的组织知识的方式。
核心论据:列举了大量 PTI/ETI 边界模糊的案例(Cf 蛋白、EIX 受体、质外体效应蛋白识别等),论证现有二分法的不自洽性在逻辑上不可修补。
影响与局限:Invasion Model 引发了持续至今的术语论争。其贡献在于迫使领域反思分类框架的隐含假设;局限在于作为一个"纯概念"提案,缺乏独立的实验预测来区分自身与竞争框架。
2.7当前争论与未解问题
- 不同 NLR 对 PTI 底盘的依赖是否一致?CNL 型 NLR(如 ZAR1)直接形成膜孔道,可能对 PTI 的依赖较低;TNL 型 NLR(如 RPP1、RPS4)需要通过 EDS1-helper NLR 轴传导信号,可能更依赖 PTI 组分。这一假说尚未被系统验证。
- 协同机制在作物中是否保守?拟南芥的结果能否外推到水稻、小麦、番茄等作物?水稻的 NLR 免疫网络与拟南芥有显著差异(如缺乏典型的 TNL),协同模式可能不同 (Duxbury et al., 2021)。
- 协同的定量程度是否可预测?给定一个 PRR-NLR 的组合,能否预测其协同增效的幅度?还是说协同效应高度依赖于具体的信号网络配置?建立这种预测能力是将协同概念应用于育种的前提。
- 协同失效时,系统最先在哪个节点崩溃?如果我们将免疫网络视为一个工程系统,哪些节点是"单点故障"?RBOHD 的功能缺失似乎对 PTI 和 ETI 的协同效应影响都很大——它是不是一个关键瓶颈?
- PTI/ETI 术语的未来:领域是否会在可预见的将来达成术语共识?还是会维持当前的多元并存状态?历史经验表明,术语变革通常不是由论争决定的,而是由下一代研究者的使用习惯自然演化。
2.8关键实验方法
| 实验方法 | 原理与用途 | 关键参数与注意事项 | 经典文献 |
|---|---|---|---|
| 双通路遗传拆分 | 构建 PRR 和 NLR 信号组分的多重突变体组合,分别或同时激活 PTI/ETI,定量比较单独 vs 协同的免疫输出。是研究 PTI-ETI 关系的核心策略。 | 需要高阶多重突变体(如 fls2 efr cerk1 三重突变);注意遗传冗余可能掩盖效应;统计分析需要检验"超加性"而非仅"显著差异"。 | Ngou et al., 2021, Nature; Yuan et al., 2021, Science |
| 诱导型效应蛋白表达系统 | 将效应蛋白基因置于化学诱导型启动子(如雌二醇/地塞米松诱导型)控制下,在无菌条件下单独激活 ETI,避免 PAMP 的干扰。 | 注意诱导剂本身的潜在生理效应;诱导时间动态可能与自然感染不同;需要验证蛋白表达水平在生理范围内。 | Ngou et al., 2021, Nature |
| ROS / Ca²⁺ / MAPK 并行检测 | 在同一实验中同时或平行测量 ROS 爆发(luminol 法)、胞质 Ca²⁺ 浓度(aequorin 或 GCaMP 探针)和 MAPK 磷酸化(Western blot),获得免疫信号的多维动态图谱。 | 时间分辨率要求不同:Ca²⁺ 为秒级,ROS 为分钟级,MAPK 为分钟至半小时级。需要合适的活体检测探针和多通道检测设备。 | Yuan et al., 2021, Science; Thor & Peiter, 2014, J Exp Bot |
| 信号网络定量分析 | 利用多重信号突变体的表型数据(如细菌增殖),通过组合分析定量评估各信号分支的独立贡献和交互作用。可结合数学建模。 | 需要完整的突变体矩阵(所有单重、双重、三重...组合);表型测量需要高精度和足够重复;统计模型需考虑遗传性状相加和非加性效应。 | Tsuda et al., 2009, PLoS Genet; Tsuda & Katagiri, 2010, Curr Opin Plant Biol |
2.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
2.10参考文献
- Cook DE, Mesarich CH, Thomma BPHJ. Understanding plant immunity as a surveillance system to detect invasion. Annu Rev Phytopathol, 2015, 53: 541–563.
- Cui H, Tsuda K, Parker JE. Effector-triggered immunity: from pathogen perception to robust defense. Annu Rev Plant Biol, 2015, 66: 487–511.
- DeFalco TA, Zipfel C. Molecular mechanisms of early plant pattern-triggered immune signaling. Mol Cell, 2021, 81: 3449–3467.
- Deng Y, Zhai K, Xie Z, et al. Epigenetic regulation of antagonistic receptors confers rice blast resistance with yield balance. Science, 2017, 355: 962–965.
- Duxbury Z, Wu CH, Ding P. A comparative overview of the intracellular guardians of plants and animals. Annu Rev Plant Biol, 2021, 72: 751–783.
- Flor HH. Current status of the gene-for-gene concept. Annu Rev Phytopathol, 1971, 9: 275–296.
- Gómez-Gómez L, Boller T. FLS2: an LRR receptor-like kinase involved in the perception of the bacterial elicitor flagellin in Arabidopsis. Mol Cell, 2000, 5: 1003–1011.
- Jones JDG, Dangl JL. The plant immune system. Nature, 2006, 444: 323–329.
- Lapin D, Bhandari DD, Parker JE. Origins and immunity networking functions of EDS1 family proteins. Annu Rev Phytopathol, 2022, 60: 253–276.
- Lu D, Wu S, Gao X, et al. A receptor-like cytoplasmic kinase, BIK1, associates with a flagellin receptor complex to initiate plant innate immunity. Proc Natl Acad Sci USA, 2010, 107: 496–501.
- Navarro L, Zipfel C, Rowland O, et al. The transcriptional innate immune response to flg22. Interplay and overlap with Avr gene-dependent defense responses and bacterial pathogenesis. Plant Physiol, 2004, 135: 1113–1128.
- Ngou BPM, Ahn HK, Ding P, Jones JDG. Mutual potentiation of plant immunity by cell-surface and intracellular receptors. Nature, 2021, 592: 110–115.
- Ngou BPM, Ding P, Jones JDG. Thirty years of resistance: Zig-zag through the plant immune system. Plant Cell, 2022, 34: 1253–1272.
- Pruitt RN, Gust AA, Nürnberger T. Plant immunity unified. Nat Plants, 2021, 7: 382–383.
- Tao Y, Xie Z, Chen W, et al. Quantitative nature of Arabidopsis responses during compatible and incompatible interactions with the bacterial pathogen Pseudomonas syringae. Plant Cell, 2003, 15: 317–330.
- Thomma BPHJ, Nürnberger T, Joosten MHAJ. Of PAMPs and effectors: the blurred PTI-ETI dichotomy. Plant Cell, 2011, 23: 4–15.
- Thor K, Peiter E. Cytosolic free calcium and plant immune signalling. J Exp Bot, 2014, 65: 5955–5968.
- Toth R, Choi S, Le Naour-Vernet M, et al. Motif-based substrate mapping of the receptor-like cytoplasmic kinase BIK1 reveals novel components and regulatory nodes of plant immunity. Nat Plants, 2026, 12: 465–480. DOI: 10.1038/s41477-025-02218-z.
- Tsuda K, Katagiri F. Comparing signaling mechanisms engaged in pattern-triggered and effector-triggered immunity. Curr Opin Plant Biol, 2010, 13: 459–465.
- Tsuda K, Sato M, Stoddard T, et al. Network properties of robust immunity in plants. PLoS Genet, 2009, 5: e1000772.
- Wang J, Hu M, Wang J, et al. Reconstitution and structure of a plant NLR resistosome conferring immunity. Science, 2019, 364: eaav5870.
- Yuan M, Jiang Z, Bi G, et al. Pattern-recognition receptors are required for NLR-mediated plant immunity. Nature, 2021, 592: 105–109.
- Zhang J, Shao F, Li Y, et al. A Pseudomonas syringae effector inactivates MAPKs to suppress PAMP-induced immunity in plants. Cell Host Microbe, 2007, 1: 175–185.
- Zipfel C. Plant pattern-recognition receptors. Trends Immunol, 2014, 35: 345–351.
- Zipfel C, Kunze G, Chinchilla D, et al. Perception of the bacterial PAMP EF-Tu by the receptor EFR restricts Agrobacterium-mediated transformation. Cell, 2006, 125: 749–760.