非编码 RNA 与免疫调控
超越经典的"基因→蛋白"框架,非编码 RNA 是免疫调控中日益重要的一层
本章目录
- RNA 沉默作为抗病毒免疫的核心机制
- miRNA 在免疫调控中的角色
- lncRNA 与免疫的新关联
- 跨界 RNA 转移(cross-kingdom RNAi)
- 表观遗传学与免疫记忆
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
前面各章描述的免疫信号通路——从 PRR 和 NLR 的识别,到激酶级联和激素网络的信号传递,再到转录因子驱动的基因表达——遵循的是经典的"蛋白质中心"逻辑。但在这个蛋白质构成的信号骨架之下,还潜伏着一个庞大而精密的调控层:非编码 RNA(non-coding RNA, ncRNA)。
这个调控层的重要性最初在抗病毒免疫中被认识——RNA 沉默是植物对抗 RNA 病毒的最核心防线 → 第1章 1.1节。但随着研究的深入,ncRNA 的角色已远远超出了抗病毒:内源 miRNA 通过精确调节免疫受体和信号蛋白的表达水平来微调免疫系统的"灵敏度",lncRNA 通过影响染色质状态参与免疫记忆的建立,而跨界 RNA 转移更将植物-病原的信息战从蛋白质层面扩展到了 RNA 层面。
理解 ncRNA 在免疫中的角色,不仅补全了免疫调控的分子图景,还为开发新一代抗病策略(如 RNAi 介导的抗病和 HIGS)提供了全新的工具箱。本章将从 RNA 沉默的抗病毒核心功能出发,依次展开内源小 RNA、lncRNA 和跨界 RNA 转移的免疫调控逻辑,最后讨论表观遗传学与免疫记忆的 RNA 维度。
13.1RNA 沉默作为抗病毒免疫的核心机制
认知演变
过去:RNA 沉默最初被视为实验室中的基因工具或转座子控制机制,与免疫关系不大。
转折:2000年代初,多项研究证明 RNA 沉默是植物抗病毒免疫的主要机制——几乎所有植物病毒都编码 RNA 沉默抑制子(VSR)这一事实,从反面证明了沉默路径的防御重要性。
现在:RNA 沉默被认为是与 PTI/ETI 平行的第三大免疫层——尤其对 RNA 病毒,它比 NLR 介导的免疫更为普遍和基础。
抗病毒 RNA 沉默的分子机制
当 RNA 病毒在宿主细胞中复制时,其 RNA 依赖的 RNA 聚合酶(RdRP)产生的双链 RNA(dsRNA)复制中间体被宿主 Dicer-like(DCL)蛋白识别并切割为21-24 nt 的小干扰 RNA(virus-derived siRNA, vsiRNA)。这些 vsiRNA 被装载入 Argonaute(AGO)蛋白,形成 RNA 诱导沉默复合体(RISC),通过碱基互补配对靶向降解病毒 RNA (Ding & Voinnet, 2007)。
这个系统的精妙之处在于其自放大特性:宿主的 RDR(RNA-Dependent RNA Polymerase,如 RDR6)以初级 siRNA 引导的切割产物为模板,合成新的 dsRNA,产生"次级 siRNA"——形成正反馈环路,大幅放大沉默信号。更重要的是,沉默信号可以通过胞间连丝在细胞间移动,并通过韧皮部实现全株性传播——为病毒还未到达的远端组织预先建立防御 (Melnyk et al., 2011)。
病毒的反制:RNA 沉默抑制子(VSR)
面对如此强力的沉默防线,病毒的进化回应是"以牙还牙"——几乎所有已知的植物病毒都编码至少一种 VSR。不同病毒的 VSR 在结构上高度多样(暗示独立进化起源),但在功能上趋同——它们靶向沉默通路的不同步骤:
- dsRNA 结合:如番茄丛矮病毒(TBSV)的 P19 形成同源二聚体,以尺寸特异性方式结合21 nt 的 siRNA 双链体,阻止其装载入 AGO (Vargason et al., 2003)。P19 是第一个被解析晶体结构的 VSR,其与 siRNA 的共结晶是理解 VSR 作用机制的里程碑。
- AGO 降解:如豇豆花叶病毒(CMV)的 2b 蛋白直接与 AGO1 互作并抑制其切割活性。
- 甲基化抑制:如马铃薯 Y 病毒(PVY)的 HcPro 干扰 HEN1 对 siRNA 3' 端的甲基化修饰,导致 siRNA 不稳定而降解。
VSR 的存在创造了一种持续的分子军备竞赛——与效应子-NLR 的博弈遥相呼应 → 第7章。值得注意的是,一些 NLR 蛋白已被证明能直接识别 VSR(如烟草的 N 蛋白识别 TMV 的解旋酶/VSR 功能域),将 RNA 沉默防线与 ETI 防线在分子层面连接起来 → 第4章。
图 13.1 抗病毒 RNA 沉默通路与 VSR 靶点。病毒复制产生的 dsRNA 被 DCL 加工为 vsiRNA,随后装载 AGO/RISC 并引导病毒 RNA 降解;病毒 RNA 沉默抑制子可在多个步骤阻断这一防线。
13.2miRNA 在免疫调控中的角色
miRNA 介导的免疫增益控制
与外源 siRNA 不同,miRNA 是植物基因组自身编码的调控分子。MIR 基因转录产生前体 RNA,经 DCL1 加工为成熟 miRNA(通常21 nt),装载入 AGO1 后以碱基互补方式切割或翻译抑制靶标 mRNA。关键在于:多个 miRNA 家族的靶标恰好是免疫信号通路的核心组分——这使得 miRNA 成为免疫系统"增益"(gain)的精密调节器。
最具代表性的免疫相关 miRNA 包括:
- miR393——最早被鉴定的"免疫 miRNA":Navarro et al. (2006) 在 Science 上报道,flg22 处理诱导 miR393 的积累,miR393 靶向降解生长素受体 TIR1/AFB 的 mRNA。由于生长素信号促进易感性(生长素促进细菌毒力基因表达),miR393 通过抑制生长素信号来间接增强免疫——这是第一个将 miRNA 与植物免疫直接连接的发现,也是生长素-免疫拮抗的重要分子机制 → 第5章 5.4节。
- miR482/miR2118——NLR 表达的"刹车":这两个 miRNA 家族靶向多种 NLR 基因的 mRNA,在非胁迫条件下维持 NLR 的低水平表达。当病原入侵触发免疫后,miR482/2118 的表达被下调,从而"释放"NLR 的表达上限——实现NLR 库的动态调控 (Shivaprasad et al., 2012; Zhai et al., 2011)。这种设计逻辑精妙而合理:NLR 的组成性高表达会导致自身免疫代价 → 第11章,miRNA 提供了一种低成本的"按需激活"机制。
- miR160/miR167——生长素响应因子的调控:这两个 miRNA 家族靶向 ARF(Auxin Response Factor)家族成员,通过调节生长素信号通路间接影响免疫-生长平衡。
- miR472——NLR 的精确制导:在拟南芥中,miR472 靶向 CC-NLR 亚家族的多个成员,参与 RDR6 依赖的次级 siRNA(phasiRNA)产生,形成"miRNA-phasiRNA"级联,对 NLR 转录本进行分层调控 (Boccara et al., 2014)。
miRNA 调控的系统逻辑
从系统生物学的角度看,miRNA 对免疫的调控不是简单的"开关",而是一种网络级的"增益控制"(gain control):
- 基线设定:在非胁迫条件下,免疫相关 miRNA 维持靶标基因的低表达水平,避免不必要的免疫激活和生长代价。
- 快速解除抑制:病原信号(如 PAMP 识别)触发特定 miRNA 的下调,释放靶标基因的表达——这种"去抑制"比从头转录更快,能在分钟至小时级别改变蛋白质组。
- 时序精度:不同 miRNA 对病原信号的响应时序不同,使得免疫通路的各个节点按照特定的时间序列被依次"解锁"——先激活早期识别组分,再释放下游效应模块。
- 恢复抑制:病原被清除后,miRNA 表达恢复,重新建立靶标基因的低表达基线——完成免疫应答的"关闭"。
这种设计的核心优势在于可逆性和低代价——与表观遗传修饰或蛋白质降解相比,miRNA 介导的 mRNA 切割提供了一种快速、可逆、且能量消耗较低的调控方式。这可能解释了为什么进化选择了 miRNA 而非转录因子来承担免疫系统"增益旋钮"的角色——当需要频繁的上下调节时,miRNA 通路的效率优势尤为明显。
13.3lncRNA 与免疫的新关联
长链非编码 RNA(lncRNA,>200 nt)是一个庞大但功能大部分未知的 RNA 类别。在动物免疫学中,lncRNA 的角色已被广泛研究(如 NEAT1、MALAT1 等),但在植物免疫中,这一领域仍处于早期阶段。
已知的免疫相关 lncRNA
尽管功能验证的案例有限,已有若干 lncRNA 被证明参与植物免疫调控:
- ELENA1(ELF18-INDUCED LONG-NONCODING RNA 1):这是拟南芥中研究最深入的免疫 lncRNA。ELENA1 被 elf18(EF-Tu 受体 EFR 的配体)诱导,与 MED19a(Mediator 复合体亚基)互作,增强 PR1 等防御基因的转录。elena1 敲除突变体对 Pst DC3000 更敏感 (Seo et al., 2017)。
- ALEX1:在水稻中鉴定的一个 lncRNA,参与 JA 信号通路的调节,影响对稻瘟菌的抗性 (Yu et al., 2020)。
- 天然反义转录本(NAT):多个免疫相关基因座被发现有反义 lncRNA 的转录。这些 NAT 可以通过 RNA-RNA 互作调节正义链的稳定性或翻译效率,为免疫基因的表达增加了一层精细调控。
lncRNA 与免疫记忆
lncRNA 在免疫中可能最重要的角色不是急性防御反应,而是免疫记忆的建立和维持。多条线索将 lncRNA 与 priming 和跨代免疫联系起来:
- lncRNA 可以作为"导引"将染色质修饰复合体(如 PRC2 或 COMPASS)引导到特定基因组位点,建立特异性的组蛋白修饰标记。在免疫 priming 中,防御基因启动子区域的 H3K4me3 修饰被增强但基因不被完全激活——lncRNA 可能参与这种"预设"标记的建立 → 第11章。
- 在拟南芥中,SA 处理后某些基因座的 lncRNA 表达与 DNA 甲基化变化相关联——暗示 lncRNA 可能参与 RNA 指导的 DNA 甲基化(RdDM)通路与免疫信号的交叉 (Huang et al., 2021)。
然而,必须坦率承认:目前 lncRNA 在植物免疫中的因果性证据仍然薄弱。大多数研究停留在"转录组中鉴定到差异表达的 lncRNA"的相关性层面,缺乏系统的功能验证。将 lncRNA 从"相关因子"提升为"因果调控者",需要结合基因编辑(CRISPR 敲除/敲入 lncRNA 基因座)、结构域缺失分析和蛋白质互作组学等多种手段——这是当前研究的主要瓶颈。
13.4跨界 RNA 转移(cross-kingdom RNAi)
如果说 miRNA 和 lncRNA 代表了免疫调控的"内部事务",那么跨界 RNA 转移(cross-kingdom RNAi)则将 RNA 的角色扩展到了植物-病原之间的"信息战"。
病原→宿主方向:RNA 劫持
2013年,Weiberg et al. 在 Science 上发表了一项改变认知的发现:灰霉菌 Botrytis cinerea 产生的小 RNA(Bc-siRNA)可以进入拟南芥和番茄细胞,劫持宿主的 AGO1,靶向沉默宿主的免疫基因(包括 MAPK 通路的成员)。这一发现意味着:
- 病原的"武器库"不仅包括效应蛋白,还包括小 RNA——后者可以精准、低成本地压制宿主防御。
- 宿主的 RNA 沉默机器(特别是 AGO 蛋白)既是防御工具,也可能成为被病原利用的"后门"。
Wang et al. (2017) 进一步鉴定了一个具体的 B. cinerea 小 RNA——Bc-siR37,它靶向拟南芥的 WRKY7、PMR6 和 FEI2 等多个防御基因。在 ago1 突变体中,Bc-siR37 的免疫抑制效应消失,证实了 AGO1 在跨界沉默中的必要角色。
宿主→病原方向:RNA 反击
如果病原能用小 RNA 攻击宿主,植物是否也能"以其人之道还治其人之身"?2016年和2018年的两项关键研究给出了肯定答案:
- Zhang et al. (2016):发现棉花产生的 miRNA(miR166 和 miR159)可以被转运到寄生的 Verticillium dahliae 真菌中,靶向沉默其毒力相关基因(如 Ca²⁺ 依赖的 cysteine protease 基因 Clp-1),降低病原的致病力。
- Cai et al. (2018):更进一步揭示了传递机制——拟南芥通过分泌胞外囊泡(extracellular vesicles, EVs)将含有 siRNA 的货物运送到 B. cinerea 感染位点。这些囊泡富含 TET8(一种四跨膜蛋白)和多种靶向 B. cinerea 毒力基因的 siRNA。tet8 突变体的囊泡分泌减少,对 B. cinerea 也更敏感。
这些发现开辟了一个全新的应用方向:宿主诱导基因沉默(Host-Induced Gene Silencing, HIGS)——在转基因植物中表达靶向病原关键基因的 dsRNA/miRNA,使植物成为持续的 RNA "武器工厂"。HIGS 已在多种病理系统中展示了原理验证,包括抗真菌、抗卵菌和抗线虫 → 第14章。
2025–2026 年的研究把 RNA 防御从“病原-宿主”扩展到“宿主-微生物组-病原”的三方系统。Liu et al. (2025) 发现有机肥可促进番茄根系分泌 miR159 和 miR319c-3p 等 miRNA,这些 RNA 信号既有助于扩增有益根际微生物,又抑制 Ralstonia solanacearum 的增殖。Ni et al. (2026) 则在水稻中揭示一个 ceRNA 模块可削弱 Rhizoctonia solani 诱导的跨界 RNAi,从而降低纹枯病菌致病性。也就是说,RNA 不只是“沉默工具”,还可能是宿主管理微生物组与反制病原 RNA 攻击的调节货币。
图 13.2 跨界 RNA 转移的双向机制。病原小 RNA 可以进入植物细胞并劫持宿主 AGO,植物也可通过胞外囊泡、根系分泌 miRNA 或 ceRNA 模块反制病原 RNA 攻击,并可能重塑有益根际微生物。
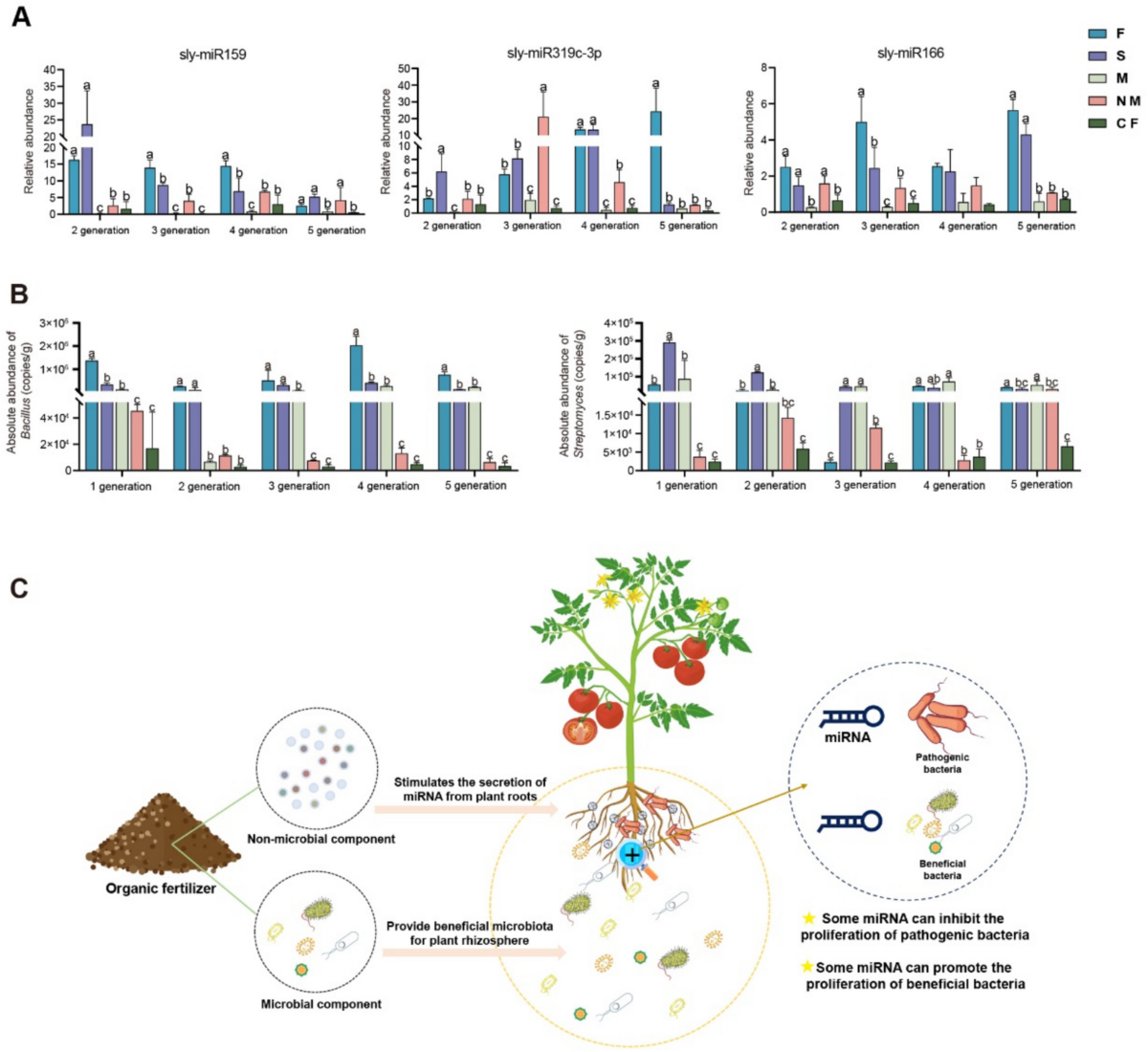
图 13.3 论文原图:根系 miRNA 连接有机肥、根际微生物与青枯病抑制。原图为 Liu et al. (2025) Microbiome Fig. 7,DOI: 10.1186/s40168-025-02137-3。依据 CC BY-NC-ND 4.0 原样复用;图片未作裁剪、改色或内容改动。
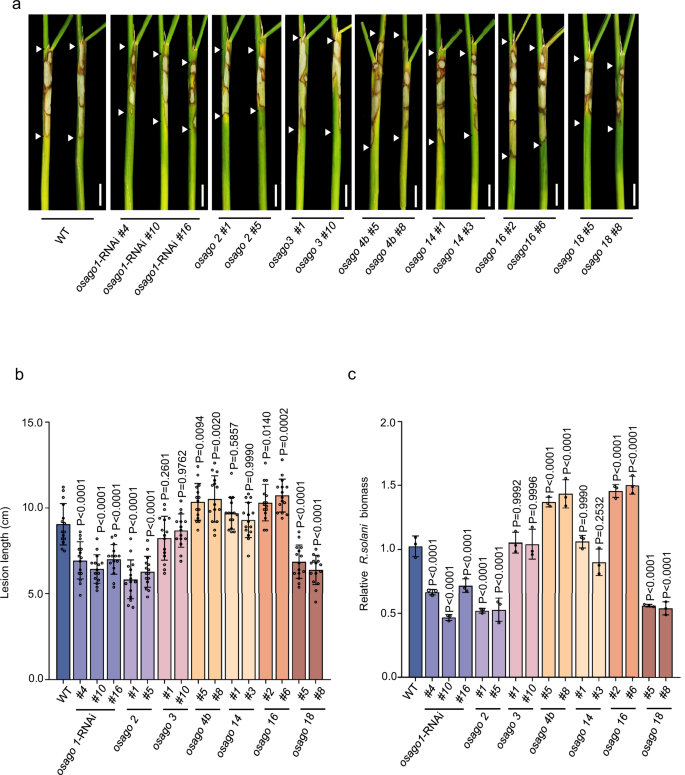
图 13.4 论文原图:跨界 RNAi 相关 AGO 节点的遗传证据。原图为 Ni et al. (2026) Nature Communications Fig. 1,DOI: 10.1038/s41467-026-72158-5。依据 CC BY-NC-ND 4.0 原样复用;图片未作裁剪、改色或内容改动。
13.5表观遗传学与免疫记忆
ncRNA 与免疫的交叉不止于急性调控——RNA 指导的表观遗传修饰可能是免疫记忆(priming)的分子基础之一。
RNA 指导的 DNA 甲基化(RdDM)与免疫
植物特有的 RdDM 通路通过24 nt siRNA-AGO4 复合体引导 DRM2 甲基转移酶到特定基因组位点进行 DNA 甲基化。越来越多的证据表明,RdDM 通路与免疫存在交叉:
- 转座子去抑制与防御基因激活:SA 信号和病原侵染可以局部降低某些转座子和重复序列的 DNA 甲基化水平。由于许多防御基因(尤其是 NLR 基因)位于富含转座子的基因组区域,转座子的去甲基化可能通过"顺式"效应增强邻近防御基因的表达 (Dowen et al., 2012)。
- 跨代免疫记忆:某些表观遗传变化(包括 DNA 甲基化和组蛋白修饰的改变)可以在有限的代际间传递。Luna et al. (2012) 报道,拟南芥经 Pst DC3000 处理后,其子代在没有再次接触病原的情况下表现出增强的 SA 依赖性防御——这种跨代效应与特定基因组位点的 DNA 甲基化变化相关。
组蛋白修饰与免疫 priming
免疫 priming 的表观遗传基础不限于 DNA 甲基化。Jaskiewicz et al. (2011) 发现,经 SA 或病原处理的拟南芥在防御基因启动子区域出现持久的 H3K4me3(激活标记)和 H3 乙酰化增加,即使在 SA 水平恢复正常后这些标记仍然存在。这种"表观遗传疤痕"可能解释了 priming 的分子基础:防御基因虽然未被完全激活,但其染色质状态已经被"预设"为更容易被再次激活的状态 → 第11章。
染色质重塑复合物:免疫转录重编程的"门禁系统"
除了组蛋白修饰酶,ATP 依赖的染色质重塑复合物(chromatin remodeling complexes)在免疫中扮演着关键的"门禁"角色——它们通过移动、移除或重组核小体来改变特定基因组区域的可及性,决定哪些基因可以被转录因子结合:
- SWI/SNF 复合物:拟南芥 SWI/SNF 家族成员 SYD 和 BRM 是免疫的负调控因子——syd 和 brm 突变体表现出增强的抗病性,部分原因是在这些突变体中,PR1 等防御基因的启动子区域核小体占有率降低、染色质更开放,导致基础防御水平升高 (Walley et al., 2008)。SWI/SNF 复合物还参与 SA 介导的转录重编程,调控从生长程序到防御程序的"开关"——在无病原时维持生长相关基因的开放构象,在病原感知后将 SWI/SNF 活性转向防御基因座的开放。
- INO80 复合物:INO80 染色质重塑复合物在 DNA 损伤修复和转录调控中起作用,有证据表明其也参与防御基因的转录调控。INO80 的突变影响 SA 响应基因的表达水平。
- CHR5 和 CHR11/17:这些 ISWI 家族的染色质重塑因子参与核小体间距的调节,影响转录因子对免疫基因启动子的访问效率。
免疫记忆的跨代传递:超越遗传的防御遗产
植物免疫最令人着迷但也最具争议的现象之一是跨代免疫记忆(transgenerational immune memory)——亲代经历的病原攻击,是否能让未经历的子代获得增强的抗性?
- Luna et al. (2012) 报道拟南芥经 Pst DC3000 处理后,子代在没有再次接触病原的情况下表现出增强的 SA 依赖性防御——这种增强与特定的 DNA 甲基化变化相关,且在二代后减弱。
- Slaughter et al. (2012) 在拟南芥中展示了类似的跨代 priming 效应,但发现效应的稳定性依赖于子代的环境条件——在胁迫环境中跨代记忆更稳定,在无胁迫环境中迅速衰减。这暗示跨代表观遗传是环境依赖的,而非硬编码的"遗传"。
- Holeski et al. (2012) 在 Mimulus guttatus(猴面花)中展示了跨代 herbivory 防御 priming,说明这一现象并非拟南芥特有。
然而,必须强调:跨代免疫记忆的因果证据链仍然脆弱。主要挑战包括:(1)很难排除种子储存的代谢物或微生物组的影响(而非真正的表观遗传传递);(2)DNA 甲基化变化在每代都被大规模重置(通过 RdDM 和 DEMETER 介导的去甲基化),表观等位基因(epiallele)的稳定传递机制基本未知;(3)效应量通常很小——子代的抗性增强幅度远小于亲代本身的 priming 效应。这些问题使"跨代免疫记忆是否是进化上被选择的适应"这一问题仍然悬而未决。
ncRNA 在这个过程中扮演什么角色?一种可能的模型是:免疫信号诱导特定的 lncRNA 或 siRNA 产生 → 这些 ncRNA 引导染色质修饰酶到防御基因座 → 建立持久的表观遗传标记 → 后续的免疫刺激可以更快速地在这些"预标记"的位点启动全面的转录激活。这一模型的各个环节已有间接证据支持,但完整的因果链条尚未在任何单一系统中被验证。
ncRNA 介导的免疫调控是进化的"锦上添花"还是"不可或缺"?
一个根本性的问题是:如果去除所有已知的免疫相关 miRNA 和 lncRNA,植物的免疫系统是否会崩溃?还是仅仅变得"不那么精确"?目前的证据倾向于后者——单个 miRNA 突变体的免疫表型通常是定量的(抗性降低30-50%)而非定性的(完全丧失抗性)。但 miRNA 家族之间可能存在大量的功能冗余,需要多基因突变体才能揭示全局效应。如果 ncRNA 主要承担"微调"功能而非"开关"功能,那么它们的进化优势在于:以极低的成本(几百个碱基的 RNA,无需翻译为蛋白质)实现对复杂网络的精密调节——这是蛋白质调控因子难以匹敌的效率。
13.6里程碑研究思路拆解
里程碑 1:Navarro et al. (2006) — 第一个免疫 miRNA 的鉴定
面对的问题:miRNA 是否参与 PTI 信号的调控?
关键思路:用 flg22 处理拟南芥后进行 small RNA 组学分析,鉴定差异表达的 miRNA,并追踪其靶标基因的生物学功能。
关键证据链:(1)flg22 处理诱导 miR393 积累;(2)miR393 的靶标是生长素受体 TIR1/AFB;(3)miR393 过表达增强对 Pst DC3000 的抗性;(4)外源生长素处理增加细菌易感性。
影响:首次建立 miRNA-免疫的因果连接,揭示了生长素-免疫拮抗的分子机制。同时为后续大量免疫 miRNA 的鉴定开辟了方法学范式。
里程碑 2:Weiberg et al. (2013) — 真菌小 RNA 劫持宿主沉默机器
面对的问题:病原是否可以通过小 RNA 实现跨界的基因沉默来压制宿主免疫?
关键思路:对 B. cinerea 感染的拟南芥和番茄进行小 RNA 测序,区分宿主来源和病原来源的小 RNA,然后通过 AGO 免疫沉淀(AGO-IP)确认病原小 RNA 是否被宿主 AGO 蛋白装载。
关键证据链:(1)B. cinerea 小 RNA 在宿主组织中大量积累;(2)Bc-siRNA 与宿主 AGO1 物理互作(AGO1-IP-seq);(3)Bc-siRNA 的靶标预测并实验验证命中宿主 MAPK 基因;(4)在 ago1 突变体中,Bc-siRNA 的免疫抑制效应消失。
影响:开创性地证明病原可以利用小 RNA 作为"跨界效应子",将植物-病原互作的信息战从蛋白质层面扩展到 RNA 层面。
里程碑 3:Cai et al. (2018) — 植物胞外囊泡输出小 RNA 反击病原
面对的问题:植物是否可主动用 RNA 跨界压制病原?如果可以,传递介质是什么?
关键思路:从拟南芥感染位点的质外体液中分离胞外囊泡,分析其 RNA 货物和蛋白质组成,通过荧光标记追踪囊泡的跨界转运。
关键证据链:(1)拟南芥在 B. cinerea 感染位点分泌富含 TET8 蛋白的胞外囊泡;(2)囊泡中含有靶向 B. cinerea 毒力基因的 siRNA;(3)荧光标记的囊泡可被 B. cinerea 菌丝吸收;(4)tet8 突变体的囊泡分泌减少且对 B. cinerea 更敏感;(5)植物来源小 RNA 进入病原后可降低靶基因表达和毒力。
影响:不仅证明了跨界 RNA 传递的双向性,还鉴定了传递介质(胞外囊泡),为 HIGS 和 SIGS(Spray-Induced Gene Silencing,喷雾诱导基因沉默)等应用策略提供了机制基础。
13.7当前争论与未解问题
- 跨界 RNA 传递的效率由哪些因素决定?在自然感染条件下,有多少小 RNA 能成功跨越细胞壁-质膜双重屏障被病原吸收?传递效率是否足以在田间条件下产生有意义的保护效果?胞外囊泡的稳定性和靶向性如何?
- 田间环境中 RNA 防御如何保持稳定?dsRNA 在土壤和叶表环境中容易被核酸酶降解。SIGS 策略(直接喷洒 dsRNA)的田间持效期通常只有数天——如何延长 RNA 的环境稳定性?纳米载体或细菌表达系统是否能解决这一问题?
- lncRNA 在免疫记忆中的因果证据还缺什么?目前大多数 lncRNA-免疫关联是相关性的。需要:(1)CRISPR 精确删除 lncRNA 基因座(而不影响邻近基因)的突变体;(2)lncRNA 域缺失/嵌合体实验区分 RNA 序列功能和转录行为功能;(3)lncRNA-蛋白质互作组学确认具体的效应分子。
- 如何构建低脱靶 RNA 抗病工程体系?HIGS 和 SIGS 的一个核心安全关切是脱靶效应——设计的 dsRNA 是否会意外沉默宿主或非靶标微生物的基因?如何在设计阶段进行全面的脱靶预测?
- ncRNA 调控是否在作物中保守?大多数机制发现来自拟南芥。miR393-生长素受体轴在作物中是否以相同方式运作?跨界 RNA 转移在不同病理系统中的普遍性和效率是否一致?
13.8关键实验方法
| 实验方法 | 用途 | 经典文献 |
|---|---|---|
| small RNA-seq + AGO-IP | 鉴定与特定 AGO 蛋白结合的功能性小 RNA,区分宿主和病原来源 | Weiberg et al., 2013, Science |
| 胞外囊泡分离与示踪 | 纯化植物分泌的胞外囊泡,分析其 RNA 货物,荧光标记追踪跨界转运 | Cai et al., 2018, Science |
| 靶基因报告系统(5'RACE/GFP sensor) | 验证特定 miRNA/siRNA 对靶标 mRNA 的切割,确认沉默因果关系 | Zhang et al., 2016, Nat Plants |
| CRISPR 敲除 ncRNA 基因座 | 建立 lncRNA/miRNA 与免疫表型的因果关系 | Seo et al., 2017, Plant Cell |
| ChIP-seq 与 ATAC-seq | 解析免疫相关基因座的组蛋白修饰和染色质可及性变化 | Jaskiewicz et al., 2011, Plant Cell |
13.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
13.10参考文献
- Boccara M, Sarazin A, Thiébeauld O, et al. The Arabidopsis miR472-RDR6 silencing pathway modulates PAMP- and effector-triggered immunity through the post-transcriptional control of disease resistance genes. PLoS Pathog, 2014, 10: e1003883.
- Borges F, Martienssen RA. The expanding world of small RNAs in plants. Nat Rev Mol Cell Biol, 2015, 16: 727–741.
- Cai Q, Qiao L, Wang M, et al. Plants send small RNAs in extracellular vesicles to fungal pathogen to silence virulence genes. Science, 2018, 360: 1126–1129.
- Ding SW, Voinnet O. Antiviral immunity directed by small RNAs. Cell, 2007, 130: 209–222.
- Dowen RH, Pelizzola M, Schmitz RJ, et al. Widespread dynamic DNA methylation in response to biotic stress. Proc Natl Acad Sci USA, 2012, 109: E2183–E2191.
- Holeski LM, Jander G, Agrawal AA. Transgenerational defense induction and epigenetic inheritance in plants. Trends Ecol Evol, 2012, 27: 618–626.
- Huang CY, Wang H, Hu P, et al. Long noncoding RNAs and their roles in plant immune responses. Plant Commun, 2021, 2: 100228.
- Jaskiewicz M, Conrath U, Peterhänsel C. Chromatin modification acts as a memory for systemic acquired resistance in the plant stress response. EMBO Rep, 2011, 12: 50–55.
- Liu S, Li HY, Zhang T, et al. Organic fertilizer enhances the secretion of microRNAs from tomato roots to facilitate beneficial rhizosphere microorganism expansion and suppress Ralstonia solanacearum proliferation. Microbiome, 2025, 13: 159. DOI: 10.1186/s40168-025-02137-3.
- Luna E, Bruce TJA, Roberts MR, et al. Next-generation systemic acquired resistance. Plant Physiol, 2012, 158: 844–853.
- Melnyk CW, Molnar A, Baulcombe DC. Intercellular and systemic movement of RNA silencing signals. EMBO J, 2011, 30: 3553–3563.
- Navarro L, Dunoyer P, Jay F, et al. A plant miRNA contributes to antibacterial resistance by repressing auxin signaling. Science, 2006, 312: 436–439.
- Ni J, Mao W, Shi T, et al. A rice ceRNA module suppresses Rhizoctonia solani-induced cross-kingdom RNAi to reduce fungal pathogenicity. Nat Commun, 2026. DOI: 10.1038/s41467-026-72158-5.
- Seo JS, Sun HX, Park BS, et al. ELF18-INDUCED LONG-NONCODING RNA associates with Mediator to enhance expression of innate immune response genes in Arabidopsis. Plant Cell, 2017, 29: 1024–1038.
- Shivaprasad PV, Chen HM, Patel K, et al. A microRNA superfamily regulates nucleotide binding site–leucine-rich repeats and other mRNAs. Plant Cell, 2012, 24: 859–874.
- Slaughter A, Daniel X, Flors V, et al. Descendants of primed Arabidopsis plants exhibit resistance to biotic stress. Plant Physiol, 2012, 158: 835–843.
- Vargason JM, Szittya G, Burgyán J, Hall TMT. Size selective recognition of siRNA by an RNA silencing suppressor. Cell, 2003, 115: 799–811.
- Walley JW, Rowe HC, Xiao Y, et al. The chromatin remodeler SPLAYED regulates specific stress signaling pathways. PLoS Pathog, 2008, 4: e1000237.
- Wang M, Weiberg A, Dellota E Jr, Yamane D, Jin H. Botrytis small RNA Bc-siR37 suppresses plant defense genes by cross-kingdom RNAi. Nat Plants, 2017, 3: 16231.
- Weiberg A, Wang M, Lin FM, et al. Fungal small RNAs suppress plant immunity by hijacking host RNA interference pathways. Science, 2013, 342: 118–123.
- Yu Y, Zhou YF, Feng YZ, et al. Transcriptional landscape of pathogen-responsive lncRNAs in rice unveils the role of ALEX1 in jasmonate pathway and disease resistance. Plant Biotechnol J, 2020, 18: 679–690.
- Zhai J, Jeong DH, De Paoli E, et al. MicroRNAs as master regulators of the plant NB-LRR defense gene family via the production of phased, trans-acting siRNAs. Genes Dev, 2011, 25: 2540–2553.
- Zhang T, Zhao YL, Zhao JH, et al. Cotton plants export microRNAs to inhibit virulence gene expression in a fungal pathogen. Nat Plants, 2016, 2: 16153.