环境因子与免疫
免疫不发生在真空中。温度、湿度、光照、土壤条件时刻调控着免疫的效率
本章目录
- 温度与免疫:从 Autoimmunity 到 TIR-NLR 热敏性
- 光信号、湿度与免疫的交叉调控
- 水分胁迫、盐胁迫与多重胁迫组合效应
- 土壤理化性质对免疫的间接影响
- 气候变化背景下的植物免疫新挑战
- 里程碑研究思路拆解
- 当前争论与未解问题
- 关键实验方法
- 推荐阅读
实验室中的免疫反应发生在恒温恒湿、人工光照的生长箱中。但田间的植物每天经历温度波动、光照变化、干旱威胁和养分变动——每一个环境变量都在调节免疫系统的输出。一个在22°C下表现出强烈 ETI 的拟南芥基因型,在28°C下可能完全丧失抗性。这不是实验的"噪声",而是环境对免疫网络的直接干预。
理解环境因子如何进入免疫网络并改变其行为,对于将实验室发现转化为田间策略至关重要——因为在气候变化的大背景下,我们需要的不仅是"能抗病的品种",而是"在多变环境下仍能稳定抗病的品种"。
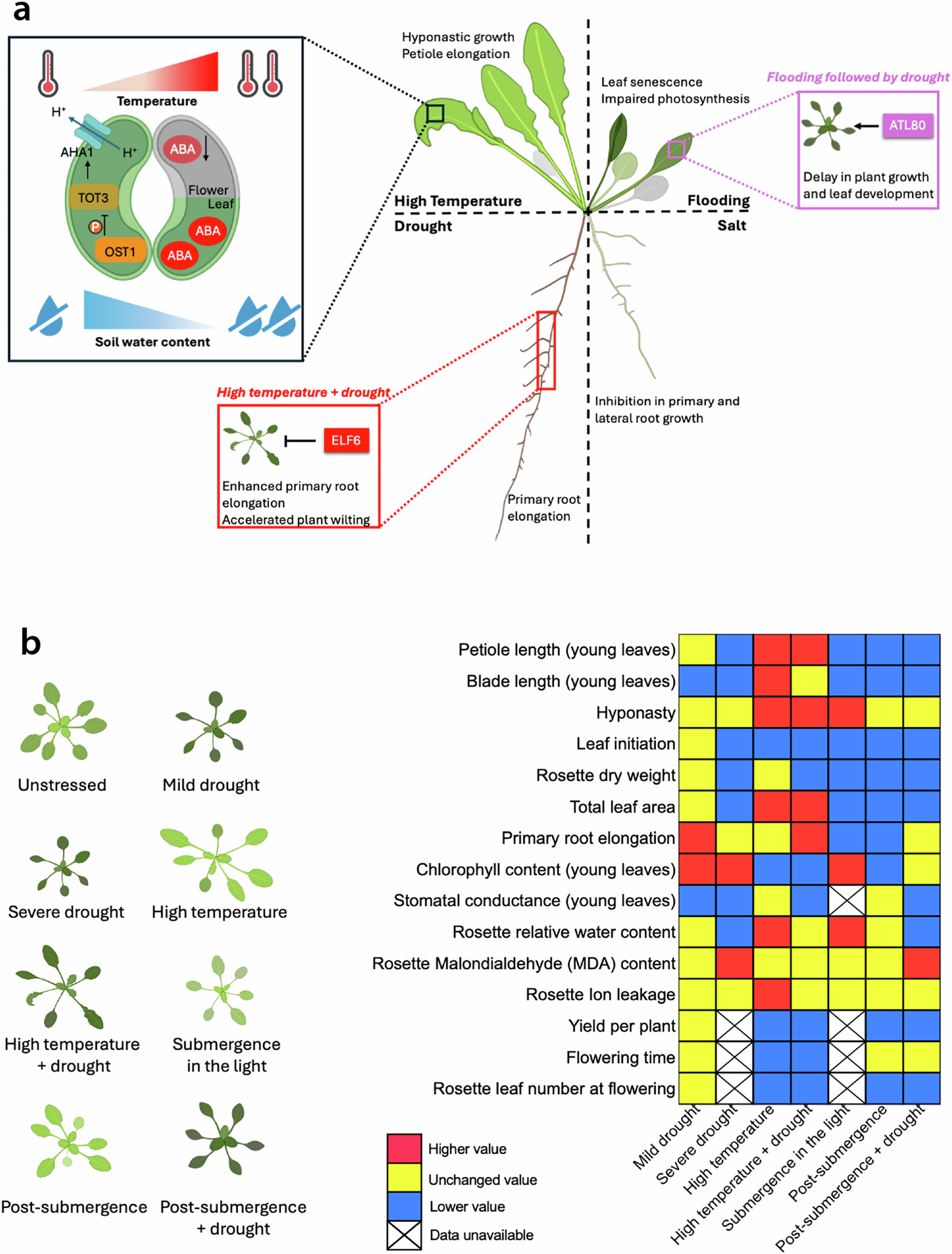
图 12.P1 论文原图:多重非生物胁迫响应的整合框架。原图为 Jiang et al. (2025) Communications Biology Fig. 1,DOI: 10.1038/s42003-025-08077-w。该图为温度、干旱、盐分和光等环境变量如何共同塑造植物状态提供了最新综述框架,可作为本章环境门控免疫的背景图。依据 CC BY 4.0 原样复用;图片未作裁剪、改色或内容改动。
12.1温度与免疫:从 Autoimmunity 到温度敏感 NLR
高温抑制免疫:普遍现象与分子机制
高温(≥28°C vs 标准的22°C)抑制植物免疫是一个广泛记录的现象。在拟南芥中,28°C条件下:
- SA 积累和 PR 基因表达均显著降低 (Huot et al., 2017)。
- 多种 NLR 介导的 ETI 反应减弱或完全丧失——包括 SNC1、RPP4 和 RPS4 等 (Yang & Hua, 2004; Wang et al., 2009)。
- PTI 的某些输出(如 flg22 诱导的 ROS 爆发)在高温下也减弱。
- 同时,病原(如P. syringae)的毒力在28°C下增强(T3SS 表达上调),形成了宿主防御削弱 + 病原攻击增强的”双重打击” (Velásquez et al., 2018)。
高温抑制免疫的分子机制涉及多个层面:
- NLR 稳定性降低:许多 NLR 蛋白的自抑制构象对温度敏感。高温下 NLR 可能部分展开,被蛋白质控体系识别并降解——这既减少了有效的 NLR 蛋白水平,也可能解释为什么某些自身免疫突变体(如 snc1)在高温下”自愈”(因为过度激活的 NLR 被温度依赖性降解)(Zhu et al., 2010)。
- CBP60g/SARD1 的温度响应:SA 合成的关键转录因子 CBP60g 和 SARD1 的转录水平在高温下受到抑制,直接降低了 ICS1 表达和 SA 产量。
- 热激蛋白(HSP)与免疫的竞争:高温诱导大量 HSP 的表达以维持蛋白质稳态,这可能与免疫蛋白的合成竞争翻译资源和分子伴侣 (Sugio et al., 2009)。
低温与 NLR 自激活
与高温相反,低温(≤16°C)可以增强某些 NLR 的活性,甚至导致自身免疫。拟南芥中多种杂种坏死表型是温度依赖的——在低温下表现严重,在高温下缓解 → 第6章 6.4节。这可能因为低温稳定了 NLR 的激活态构象或减缓了负调控蛋白的周转 (Bomblies et al., 2007)。
TIR-NLR 的温度敏感性:2022 年的机制突破
2022 年,Kim et al. 在 Nature 上报道了一个关键发现:TIR 结构域 NLR(TNL)的温度敏感性可能源于其 NADase 活性的热不稳定性。TNL 的 TIR 结构域在激活后切割 NAD⁺,产生次级信使分子(如 pRib-AMP 和 pRib-ADP),这些分子进一步激活 EDS1-PAD4 和 EDS1-SAG101 复合体,最终触发 HR → 第4章 4.4节。Kim 等发现:在 28°C 下,TNL 的 TIR 结构域 NADase 活性显著降低——不是蛋白降解了,而是酶活性本身被高温抑制。更有趣的是,CNL(CC-NLR,如 ZAR1)在相同温度范围内不受影响——因为 CNL 不依赖 NADase 活性,而是通过 CC 结构域形成钙通道。
这一发现具有深远的进化含义:TNL 可能是为温带气候"优化"的 NLR 类型,而 CNL 对温度的耐受范围更宽。全球变暖背景下,依赖 TNL 型 NLR 的抗病策略可能比依赖 CNL 的策略面临更大的失效风险——这对育种中的 NLR 类型选择有直接启示。这也部分解释了为什么热带作物(如水稻、木薯)的 NLR 库中 CNL 比例更高,而温带植物(如拟南芥、芸薹属)的 TNL 更为丰富。
12.2光信号、湿度与免疫的交叉调控
光受体直接参与免疫调控
植物的光感知系统不仅调控生长和发育,也直接影响免疫反应。多种光受体已被证明参与免疫调控:
- 光敏色素(Phytochrome):红光/远红光受体 phyB 正调控 SA 通路和 JA 通路。在荫蔽条件下(低红光/远红光比值,phyB 失活),植物的免疫能力下降——“荫蔽逃避综合征”(Shade Avoidance Syndrome)优先将资源分配给茎的伸长生长,牺牲免疫投入 (de Wit et al., 2013; Campos et al., 2016)。
- 隐花色素(Cryptochrome):蓝光受体 CRY 调控 JA 信号通路,影响植物对昆虫和坏死营养型病原的防御。
- 叶绿体信号(Retrograde signaling):叶绿体是 ROS 产生的主要位点之一。强光诱导的叶绿体 ROS 爆发可以通过逆行信号激活核基因的防御表达——将光胁迫信号与免疫信号耦合 (Mühlenbock et al., 2008)。
昼夜节律:免疫的”时间表”
植物的免疫能力不是全天均一的,而是受昼夜节律的系统性调控。Wang et al. (2011) 的工作表明,拟南芥的抗病能力在清晨达到最高——这恰好是许多叶部细菌侵染的高风险时段(叶面露水未干,气孔刚开放)。
节律调控免疫的分子机制涉及核心时钟组分 CCA1(Circadian Clock Associated 1)。CCA1 直接结合多种防御基因的启动子,根据时间节律调节其表达。cca1 突变体不仅丧失了免疫的节律性,整体抗性水平也降低——暗示节律不仅是免疫的”时间标签”,也是免疫效率的增强因子(通过在高风险时段预先提升防御) (Wang et al., 2011)。
这种”预测式防御”(anticipatory defense)是一种精巧的代价控制策略:不是全天24小时维持高水平防御,而是在高风险时段集中资源 → 第11章。
湿度:被低估的免疫调节因子
湿度对植物免疫的影响长期以来被低估——部分原因是实验室研究通常在可控湿度下进行,且高湿度常被简单地等同于”有利于病原”。但近年的研究揭示了湿度-免疫之间更为精妙的分子连接:
- 高湿度增强 PTI 输出:在高相对湿度(>90% RH)条件下,拟南芥的 flg22 诱导 ROS 爆发和防御基因表达均增强——部分原因是高湿度下气孔持续开放,增加了 PRR 与 PAMP 的接触概率 (Zhou et al., 2014)。这一效应与直觉相反:我们通常认为高湿度有利于病害(确实有利于某些真菌病原的孢子萌发),但对细菌的 PTI 层防御而言,高湿度反而增强了第一线识别。
- 湿度感应与 ABA 信号的交叉:植物的湿度感知涉及多个信号通路,其中 ABA 信号是核心枢纽。在低湿度(干旱)条件下,ABA 大量积累并促进气孔关闭;在高湿度条件下,ABA 水平降低,气孔开放。由于 ABA 与 SA 信号存在拮抗关系 → 第5章 5.4节,湿度通过 ABA 间接调节 SA 依赖性防御的强度——高湿度 → 低 ABA → SA 防御增强;低湿度 → 高 ABA → SA 防御受抑但气孔防御增强。这种”湿度-ABA-SA”三角关系解释了为什么不同湿度条件下植物对不同类型病原(细菌 vs 真菌)的相对抗性可能完全不同。
- 叶际水滴的免疫生态学:叶片表面的自由水(露水、雨水)不仅为病原提供侵入通道,也改变了叶际微生物组的化学微环境。液滴中溶解的植物表面代谢物和 MAMP 可以在局部形成高浓度的”免疫诱导微区”,触发局部防御 priming (Xin et al., 2016)。
12.3水分胁迫、盐胁迫与免疫的交汇
干旱与免疫的拮抗
干旱胁迫与免疫之间的关系主要通过 ABA 信号通路介导。干旱诱导 ABA 大量积累以促进气孔关闭(减少水分散失),但高水平 ABA 同时抑制 SA 合成和信号 → 第5章 5.4节。这意味着干旱胁迫下的植物对活体营养型病原更加易感——一个具有重要农业意义的发现 (Mohr & Cahill, 2007)。
然而,ABA 介导的气孔关闭在免疫早期阶段是保护性的——关闭的气孔阻止了细菌进入。因此 ABA-免疫的关系高度时间依赖:在感染最初几小时(气孔防御阶段),ABA 有利于抗性;但在持续感染阶段(需要 SA 驱动的全面防御),ABA 不利于抗性。
盐胁迫与免疫
盐胁迫(高 Na⁺/Cl⁻)通过离子毒性和渗透压胁迫两个层面影响免疫:
- 离子效应:高盐改变胞质 Ca²⁺ 签名——盐胁迫诱导的 Ca²⁺ 升高可能与 PAMP 诱导的 Ca²⁺ 信号产生交叉干扰,降低免疫 Ca²⁺ 签名的特异性 (Choi et al., 2014)。
- FERONIA 的整合作用:受体激酶 FERONIA 同时参与盐胁迫响应(通过感知细胞壁完整性)和免疫调控(通过 RALF 肽调节 PRR 复合体组装)→ 第3章 3.5节。FERONIA 可能是盐胁迫-免疫信号交汇的一个关键节点 (Feng et al., 2018)。
多重胁迫的协同与拮抗:为什么"组合效应"不是简单的加法
田间的植物很少只面对单一胁迫——更常见的是多重胁迫的同时或序贯打击。理解这些胁迫的组合效应,是将实验室知识转化为田间预测的关键一步:
- 高温 + 干旱:这是气候变化情景下最常见的胁迫组合。高温抑制 SA 防御 → 干旱诱导 ABA 进一步拮抗 SA → 形成对活体营养型病原的"双重削弱"。但同时,高温促进 JA 信号 → 可能增强对坏死营养型病原和昆虫的抗性。这种"输一赢一"的格局暗示:在高温干旱年份,我们应该预期活体营养型病害(锈病、白粉病)加重,而坏死营养型病害(灰霉病)可能减轻。
- 高温 + 高湿:这是另一种在热浪后紧接暴雨时常见的组合。高温已削弱 NLR 功能,而随后的高湿创造了真菌病害的理想条件——形成"窗口期脆弱性"(window of vulnerability)。水稻稻瘟病在高温高湿的夏季台风季节暴发,正是这种组合效应的田间体现。
- 盐胁迫 + 病原侵染:盐胁迫对免疫的影响是病原类型依赖的。盐胁迫增强 ABA 信号 → 部分抑制 SA 防御 → 对细菌更易感;但盐胁迫诱导的渗透保护物质(如脯氨酸)可能抑制某些真菌的生长——再次体现出免疫-环境互作的"非单调性"。
- "胁迫序列"效应:胁迫的时序很重要。先经历高温再遭遇病原,与先感染再遭遇高温,结果可能截然不同——因为高温在感染前削弱免疫,在感染后则可能限制病原(如果病原也是温度敏感的)。极少有研究系统地比较不同胁迫序列对疾病结局的影响,这是未来研究的一个重要空白。
12.4土壤理化性质对免疫的间接影响
土壤的理化性质不直接作用于植物免疫信号通路,但通过影响微生物组组成和营养可用性间接调控免疫输出:
- 土壤 pH:土壤酸碱度显著影响根际微生物群落结构。碱性土壤倾向于富集某些放线菌(Actinobacteria),而酸性土壤富集 Proteobacteria。由于不同微生物类群的 ISR 诱导能力不同,土壤 pH 可以间接影响植物的基础免疫状态。
- 磷可用性:低磷条件下,植物通过 PHR1 调控的磷饥饿响应重塑根际微生物组 (Castrillo et al., 2017) → 第10章 10.2节。同时,低磷胁迫增强 JA 信号并可能抑制 SA 信号——将营养胁迫和免疫信号直接耦合。
- 铁可用性:缺铁诱导的香豆素分泌既是铁获取策略也是微生物组塑造手段 → 第10章 10.6节。铁状态、根际微生物组和免疫之间形成了一个三方耦合网络。
12.5气候变化背景下的植物免疫新挑战
气候变化不是一个遥远的未来问题——它正在以可观测的速度改变植物-病原互作的格局。
温度升高的系统性影响
全球平均温度的持续升高意味着:(1)植物免疫(特别是温度敏感的 NLR 介导抗性)的效率可能下降;(2)病原的地理分布向高纬度和高海拔扩展;(3)病原的世代周转加速,进化速率增加。这三者叠加可能导致当前有效的抗性策略在未来几十年内加速失效 (Velásquez et al., 2018)。
CO₂ 升高与免疫的互作
大气 CO₂ 浓度升高对植物免疫的影响是一个尚不成熟但日益受到关注的领域。初步证据表明:(1)高 CO₂ 可能通过改变 C/N 比来影响 SA 和 JA 合成的前体供应;(2)高 CO₂ 促进气孔关闭(减少 CO₂ 需求),可能间接增强气孔免疫;(3)高 CO₂ 改变叶片碳水化合物组成,可能影响病原的营养获取效率。
极端天气事件与"胁迫序列"效应
气候变化的另一个特征是极端天气事件(热浪、暴雨、干旱)频率和强度增加。这些事件可能导致植物免疫系统在短时间内遭受多重胁迫的同时打击——例如热浪后紧接暴雨可能同时削弱热敏感 NLR 的功能并创造有利于真菌病害的高湿环境。理解"胁迫序列"(stress sequence)对免疫的累积影响,是未来研究的重要方向。
2024–2026 年的综述和实证研究进一步强化了这一关切:Zhao et al. (2024) 系统评估了气候变化下植物病害的地理扩张及其机理基础,证明温度升高、CO₂ 增加和降水模式改变正在系统性地重绘病原地理分布图。Jiang et al. (2025) 在 Communications Biology 上提出了植物多重非生物胁迫整合的最新框架,为理解"高温+干旱+病原"的组合效应提供了系统视角。
能否培育出在28°C以上仍保持高效 NLR 免疫的作物品种?
这个问题直指气候变化背景下植物免疫的核心挑战。策略包括:(1)筛选天然的"温度稳定型"NLR 等位——某些热带作物的 NLR 可能已适应高温环境;(2)通过结构引导的蛋白工程增强 NLR 在高温下的热稳定性;(3)转向不依赖 NLR 的防御策略——如增强 PRR 层抗性或利用 RNA 沉默 → 第14章。
12.6里程碑研究思路拆解
Wang et al. (2011) — 昼夜节律调控免疫时序
面对的问题:免疫为何在一天内存在稳定时段差异?
关键思路:将节律核心节点与病原挑战 readout 联合验证。
关键证据链:节律节点突变会导致防御时序与抗病性同步失衡。
影响:推动”时间维度”进入免疫实验标准设计。
Toyota et al. (2018) — 谷氨酸受体介导的长距离钙信号传播
面对的问题:植物没有神经系统,如何在物理损伤或病原攻击时实现全株范围内的快速信号传播?已知 Ca²⁺ 波可以从损伤位点向远端传播,但介导这种”长距离 Ca²⁺ 信号”的分子传感器是什么?
关键思路:利用表达钙报告基因 GCaMP3 的拟南芥转基因系,结合机械损伤和谷氨酸处理,追踪 Ca²⁺ 波在整株中的传播速度和模式。通过筛选已知配体门控离子通道的突变体,锁定 GLR(Glutamate Receptor-Like)家族作为候选传感器。
关键证据链:(1)机械损伤在数秒内触发从伤口向全株传播的 Ca²⁺ 波,传播速度约 1 mm/s;(2)伤口导致谷氨酸从受损细胞快速释放到质外体;(3)外源施加谷氨酸模拟了损伤触发的 Ca²⁺ 波;(4)glr3.3 glr3.6 双突变体中,Ca²⁺ 波显著减弱——确认 GLR3.3 和 GLR3.6 是主要的谷氨酸感知通道;(5)这些 GLR 在韧皮部中表达,将质外体谷氨酸信号转化为胞内 Ca²⁺ 信号,实现长距离传播。
影响:首次鉴定了植物”长距离 Ca²⁺ 波”的分子传感器,揭示了一种类似动物神经递质信号但使用完全不同的分子元件的快速通讯机制——为理解环境胁迫(包括病原攻击)如何在全株范围内快速协调防御提供了机制基础。
12.7当前争论与未解问题
- 温度敏感 NLR 的共性机制能否预测?
- 环境门控节点在不同作物中是否保守?
- 气候变化背景下如何维持抗性稳定输出?
- 多因子模型能否支持田间级预测?
12.8关键实验方法
| 实验方法 | 用途 | 经典文献 |
|---|---|---|
| 可编程环境舱 | 控制温光条件并测免疫输出 | Wang et al., 2011, Nature |
| 时序转录组 | 解析节律门控防御重编程 | Bhardwaj et al., 2011, Plant J |
| 病原增殖联测 | 连接环境响应与终点抗性 | Velásquez et al., 2018, Curr Biol |
| 多变量统计建模 | 提升田间外推能力 | Desaint et al., 2021, New Phytol |
12.9推荐阅读
🔴 必读
🟡 重要
🟢 拓展
12.10参考文献
- Bomblies K, Lempe J, Epple P, et al. Autoimmune response as a mechanism for a Dobzhansky-Muller-type incompatibility syndrome in plants. PLoS Biol, 2007, 5: e236.
- Campos ML, Yoshida Y, Major IT, et al. Rewiring of jasmonate and phytochrome B signalling uncouples plant growth-defense tradeoffs. Nat Commun, 2016, 7: 12570.
- Castrillo G, Teixeira PJPL, Paredes SH, et al. Root microbiota drive direct integration of phosphate stress and immunity. Nature, 2017, 543: 513–518.
- Choi WG, Toyota M, Kim SH, et al. Salt stress-induced Ca²⁺ waves are associated with rapid, long-distance root-to-shoot signaling in plants. Proc Natl Acad Sci USA, 2014, 111: 6497–6502.
- de Wit M, Spoel SH, Sanchez-Perez GF, et al. Perception of low red:far-red ratio compromises both salicylic acid- and jasmonic acid-dependent pathogen defences in Arabidopsis. Plant J, 2013, 75: 90–103.
- Feng W, Kita D, Peaucelle A, et al. The FERONIA receptor kinase maintains cell-wall integrity during salt stress through Ca²⁺ signaling. Curr Biol, 2018, 28: 666–675.
- Huot B, Castroverde CDM, Velásquez AC, et al. Dual impact of elevated temperature on plant defence and bacterial virulence in Arabidopsis. Nat Commun, 2017, 8: 1808.
- Jiang Z, van Zanten M, Sasidharan R. Mechanisms of plant acclimation to multiple abiotic stresses. Commun Biol, 2025, 8: 700. DOI: 10.1038/s42003-025-08077-w.
- Kim JH, Castroverde CDM, Huang S, et al. Increasing the resilience of plant immunity to a warming climate. Nature, 2022, 607: 339–344. DOI: 10.1038/s41586-022-04902-y.
- Mohr PG, Cahill DM. Suppression by ABA of salicylic acid and lignin accumulation and the expression of multiple genes, in Arabidopsis infected with Pseudomonas syringae. Funct Integr Genomics, 2007, 7: 181–191.
- Mühlenbock P, Szechyńska-Hebda M, Płaszczyca M, et al. Chloroplast signaling and LESION SIMULATING DISEASE1 regulate crosstalk between light acclimation and immunity in Arabidopsis. Plant Cell, 2008, 20: 2339–2356.
- Sugio A, Dreos R, Aparicio F, Maule AJ. The cytosolic protein response as a subcomponent of the wider heat shock response in Arabidopsis. Plant Cell, 2009, 21: 642–654.
- Toyota M, Spencer D, Sawai-Toyota S, et al. Glutamate triggers long-distance, calcium-based plant defense signaling. Science, 2018, 361: 1112–1115.
- Velásquez AC, Castroverde CDM, He SY. Plant-pathogen warfare under changing climate conditions. Curr Biol, 2018, 28: R619–R634.
- Wang W, Barnaby JY, Tada Y, et al. Timing of plant immune responses by a central circadian regulator. Nature, 2011, 470: 110–114.
- Wang Y, Bao Z, Zhu Y, Hua J. Analysis of temperature modulation of plant defense against biotrophic microbes. Mol Plant-Microbe Interact, 2009, 22: 498–506.
- Xin XF, Nomura K, Aung K, et al. Bacteria establish an aqueous living space in plants crucial for virulence. Nature, 2016, 539: 524–529.
- Yang S, Hua J. A haplotype-specific resistance gene regulated by BONZAI1 mediates temperature-dependent growth control in Arabidopsis. Plant Cell, 2004, 16: 1060–1071.
- Zhao Y, Wu J, Liu X, et al. Climate change impacts on plant-pathogen interactions and disease distribution. Annu Rev Phytopathol, 2024, 62: 157–181.
- Zhou M, Wang W, Karapetyan S, et al. High humidity induces stomatal immunity to bacterial pathogens in Arabidopsis. Plant Physiol, 2014, 166: 1533–1540.
- Zhu Y, Qian W, Hua J. Temperature modulates plant defense responses through NB-LRR proteins. PLoS Pathog, 2010, 6: e1000844.